- 176.23 KB
- 2022-04-26 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
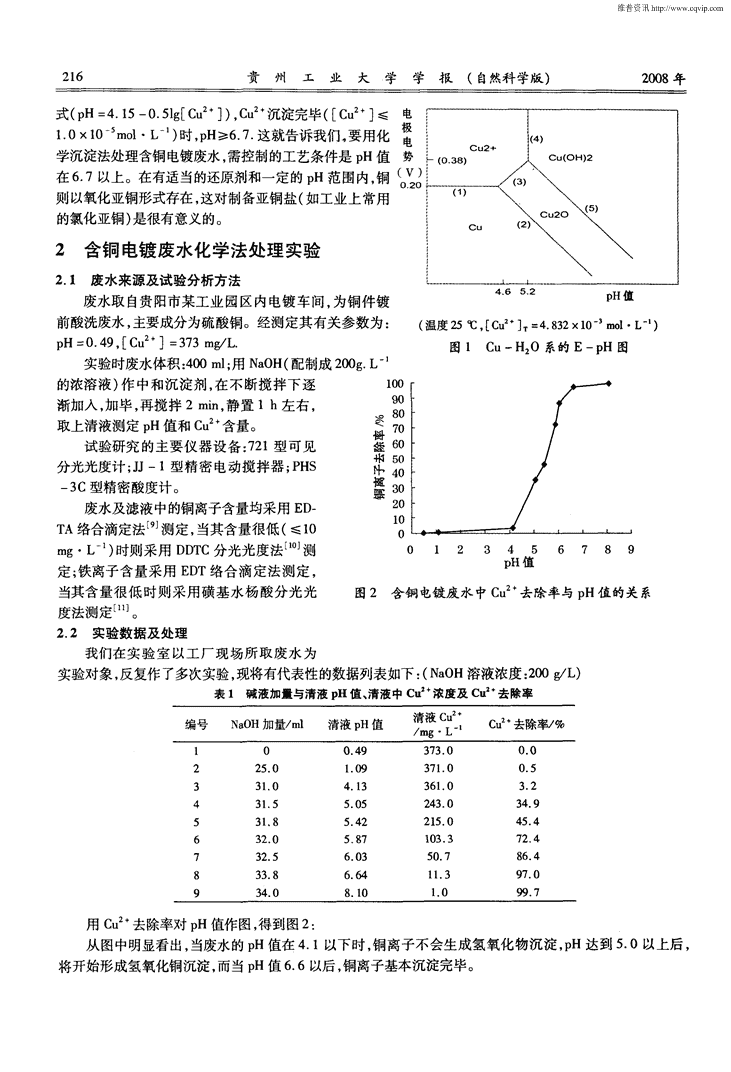
维普资讯http://www.cqvip.com第37卷第3期贵州工业大学学报(自然科学版)Vo1.37No.32008年5月J0URNALOFGUIZHOUUNIVERSnY0FTECHNOLOGYMay.2008NaturalScienceEdition文章编号:1009—0193(2008)03—0214—04Cu—H2O系E—pH图及其在电镀废水处理中的应用刘定富(贵州大学化学工程学院,贵州贵阳550003)摘要:根据电势一pH图可判断有关物相能够稳定存在的条件及相互间反应的趋势,这在湿法冶金、腐蚀与防腐及化工生产中有广泛应用。根据文献数据计算并绘制出cu—H,0系的E—pH图,然后将之用于指导含铜电镀废水处理时工艺条件的选择,并与实验数据进行对比,两者基本吻合,这表明E—pH图对电镀废水处理有实际指导作用。关键词:电势一pH图;电镀废水;Nernst方程;电极电势中图分类号:TQ09;X781.1文献标识码:A0引言电镀是利用电化学方法对金属和非金属的表面进行装饰、防护以获得某些新的性能的一种工艺过程。电镀废水的成分很复杂,其中含有重金属离子、消化物等,有些属于致癌、致畸或致突变的剧毒物质,对人类危害极大。因此,对于电镀废水必须进行治理,清除或减少其对环境的污染。含铜废水是电镀生产中常见且量比较大的一类,对其治理和综合利用国内外进行了许多研究J,目的在于既去除掉废水中有害的二价铜离子,使排放水达标,又回收利用宝贵的金属铜。电势一pH图(简称E—pH图),是比利时腐蚀学家Pourbaix首先提出的。利用热力学数据和电化学原理,对电化学平衡进行一系列计算,可作出金属一水体系在某温度时的电势一pH图或称物质优势范围图。它是一种电化学平衡图,它将体系中全部反应物和生成物的平衡条件以及平衡电极电势、溶液的pH值等变数集中反映在图中,因此从E—pH图上可以判断在给定条件下某化学反应或电化学反应进行的趋势及体系中有关物相稳定存在的条件。根据cu—H0系的主要化学反应及相关热力学数据,计算并绘制出该体系的E—pH图,据以确定含铜电镀废水用化学沉淀法处理时的工艺条件(pH值),并与实验研究结果进行比较。旨在表明电势一pH图对电镀废水处理有实际指导作用。1Cu—H2o系E—pH图的绘制1.1基本原理对任一电极反应:p氧化态+ne—q还原态其Nemst方程式+RT+In()式中:‘P是电极电势;‘P。是该电极反应的标准电极电势;R是普适气体常数;T是热力学温度;n是电极反应中转移的电子数;F是法拉第常数,其数值约为96500C·mol~-[氧化态]和[还原态]分别为氧化态物质和还原态物质的平衡浓度(严格说来应是活度,当溶液很稀时才可用浓度代替之)。若考虑常温(25℃),则上式可简化为:‘P‘P。+0·059161g粉()由(1)式可知,电极电势(‘P)值的大小不仅与电极材料及物质的性质(‘P。)有关,而且与参加电极反应的收稿日期:2008一O2一O5作者简介:刘定富(1962一),男,贵州余庆人,副教授,研究方向:工业废水综合处理。n维普资讯http://www.cqvip.com第3期刘定富:Cu—H:0系E—pH图及其在电镀废水处理中的应用215各物质的浓度、温度有关,在有H或OH一参与的氧化还原反应中,还与溶液的酸度(pH值)有关。电势一pH图就是将各电极反应的电极电势与pH值或pH值与物质浓度的关系在同一张平面图上画出来。根据化学平衡原理和电化学基本理论,对任一化学反应都有:F.,△二=一RTlnK。=一zFE。或K。=exp()式中:△G二是化学反应的标准摩尔吉布斯函数变;K。是反应的标准平衡常数;z是化学反应中转移的电子数;E。是该反应的标准电动势。T1o若只考虑常温(25c【=),则上式可简化成:K。=exP(0.~2569)(2)由(2)式可知,只要得知化学反应的标准电动势,即可求出其平衡常数,反之亦然。1.225℃下Cu—H:O系的重要化学反应及相关热力学数据表1Cu—H:O系的重要化学反应及热力学数据表中有标记的数据是利用有关电极反应的标准电极电势及相关物质的溶度积常数计算的。例如反应(5):2Cu(OH):+2e+2H=Cu:0+3H:0AGo=一2F‘P,可由以下四个反应:2Cu+2e=2Cu(5—1)△Go=一2F‘P2Cu(OH)2=2Cun+40H一(5—2)△Go=一RTln(k(oH))2Cu+20H一=Cu20+H20(5—3)△Go=一RTIn(k印.co)一)2H+2OH一=2H2O(5—4)△Go=一RTIn(k)一加和而得,根据热力学状态函数G的性质有:△Go.=△Go+△+△+△G:即:一2F‘P=一2F‘P一RTIn(k,c(0H):2一RTln(k,co)一一RThl(k)(3)从有关手册中查出25c【=时Cu(OH):和Cu:0的k(溶度积常数)分别是2.0×10一、和2.0×10.水的离子积常数(25c【=)k为1.0×10-14.在T:298.15k,R=8.315J.K~.mol下,将这些值代入(3)式中,可得出:‘P=‘P:+0.059161ogk即,c(0H)一0.059161og(k即.co)一0.059161ogk=0.69伏。反应(2)和(3)的标准电极电势亦可用同样方法求出。1.3Cu—H20系的E—pH图根据表l中数据,以电极电势(E)为纵坐标,pH值为横坐标,在同一张图上将反应(1)一(5)所对应的关系式绘制出来(作图时尤其要注意各条曲线的交点及其物理意义)即得到Cu—H:0系的电势一pH图。图中每条线的编号与表1中相同,为便于讨论问题,标出了主要点的电势值和pH值以及各个区域内稳定存在的物相。实际情况要复杂得多,Cu(OH):只有在7Oc【=以下才是稳定的,当温度高于7Oc【=时,它将分解转化成CuO;在适当条件下,二价铜离子也可以被还原成亚铜离子,并以CuOH形式存在,但极不稳定,温度大于35c【=即分解成Cu:0-8J,故图中没有标出CuOH稳定存在的区域。从图1明显看出,当溶液的pH值小于5.2且体系中没有适当的还原剂时,铜以二价离子状态存在,如果加入碱调节溶液的酸度,当pH值达到5.2以上后,将形成氢氧化铜(Ⅱ)沉淀;根据反应(4)及相应的关系n维普资讯http://www.cqvip.com216贵州工业大学学报(自然科学版)2008年式(pH=4.15—0.5lg[Cu]),cu沉淀完毕([cu]≤电1.0×10。。mol·L)时,pH>~6.7.这就告诉我们,要用化I(4)CU2+{学沉淀法处理含铜电镀废水,需控制的工艺条件是pH值势-(0.38)2在6.7以上。在有适当的还原剂和一定的pH范围内,铜ln则以氧化亚铜形式存在,这对制备亚铜盐(如工业上常用(’)\\\c2。’的氯化亚铜)是很有意义的。cu(2)\\2含铜电镀废水化学法处理实验\\\2.1废水来源及试验分析方法废水取自贵阳市某工业园区内电镀车间,为铜件镀前酸洗废水,主要成分为硫酸铜。经测定其有关参数为:(温度25℃,[cu]T=4.832×i0一mol·L)pH:O.49,[cu]=373mg/L.图1Cu—H20系的E—pH图实验时废水体积:400ml;用NaOH(配制成200g.L的浓溶液)作中和沉淀剂,在不断搅拌下逐】渐加入,加毕,再搅拌2min,静置1h左右,∞5;∞∞∞∞{;}mO取上清液测定pH值和Cu含量。试验研究的主要仪器设备:721型可见分光光度计;JJ一1型精密电动搅拌器;PHSr,t-’,一3c型精密酸度计。罄废水及滤液中的铜离子含量均采用ED—TA络合滴定法[9测定,当其含量很低(≤1Omg·L)时则采用DDTC分光光度法I1。测0l23456789pH值定;铁离子含量采用EDT络合滴定法测定,当其含量很低时则采用磺基水杨酸分光光图2含铜电镀废水中Cu去除率与pH值的关系度法测定“。2.2实验数据及处理我们在实验室以工厂现场所取废水为实验对象,反复作了多次实验,现将有代表性的数据列表如下:(NaOH溶液浓度:200g/L)表1碱液加量与清液pit值、清液中C浓度及C去除率用cu去除率对pH值作图,得到图2:从图中明显看出,当废水的pH值在4.1以下时,铜离子不会生成氢氧化物沉淀,pH达到5.O以上后,将开始形成氢氧化铜沉淀,而当pH值6.6以后,铜离子基本沉淀完毕。n维普资讯http://www.cqvip.com第3期刘定富:Cu—H0系E—pH图及其在电镀废水处理中的应用2173讨论确定Cu—H0系中的主要化学反应及相应的热力学数据后,可以绘制出其E—pH图,从图上可以知道该体系中各种物相稳定存在的条件(pH值范围),以及不同物相间的反应趋势和f条件。因此可以利用E—pH图来指导含铜电镀废水化学沉淀法处理时工艺条件(pH值)的选择,由此确定的条件是pH值为6.7以上;通过实验研究,我们得出含铜电镀废水用化学沉淀法处理时,铜离子沉淀完毕的条件是pH值需控制在6.6以上。可见两者基本吻合。此外,通过E—pH图我们可以知道体系中有关物相稳定存在的条件(氧化剂或还原剂的‘p。值及体系的pH值),这对化合物的制备很重要。尽管我们所讨论的体系比较简单,但却清楚地表明,E—pH图不仅在湿法冶金、腐蚀与防腐和化工生产中有重要应用,而且在电镀废水的治理及物质的制备中也有实际指导意义。参考文献:[1]陈凡植,张岸飞,陈淦康,等.含铜含镍电镀污泥的综合利用[J].环境与开发,2001,16(1):21—22,25.[2]毛谙章.电镀污泥中铜的回收[J].化工技术与开发,2004,33(2):45—47,16.[3]A.H.M.Veeken,H.V.M.Hamelers.Removalofheavymetalsfromsewagesludgebyextractionwithorganicacids[J].Wat.Sci.Tech.1999,40(1):129—136.[4]I.Dobrevsky,M.Dimova—Todorova,T.Panayotova.Eleetroplatingrinsewastewatertreatmentbyionexchange[J].Desali—as-tion,1996,(108):277—280.[5]天津大学物理化学教研室.物理化学(第三版,下册)[M].北京:高等教育出版社,1992.[6]傅崇说.有色冶金原理[M].北京:冶金工业出版社,1984.[7]中南矿冶学院分析化学教研室.分析化学手册[M].北京:科学出版社,1982.[8]李首代,冯丽娟,李景峰.常温下氢氧化亚铜的合成[J].天津化工,2004,18(5):43—44.[9]徐红娣.电镀溶液分析技术[M].北京:机械工业出版社,1993:98—99.[10]刘颖,李佳,王颖.二乙基二硫代氨基甲酸钠水相光度法测定微量铜(Ⅱ)[J].广东微量元素科学,1999,6(7):64—66.[11]李文莉,熊金平,张延东.酸性镀铜溶液中铁含量的测定[J].河北化工,1995,(4):51—53.E-pHDiagramofCu-H20SystemandApplicationinTreatmentofElectroplatingWasteWaterLIUDing—fu(SchoolofChemicalEngineering,GuizhouUniversity,Guiyang550003,China)Abstract:theconditionofsteady—goingpresenceandtrendofreactioneachotherforrelationalsubstancecanbejudgedfrompotential—pHdiagram,Thisiswidelyappliedinchemicalproduction,corrosionandanticorrosion,hydrometallurgy.Inthisarticle,thepotential—pHdiagramofCu—H2Osystemwasdrawnbymeansofdataofliteratureoraccount,thenitwasappHedtoconfi1211thesuitabletechnicalconditionwhentreatmentofelectroplatlngwastewatercontainscopper。Theresultfrompotential—pHdiagrammatcheswellwiththeexperimentalresult,whichindicatesthattheelectricpotential—pHdiagramcanbeausefulguid.ancetotreatmenttotheelectroplatingwastewater。Keywords:electricpotential—pHdiagram;electropladngwastewater;Nemstequation;electrodepotential