- 166.38 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
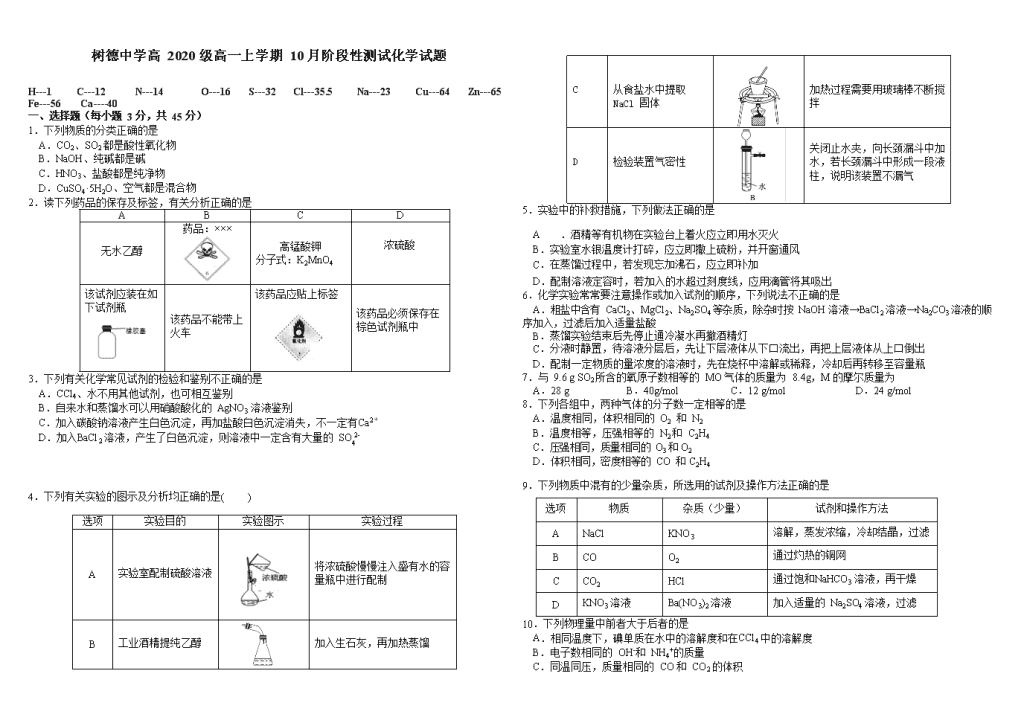
树德中学高 2020 级高一上学期 10 月阶段性测试化学试题
H---1
C---12
N---14
O---16
S---32
Cl---35.5
Na---23
Cu---64
Zn---65
Fe---56
Ca 40
一、选择题(每小题 3 分,共 45 分)
1.下列物质的分类正确的是
A.CO2、SO2 都是酸性氧化物
B.NaOH、纯碱都是碱
C.HNO3、盐酸都是纯净物
D.CuSO4·5H2O、空气都是混合物
2.读下列药品的保存及标签,有关分析正确的是
A
B
C
D
无水乙醇
药品:×××
高锰酸钾 分子式:K2MnO4
浓硫酸
该试剂应装在如下试剂瓶
该药品不能带上火车
该药品应贴上标签
该药品必须保存在棕色试剂瓶中
3.下列有关化学常见试剂的检验和鉴别不正确的是
A.CCl4、水不用其他试剂,也可相互鉴别
B.自来水和蒸馏水可以用硝酸酸化的 AgNO3 溶液鉴别
C.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,不一定有Ca2+
4
D.加入BaCl2 溶液,产生了白色沉淀,则溶液中一定含有大量的 SO 2-
C
从食盐水中提取
NaCl 固体
加热过程需要用玻璃棒不断搅拌
D
检验装置气密性
关闭止水夹,向长颈漏斗中加水,若长颈漏斗中形成一段液柱,说明该装置不漏气
5.实验中的补救措施,下列做法正确的是
A.酒精等有机物在实验台上着火应立即用水灭火
B.实验室水银温度计打碎,应立即撒上硫粉,并开窗通风
C.在蒸馏过程中,若发现忘加沸石,应立即补加
D.配制溶液定容时,若加入的水超过刻度线,应用滴管将其吸出
6.化学实验常常要注意操作或加入试剂的顺序,下列说法不正确的是
A.粗盐中含有 CaCl2、MgCl2、Na2SO4 等杂质,除杂时按 NaOH 溶液→BaCl2 溶液→Na2CO3 溶液的顺序加入,过滤后加入适量盐酸
B.蒸馏实验结束后先停止通冷凝水再撤酒精灯
C.分液时静置,待溶液分层后,先让下层液体从下口流出,再把上层液体从上口倒出
D.配制一定物质的量浓度的溶液时,先在烧杯中溶解或稀释,冷却后再转移至容量瓶7.与 9.6 g SO2 所含的氧原子数相等的 MO 气体的质量为 8.4g,M 的摩尔质量为
A.28 g B.40g/mol C.12 g/mol D.24 g/mol
8.下列各组中,两种气体的分子数一定相等的是
A.温度相同,体积相同的 O2 和 N2
B.温度相等,压强相等的 N2 和 C2H4
C.压强相同,质量相同的 O3 和O2
D.体积相同,密度相等的 CO 和C2H4
9.下列物质中混有的少量杂质,所选用的试剂及操作方法正确的是
4.下列有关实验的图示及分析均正确的是( )
选项
实验目的
实验图示
实验过程
A
实验室配制硫酸溶液
将浓硫酸慢慢注入盛有水的容量瓶中进行配制
B
工业酒精提纯乙醇
加入生石灰,再加热蒸馏
选项
物质
杂质(少量)
试剂和操作方法
A
NaCl
KNO3
溶解,蒸发浓缩,冷却结晶,过滤
B
CO
O2
通过灼热的铜网
C
CO2
HCl
通过饱和NaHCO3 溶液,再干燥
D
KNO3 溶液
Ba(NO3)2 溶液
加入适量的 Na2SO4 溶液,过滤
10.下列物理量中前者大于后者的是
A.相同温度下,碘单质在水中的溶解度和在CCl4 中的溶解度
B.电子数相同的 OH-和 NH4+的质量
C.同温同压,质量相同的 CO 和 CO2 的体积
D.相同质量的 Zn 和 Fe 与足量稀硫酸反应,产生H2 的质量
11.设 NA 表示阿伏加德罗常数的值,下列说法正确的是
A.在标准状况下,22.4 L CH4 和 CO2 的混合气体中碳原子数为 2NA
B.在标准状况下,NA 个H2O 分子的质量为 18g
C.在常温下,把 100 g CaCO3 加到少量水中,所得溶液中的Ca2+ 数等于 NA
D.0.2 mol·L-1 的硫酸铝溶液中含有 Al3+数目为 0.4NA
12.常温下下列离子的物质的量浓度与 100 mL 1 mol/L Na2CO3 溶液所含Na+的物质的量浓度相同的是A.10.6g Na2CO3 在烧杯中加 100 mL 水溶解配成溶液的 Na+
2-
B.1000 mL 0.1 mol/L MgCl2 溶液中的 Cl- C.200 mL 1mol/L CaCl2 溶液中 Cl- D.100 g 1 mol/LH2SO4 溶液中的 SO4
13.现有 V L 0.5 mol·L-1 的盐酸,欲将其浓度扩大一倍,以下方法中最宜采用的是( )
A.加热浓缩到原来体积的一半
B.加入 5 mol·L-1 的盐酸 0.125V L
C.加入 10 mol·L-1 的盐酸 0.1V L,再稀释至 1.5V L
D.通入 11.2 L 氯化氢气体
14.有 BaCl2 和 NaCl 的混合溶液 aL,将它均分成两.份.。一份滴加稀硫酸,使 Ba2+离子完全沉淀,消耗xmol H SO ;另一份滴加 AgNO 溶液,使 Cl-离子完全沉淀,消耗 ymol AgNO 。则原混合溶液中 c(Na+)
(2)步骤①操作名称为 ,若将苯加入碘水中,振荡静置后,上层液体颜色为
(3)步骤②需要上述仪器中的 (填序号),该实验操作名称为 。
(4)步骤③需要上述仪器中的 (填序号),该实验操作名称为 。
(5)步骤④需要上述仪器中的 (填序号),该仪器名称为 。
17.(13 分)下图是硫酸试剂瓶标签上的内容,阅读并填以下空白。
(1)某兴趣小组需要配制2.5 mol/L 的稀硫酸溶液90 mL 所需要的步骤如下:
① 计算,经计算需要用量筒量取 mL 的该浓硫酸;
② 量取,用 mL 量筒量取浓硫酸(量程:10mL,25mL,50mL);
③ 溶解稀释,将浓硫酸沿烧杯壁倒入水中,并用玻璃棒不断搅拌;
2 4 3
3 ;
A.(y-2x)/a mol·L-1 B.2(y-x)/a mol·L-1 C.(2y-2x)/a mol·L-1 D.(2y-4x)/a mol·L-1
15.相对分子质量为 M 的气态化合物 VL(标准状况)溶于 mg 水中,溶液的质量为 Xg,质量分数为 ω%, 物质的量浓度 cmol/L,密度为 ρg/cm3(ρ>1),则下列说法正确的是
A.溶液的质量分数 ω%可表示为: MV
22.4m
rV
B.物质的量浓度C 可表示为:
MV + 22.4m
C.向上述溶液中再加入 Xg 水后,所得溶液的物质的量浓度小于 0.5cmol/L
D.溶液密度ρ 可表示为: cM
1000w
二、非选择题(共 55 分)
16.(14 分)按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
(1)下列仪器中,使用时必须检查是否漏水的有 (填仪器序号)。
④转移,将冷却后的溶液转移到 中,玻璃棒的作用为
⑤ 洗涤,把稀释用的玻璃棒和烧杯洗涤 2~3 次,将洗涤液一并倒入废液缸中;
⑥ 定容,所用的主要玻璃仪器为 ;
⑦ 。
以上操作中有明显错误的一项为 (填序号)。
(2)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是 。
A.量取浓硫酸时,仰视读数
B.洗涤量取浓H2SO4 后的量筒,并将洗涤液转移到容量瓶中
C.定容时仰视观察液面
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
E.容量瓶不干燥
(3)若该稀 H2SO4 的质量分数为 a%,将其蒸发掉一定量的水,使其浓度升高为5 mol/L,质量分数为 b%, 则 a、b 的关系为:b 2a(填“>”“<”或“=”)
(4)酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有 NaHSO4、
KH2PO4、K2HPO4 等。已知 H3PO2 次磷酸与足量的NaOH 反应只生成一种盐NaH2PO2,该盐属于
(“正盐”或“酸式盐”),H3PO2 属于 元酸
18.(14 分)某试剂瓶中 FeSO4 溶液中含有少量 NaCl、Na2SO4 、CuSO4 和NaNO3 ,请选择适当的试剂除
(3)实验测得反应后A 室混合气体的质量为 48g,则该混合气体的密度是同温同压条件下氢气密度的
去杂质,从而得到纯净的NaNO3 晶体和 FeSO4·7H2O 晶体,相应的实验流程如图所示。 倍,X 的摩尔质量为 。
(4)若在 A 室加入足量碱石灰(碱石灰可吸收 CO2 和 H2O,忽略固体所占体积),保持温度不变,最终活塞停留的位置在 刻度,此时容器内气体压强与加碱石灰前气体压强之比为 。
实验室只提供如下试剂:Ca(OH)2 溶液,NaOH 溶液,AgNO3 溶液,BaCl2 溶液,稀HNO3,稀H2SO4,铁粉,铜粉,锌粒
请回答下列问题:
- - 2-
(1)若该混合溶液中,测得 Fe2+浓度为 2 mol/L,Cu2+、Na+ 、NO3 、Cl 浓度均为 1mol/L,则 c(SO4 )=
mol/L
(2)若沉淀 A 是Cu(OH)2、Fe(OH)2 的混合物,写出实验流程中下列加入试剂的化学式:X 。
(3)向溶液 4 加入试剂 a,发生反应的化学方程式为 ,通过过滤、洗涤的到溶液 5,如何证明固.体.混.合.物.已洗净 。
(4)步骤④中涉及的操作是: 、 、过滤、洗涤、干燥
(5)上述实验步骤③中加入过量 Na2CO3 溶液的目的是 。
(6)向溶液 3 中加入适量的 (填化学式),再结晶,从而获得NaNO3 晶体。
19.(14 分)某容积固定的密闭容器由可移动的活塞隔成A、B 两室,向B 室充入 1 molN2,A 室加入一定量的X 固体,加热,发生化学反应2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。
(1) A 室混合气体的物质的量为 ,生成的 CO2 在标况下的体积为 。
(2)Y 是一种极易溶于水的有刺激性气味气体,实验室需要进行尾气处理,下列装置可用于作为Y 气体的尾气处理装置的是: 。
A
B
C
D
E
高一化学 2020-10 阶考 第 3 页 共 3 页
树德中学高 2020 级高一上学期 10 月阶段性测试化学试题【答案】
1-15:ABDDB BCDCC BCCDC
16(12 分)
(1)③④(2 分)
(2)过滤(1 分) 紫红色(1 分)
(3)④(1 分) 分液(1 分)
(4)①(1 分) (降温)结晶(1 分)
(5)⑤⑥(2 分) 蒸馏烧瓶 (1 分) (直形)冷凝管(1 分)
17(15 分)(1)13.6(2 分) 25 (1 分) 100ml 容量瓶(1 分) 引流(1 分) 胶头滴管
(1 分) 摇匀(1 分) ⑤(1 分)
(2)AB(2 分)
(3)<(2 分)
(4)正盐 (2 分) 一(1 分)
18(14 分)
(1)2.5(2 分)
(2) NaOH(2 分)
(3) Fe+CuSO4=FeSO4+Cu (2 分) 取最后一次洗涤液,加入少量 BaCl2 溶液,若无明显现象则已经洗净。(2 分)
(4)蒸发浓缩(1 分) 冷却结晶(1 分)
(5)除去过量的 Ag+、Ba2+(2 分)
(6)HNO3 (2 分)
19(14 分)
(1)2mol(2 分) 11.2L(2 分)
(2)ACD(2 分)
(3)12(2 分) 96g/mol(2 分)
(4)3 (2 分) 2:3(2 分)