- 340.93 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
课时规范练4 离子反应
一、选择题(本题共10小题,每小题6分,共60分。每小题只有一个选项符合题目要求)
1.下列说法中正确的是( )
A.氯化钠水溶液在电流的作用下电离出Na+和Cl-
B.硫酸钡难溶于水,但硫酸钡属于强电解质
C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
D.硫酸钠在水中的电离方程式可表示为Na2SO42Na++S6++4O2-
2.(2019湖北襄阳五中周测)能正确表示下列反应的离子方程式的是( )
A.硫酸铝溶液中加入过量氨水:Al3++3OH-Al(OH)3↓
B.碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CCaCO3↓+2OH-
C.冷的氢氧化钠溶液中通入氯气:Cl2+2OH-ClO-+Cl-+H2O
D.稀硫酸中加入铁粉:2Fe+6H+2Fe3++3H2↑
3.(2018江苏化学,4)室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 KI溶液:Na+、K+、ClO-、OH-
B.0.1 mol·L-1 Fe2(SO4)3溶液:Cu2+、N、N、S
C.0.1 mol·L-1 HCl溶液:Ba2+、K+、CH3COO-、N
D.0.1 mol·L-1 NaOH溶液:Mg2+、Na+、S、HC
4.(2019河南周口月考)下列解释事实的化学方程式或离子方程式正确的是( )
A.钢铁发生吸氧腐蚀:2Fe+O2+2H2O2Fe2++4OH-
B.SO2使紫色石蕊溶液变红色:SO2+H2O2H++S
C.利用NaOH溶液除去金属铝表面的氧化膜:Al2O3+2OH-2Al+H2O
D.向次氯酸钠溶液中通入足量的SO2气体:ClO-+SO2+H2OHClO+HS
5.下列各组离子或物质是否能够大量共存的评价及离子反应方程式书写均正确的是( )
选项
粒子组
评价
A
无色溶液中:Na+、Al3+、S、C
不能大量共存,因为有沉淀和气体生成
2Al3++C+3H2O2Al(OH)3↓+CO2↑
B
中性溶液中:Fe3+、N、S2-、N
不能大量共存,因为有沉淀生成
2Fe3++3S2-Fe2S3↓
C
澄清溶液中:K+、Cu2+、Cl-、NH3·H2O
不能大量共存,因为有沉淀生成
Cu2++2OH-Cu(OH)2↓
D
酸性溶液中:Fe2+、Al3+、S、I-
能大量共存于同一溶液中
6.某溶液含有K+、Fe3+、S、C、I-中的几种。取样,滴加KSCN溶液后显血红色。下列有关原溶液的说法不正确的是( )
A.一定存在的离子为Fe3+、S
B.一定不存在的离子为C、I-
C.不能确定的离子为K+、S
D.确定是否含有K+需要经过焰色反应
7.(2019广西桂林高三起点测试)常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使酚酞显红色的溶液中:Na+、Al3+、S、Cl-
B.=1×1012的溶液中:N、Na+、C、Si
C.c(Fe2+)=1 mol·L-1的溶液中:Mg2+、H+、Mn、S
D.无色透明溶液中:K+、Ca2+、Cl-、HC
8.(2019浙江温州月考)某溶液中可能含有K+、Na+、Mg2+、N、Fe2+、Br-、C、S、S中的若干种离子。某同学做了如下实验:
①取少量溶液,滴加足量氯水,有气泡产生且溶液颜色变成黄色
②另取少量溶液,滴加盐酸酸化的氯化钡溶液,无沉淀生成
③蘸取原溶液做焰色反应,透过蓝色钴玻璃观察到火焰呈紫色。
为进一步确定该溶液的组成,无需进行的实验是( )
A.上述实验③不透过蓝色钴玻璃观察火焰颜色
B.取少量溶液,滴加氯水和CCl4,振荡、静置
C.取少量溶液,滴加适量的稀硫酸和品红溶液
D.取少量溶液,滴加适量的NaOH浓溶液,加热,用湿润的红色石蕊试纸检验气体
9.(2019重庆七中月考)甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH-、Cl-、HC离子中的两种构成,可以发生如图转化:
下列说法不正确的是( )
A.在甲中滴加丁可能发生反应:HC+Ba2++OH-BaCO3↓+H2O
B.溶液丙中还可以大量共存的离子有:I-、N、S
C.白色沉淀A可溶解在溶液D中
D.甲为NaHCO3,乙为AlCl3
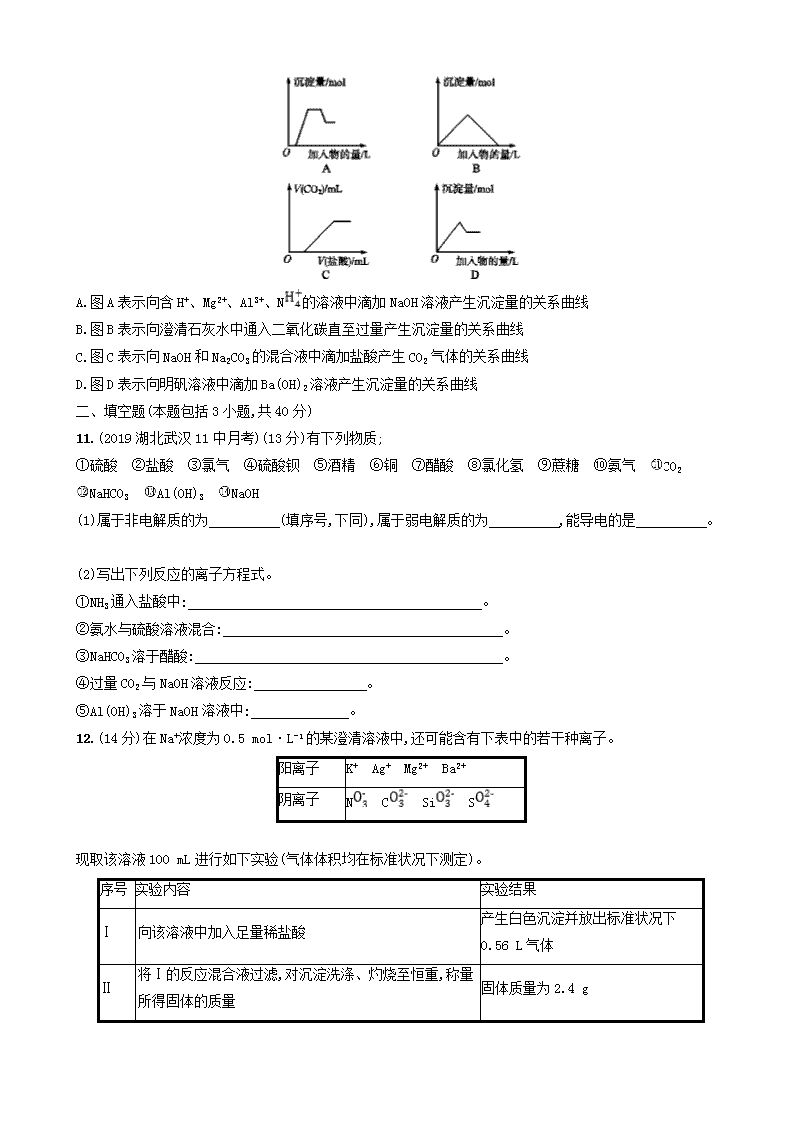
10.下列图像中的曲线(纵坐标为生成沉淀或气体的量,橫坐标为加入物的量),其中错误的是( )
A.图A表示向含H+、Mg2+、Al3+、N的溶液中滴加NaOH溶液产生沉淀量的关系曲线
B.图B表示向澄清石灰水中通入二氧化碳直至过量产生沉淀量的关系曲线
C.图C表示向NaOH和Na2CO3的混合液中滴加盐酸产生CO2气体的关系曲线
D.图D表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀量的关系曲线
二、填空题(本题包括3小题,共40分)
11.(2019湖北武汉11中月考)(13分)有下列物质;
①硫酸 ②盐酸 ③氯气 ④硫酸钡 ⑤酒精 ⑥铜 ⑦醋酸 ⑧氯化氢 ⑨蔗糖 ⑩氨气 CO2
NaHCO3 Al(OH)3 NaOH
(1)属于非电解质的为 (填序号,下同),属于弱电解质的为 ,能导电的是 。
(2)写出下列反应的离子方程式。
①NH3通入盐酸中: 。
②氨水与硫酸溶液混合: 。
③NaHCO3溶于醋酸: 。
④过量CO2与NaOH溶液反应: 。
⑤Al(OH)3溶于NaOH溶液中: 。
12.(14分)在Na+浓度为0.5 mol·L-1的某澄清溶液中,还可能含有下表中的若干种离子。
阳离子
K+ Ag+ Mg2+ Ba2+
阴离子
N C Si S
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
序号
实验内容
实验结果
Ⅰ
向该溶液中加入足量稀盐酸
产生白色沉淀并放出标准状况下0.56 L气体
Ⅱ
将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体的质量
固体质量为2.4 g
Ⅲ
向Ⅱ的滤液中滴加BaCl2溶液
无明显现象
请回答下列问题。
(1)实验Ⅰ能确定一定不存在的离子是 。
(2)实验Ⅰ中生成沉淀的离子方程式为 。
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果;一定不存在的离子填“0”;不能确定是否存在的离子填“?”)。
阴离子
N
C
Si
S
c/(mol·L-1)
(4)判断K+是否存在,若存在,求其最小浓度,若不存在,说明理由: 。
13.(13分)现有五种可溶性物质,A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、N、C、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是 和 (填化学式,且相对分子质量较小的写在第一个空)。
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质记为C,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时,产生棕黄色沉淀(红白混合颜色),向该沉淀中滴入稀硝酸,沉淀部分溶解,最后留有白色沉淀不再溶解。则X为 。
A.S B.S
C.CH3COO- D.Si
(3)B的水溶液不显中性,原因为 (用离子方程式表示)。
(4)将0.02 mol A与0.01 mol C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的质量为 (保留两位有效数字)。
(5)将Cu投入到装有D溶液的试管中,Cu不溶解,再滴加稀硫酸,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的 (填相应的离子符号)。有关反应的离子方程式为 。
(6)利用上述已经确定的物质,可能检验出D、E中的阳离子。请简述实验操作步骤、现象及结论: 。
课时规范练4 离子反应
1.B 电离的条件是溶于水或受热熔化而不是通电,A项错误;硫酸钡难溶于水,但溶于水的部分完全电离,所以硫酸钡属于强电解质,B项正确;二氧化碳溶于水生成的碳酸能部分电离,故碳酸属于弱电解质,而二氧化碳属于非电解质,C项错误;硫酸钠在水中的电离方程式可表示为Na2SO42Na++S,D项错误。
2.C NH3·H2O为弱电解质,在离子方程式中不能拆,应写分子式,A错误;澄清石灰水中Ca(OH)2完全电离为Ca2+和OH-,与Na2CO3反应的离子方程式为Ca2++CCaCO3↓,B错误;稀硫酸中的H+只能将Fe氧化为Fe2+,D错误。
3.B ClO-具有强氧化性,能氧化I-,A项错误;CH3COO-能与H+结合生成CH3COOH,C项错误;Mg2+易与OH-结合生成Mg(OH)2沉淀,HC与OH-反应生成C和H2O,D项错误。
4.C 钢铁发生吸氧腐蚀的总反应式为2Fe+O2+2H2O2Fe(OH)2,A项错误;SO2溶于水生成的亚硫酸是弱电解质,在溶液中分步电离,其第一步电离方程式为:H2SO3H++HS,B项错误;因为Al2O3具有两性,既能与强酸反应,又能与强碱反应,C项正确;ClO-与SO2易发生氧化还原反应,即ClO-+SO2+H2O2H++Cl-+S,D项错误。
5.D A项离子方程式没有配平,应该是2Al3++3C+3H2O2Al(OH)3↓+3CO2↑,错误;铁离子氧化硫离子生成单质硫和亚铁离子,不能大量共存,B项错误;一水合氨是弱电解质,应该用化学式表示,C项错误;D项四种离子间不发生反应,可以大量共存,正确。
6.C 滴加KSCN溶液后显血红色,说明原溶液中一定含有Fe3+,Fe3+与C能发生相互促进的水解反应而不能大量共存,Fe3+与I-能发生氧化还原反应而不能大量共存,故原溶液中一定不含C、I-,根据溶液呈电中性可知,原溶液中一定含S,而K+需要经过焰色反应才能确定其是否存在,A、B、D正确,C错误。
7.D 使酚酞显红色的溶液呈碱性,Al3+与OH-发生反应不能大量共存,A错误;根据c(H+)×c(OH-)=10-14,=1×1012,可以得到c(H+)=0.1 mol·L-1,则溶液显酸性,C、Si都能与H+反应,不能大量共存,B错误;Fe2+具有还原性,Mn在酸性条件下能氧化Fe2+,所以H+、Mn、Fe2+三者不能大量共存,C错误;无色透明溶液中:K+、Ca2+、Cl-、HC四种离子相互不反应,能大量共存,D正确。
8.B ①滴加足量氯水,有气泡产生,则溶液中含有C,因此溶液不可能含有Mg2+和Fe2+;溶液颜色变成黄色,可证明是Br-被氯水氧化为Br2所致,即溶液中含有Br-;②加盐酸酸化的氯化钡溶液,无沉淀生成,则不含S;实验③说明含有K+。由此可知,需要进一步检验Na+、N和S。不透过蓝色钴玻璃观察火焰颜色,可以确定是否含有Na+,即A需要;滴加氯水和CCl4,振荡、静置,是利用氧化后萃取的方法检验是否含有Br-,但实验①可以确定含有Br-,所以B不需要;滴加适量的稀硫酸和品红溶液,用于检验是否含有S,故C需要;加NaOH浓溶液,加热,用湿润的红色石蕊试纸检验气体,可以确定是否含有N,故D也需要。正确答案为B。
9.B 甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH-、Cl-、HC的两种离子构成,依据离子能大量共存的原则得出甲、乙、丙、丁中含有两种物质,即HCl和AlCl3。因为甲溶液能和乙溶液反应生成白色沉淀A、无色气体B和NaCl,故甲和乙中含有能发生相互促进水解的离子,即Al3+和HC,生成的气体B为CO2,沉淀A为Al(OH)3,然后依据甲与丙反应生成无色气体B,则可推出甲为NaHCO3、乙为AlCl3,甲与丁反应生成白色沉淀C,则C为BaCO3,丁为Ba(OH)2,丙为HCl。当Ba(OH)2过量时,与NaHCO3反应的离子方程式为HC+Ba2++OH-BaCO3↓+H2O,A正确;丙为HCl,N、H+与I-因发生氧化还原反应而不能大量共存,B错误;白色沉淀A为Al(OH)3,能溶于强碱溶液中,C正确;根据上述分析可知D正确。
10.C A项,结合OH-的能力:H+>Al3+,Mg2+>N,发生反应:H++OH-H2O,Al3++3OH-Al(OH)3↓,Mg2++2OH-Mg(OH)2↓,N+OH-NH3·H2O,Al(OH)3+OH-Al+2H2O,故正确;B项发生的反应是:CO2+Ca(OH)2CaCO3↓+H2O,CaCO3+CO2+H2OCa(HCO3)2,故正确;C项发生的反应是2NaOH+CO2Na2CO3+H2O,Na2CO3+HClNaCl+NaHCO3,NaHCO3+HClNaCl+CO2↑+H2O,生成气体前消耗的盐酸的体积大于生成气体消耗的盐酸,故错误;D项发生的离子反应:2Al3++3S+3Ba2++6OH-2Al(OH)3↓+3BaSO4↓,继续滴加Ba(OH)2溶液,发生反应2Al(OH)3+S+Ba2++2OH-BaSO4↓+2Al+4H2O,故正确。
11.答案 (1)⑤⑨⑩ ⑦ ②⑥
(2)①NH3+H+N
②NH3·H2O+H+N+H2O
③HC+CH3COOHCH3COO-+CO2↑+H2O
④CO2+OH-HC
⑤Al(OH)3+OH-Al+2H2O
12.答案 (1)Ag+、Mg2+、Ba2+
(2)Si+2H+H2SiO3↓
(3)
阴离子
N
C
Si
S
c/(mol·L-1)
?
0.25
0.4
0
(4)存在,最小浓度为0.8 mol·L-1
解析 由题知溶液为透明澄清溶液,因此溶液中的离子必能大量共存。由实验Ⅰ可知,加入足量稀盐酸产生气体,必有C,其浓度为0.56 L÷22.4 L·mol-1÷0.1 L=0.25 mol·L-1,则溶液中一定无Ag+、Mg2+、Ba2+;能生成白色沉淀,因此有Si,发生的反应为Si+2H+H2SiO3↓,灼烧后得到固体SiO2,则Si的浓度为2.4 g÷60 g·mol-1÷0.1 L=0.4 mol·L-1;由实验Ⅲ可知溶液中不含S;根据电荷守恒知2c(C)+2c(Si)=2×0.25 mol·L-1+2×0.4 mol·L-1=1.3 mol·L-1>0.5 mol·L-1,因此必有K+,K+浓度至少为0.8 mol·L-1,不能确定是否含有N。
13.答案 (1)Na2CO3 Ba(OH)2 (2)B
(3)C+H2OHC+OH- (4)6.1 g
(5)N 3Cu+8H++2N3Cu2++2NO↑+4H2O
(6)向D的溶液中逐滴加入Ba(OH)2溶液直至过量,若先出现白色沉淀后又逐渐溶解,则D中含有Al3+,E中含有Mg2+(或向D的溶液中加入适量的Na2CO3溶液,若产生了白色沉淀和无色无味的气体,则D中含有Al3+,E中含有Mg2+)
解析 (1)根据题意,C只能与Na+相结合,因此一定含有Na2CO3。此时OH-只能与Ba2+结合,所以一定还含有Ba(OH)2。(2)当C与B的溶液混合时,产生红褐色沉淀和无色无味气体,红褐色沉淀是Fe(OH)3,无色无味的气体一定是CO2,所以B是Na2CO3,C中含有Fe3+;当C与A的溶液混合时产生棕黄色沉淀(红白混合颜色),向该沉淀中滴入稀硝酸,沉淀部分溶解,最后留有白色沉淀不再溶解,这说明A是Ba(OH)2,C中还含有S,因此C是Fe2(SO4)3。(3)Na2CO3是强碱弱酸盐,C水解使溶液显碱性,离子方程式为C+H2OHC+OH-。(4)0.02 mol Ba(OH)2与0.01 mol Fe2(SO4)3混合生成0.02 mol BaSO4沉淀和 Fe(OH)3,其质量为0.02 mol×233 g· mol-1+×107 g· mol-1≈6.1 g。(5)将Cu投入到装有D溶液的试管中,Cu不溶解,再滴加稀硫酸,Cu逐渐溶解,管口附近有红棕色气体出现,红棕色气体是NO2,这说明D中含有N。在酸性条件下N能氧化金属铜,反应的离子方程式为3Cu+8H++2N3Cu2++2NO↑+4H2O。(6)D中含有N,E中含有Cl-,而剩余的阳离子只有Al3+和Mg2+,则检验出D、E中的阳离子的实验操作是:向D的溶液中逐滴加入Ba(OH)2溶液直至过量,若先出现白色沉淀后又逐渐溶解,则说明D中含有Al3+,E中含有Mg2+(或向D的溶液中加入适量Na2CO3溶液,若产生了白色沉淀和无色无味的气体,则说明D中含有Al3+,E中含有Mg2+)。