- 403.00 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
龙海二中2019-2020学年上学期第二次月考
高三化学试卷
(考试时间:90分钟 总分:100分)
可能用到的相对原子质量:Fe-56 O-16 Na-23 Cu-64 H-1 S-32
第Ⅰ卷 (选择题 共48分)
一、 选择题:(16个小题,每小题3分,共48分,每小题给出的四个选项中,只有一项符合题目要求)。
1、化学与生产、生活密切相关。下列说法正确的是
A.砒霜的主要成分是三硫化二砷
B.氢氧化铝和碳酸钠均可用于治疗胃酸过多
C.过量服用阿司匹林引起酸中毒后,可用静脉注射NaHCO3溶液的方法解毒
D.铜单质制成的“纳米铜”在空气中能燃烧,说明“纳米铜”的金属性比铜片强
2、NA是阿伏加德罗常数的值,下列说法正确的是
A.36g由35Cl和37C1组成的氯气中所含质子数一定为17NA
B.7.8 g Na2O2与足量酸性KMnO4溶液反应,转移的电子数为0.2NA
C.密闭容器中1mol PCl3与1mol Cl2反应制备PCl5(g),增加了2NA个P-Cl键
D.5.6g铁片投入足量浓硝酸中,转移的电子数为0.3NA
3、列解释事实的离子方程式正确的是
A.铜丝溶于浓硝酸生成绿色溶液:3Cu+8H++2NO==3Cu2++2NO↑+4H2O
B.稀硫酸与Ba(OH)2溶液混合出现浑浊:H++OH−+Ba2++SO=BaSO4↓+H2O
C.澄清石灰水中加入过量小苏打溶液出现浑浊:Ca2++2HCO+2OH−=CaCO3↓+CO+2H2O
D.在A1C13溶液中加入过量氨水出现浑浊:A13++3OH−=Al(OH)3↓
4、无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100mL甲气体经过如图所示实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为
A.NH3、NO2、N2 B.NH3、NO、CO2
C.NH3、NO2、CO2 D.NO、CO2、N2
5、现用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理。下列说法正确的是
A.制取氨气时烧瓶中的固体常用CaO或CaCl2
B.将湿润的蓝色石蕊试纸置于三颈瓶口,试纸变红,说明NH3已经集满
C.关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧颈口c,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,则E点时喷泉最剧烈
D.工业上,若出现液氨泄漏,喷稀盐酸比喷洒NaHCO3溶液处理效果好
6、在容积为2.0 L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是
A.从反应开始到第一次达到平衡时,A物质的平均反应速率为0.0667 mol/(L·min)
B.该反应的化学方程式为2D(s)2A(g)+B(g),该反应的平衡常数表达式为K=c(A)2·c(B)
C.已知:反应的∆H>0,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度
D.若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是a曲线
7、下列图示与对应的叙述相符的是
A.图1表示H2与O2发生反应过程中的能量变化,则H的燃烧热为241.8kJ·mo1-1
B.图2表示压强对可逆反应2A(g)+2B(g)3C(g)+D(s)的影响,乙的压强比甲的压强大
C.若图3表示等质量的钾、钠分别与足量水反应,则甲代表钠
D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
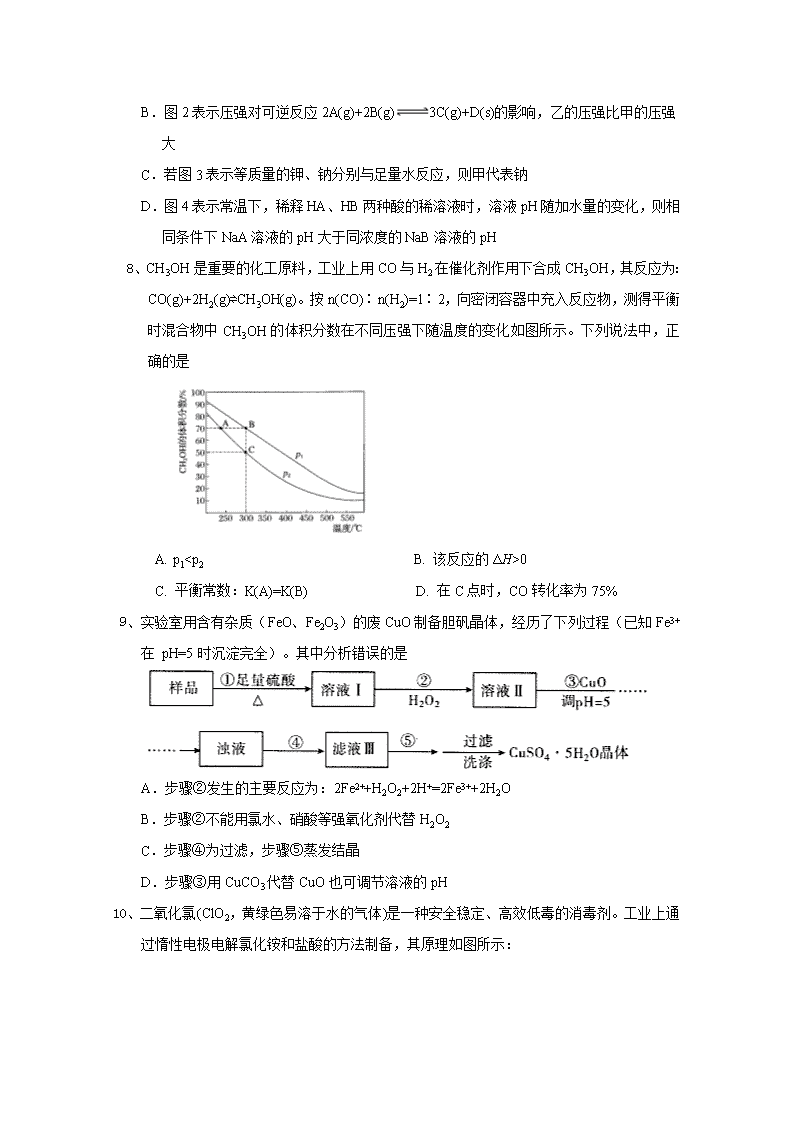
8、CH3OH是重要的化工原料,工业上用CO与H2在催化剂作用下合成CH3OH,其反应为:CO(g)+2H2(g)⇌CH3OH(g)。按n(CO)∶n(H2)=1∶2,向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法中,正确的是
A. p10
C. 平衡常数:K(A)=K(B) D. 在C点时,CO转化率为75%
9、实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历了下列过程(已知Fe3+在 pH=5时沉淀完全)。其中分析错误的是
A.步骤②发生的主要反应为:2Fe2++H2O2+2H+=2Fe3++2H2O
B.步骤②不能用氯水、硝酸等强氧化剂代替H2O2
C.步骤④为过滤,步骤⑤蒸发结晶
D.步骤③用CuCO3代替CuO也可调节溶液的pH
10、二氧化氯(ClO2,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备,其原理如图所示:
下列说法不正确的是
A.b电极接电源的负极,在b极区流出的Y溶液是稀盐酸
B.二氧化氯发生器中排出的X溶液中溶质主要为NaCl和NaOH
C.电解过程中二氧化氯发生器中产生2.24L(标准状况)NH3,则b极产生0.6g H2
D.电解池a极的电极反应式为NH-6e−+4OH−+3Cl−=NCl3+4H2O
11、在500mL KNO3和Cu(NO3)2的混合溶液中,c(NO)=6mol/L,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是
A.电解得到的Cu的物质的量为0.5mol
B.向电解后的溶液中加入98g的Cu(OH)2可恢复为原溶液
C.原混合溶液中c(K+)=4mol/L
D.电解后溶液中c(H+)=2mol/L
12、下图是一种正投入生产的大型蓄电系统。放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述正确的是
A.放电时,负极反应为3NaBr-2e−=NaBr3+2Na+
B.充电时,阳极反应为2Na2S2-2e−=Na2S4+2Na+
C.放电时,Na+经过离子交换膜,由b池移向a池
D.用该电池电解饱和食盐水,产生2.24L H2时,b池生成17.40 gNa2S4
13、常温下,向1L 0.1mol/L NH4Cl溶液中,不断加入固体NaOH后,与NH3·H2O的变化趋势如图所示(不考虑体积变化和氨的挥发)。下列说法不正确的是
A.M点溶液中水的电离程度比原溶液小
B.在M点时,n(OH-)-n(H+)=(a-0.05)mol
C.随着NaOH的加入,不断增大
D.当n(Na0H)=0.1mol时,c(Na+)=c()+c(NH3·H2O)
14、在25℃时,将1.0L c mol·L-1 CH3COOH溶液与0.1mol NaOH固体混合,使之充分反应。然后向该混合溶液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或加入)物质的物质的量的变化如图所示。下列叙述错误的是
A.水的电离程度:a>b>c
B.c点对应的混合溶液中:c(CH3COOH)>c(Na+)>c(OH-)
C.a点对应的混合溶液中:c(Na+)=c(CH3COO-)
D.该温度下,的电离平衡常数
15、25℃时,将浓度均为0.1mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是
A.Ka(HA)=1×10-6
B.b点c(B+)=c(A-)=c(OH-)=c(H+)
C.a→c过程中水的电离程度始终增大
D.c点时,随温度升高而减小
16、电解质溶液的电导率越大,导电能力越强。用0.100mol·L-1的NaOH溶液滴定10.00mL浓度均为0.100mol·L-1 的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
A.曲线②代表滴定CH3COOH溶液的曲线
B.A点溶液中:c(CH3COO-)+c(OH-)-c(H+)0.1mol·L-1
C.在相同温度下,A、B、C三点溶液中水的电离程度:A”“<’或“=”)0。
②985℃时,反应经过5s达到平衡状态,此时H2S的转化率为40%,则用H2表示的反应速率为v(H2)=____________。
③随着H2S分解温度的升高,曲线b向曲线a逐渐靠近,其原因是____________。
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如下图所示。
在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中尽可能不含CuS,可采取的措施有________。
18、 (12分) 对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一。
(1) 电镀厂的废水中含有的CN−有剧毒,需要处理加以排放。处理含CN−废水的方法之一是在微生物的作用下,CN−被氧气氧化成HCO,同时生成NH3,该反应的离子方程式为_____________。
(2)电渗析法处理厨房垃极发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A−表示乳酸根离子):
①阳极的电极反应式为________________________。
②简述浓缩室中得到浓乳酸的原理:________________________。
③电解过程中,采取一定的措施可控制阳极室的pH约为6~8,此时进入浓缩室的OH−可忽略不计。400mL 10g/L乳酸溶液通电一段时间后,浓度上升为145g/L(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为________L(提示:乳酸的摩尔质量为90 g/mol)。
19、(12分)火法炼铜是目前世界上最主要的冶炼铜的方法,其产量可占到铜总产量的85%以上,火法炼铜相关的方程式有
Cu2S(s)+O2(g)=2Cu(s)+SO2(g) ΔH1=-271.4kJ/mol 反应①
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g) ΔH2=+123.2kJ/mol 反应②
(1)Cu2S(s)在空气中煅烧生成Cu2O(s)和SO2(g)的热化学方程式是___。
(2)在2L的恒温密闭容器中通入5mol氧气并加入足量Cu2S发生反应①(不考虑其它反应),容器中的起始压强为akPa,反应过程中某气体的体积分数随时间变化如图所示,反应前3min平均反应速率v(SO2)=___mol/(L·min),该温度下反应的平衡常数KP=___(KP为以分压表示的平衡常数)。若保持温度不变向平衡体系中再通入1mol氧气,达到新平衡后氧气的体积分数__ _(填“大于”“小于”或“等于”)原平衡时氧气的体积分数。
20、(16分) N2O、NO和NO2等氮氧化物是空气污染物含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为_ __。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收。
①下列措施不能提高尾气中NO和NO2去除率的有____ (填字母代号)
A.采用气、液逆流的方式吸收尾气
B.加快通入尾气的速率
C.吸收尾气过程中定补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是____(填化学式),吸收后排放的尾气中含量较高的氮氧化物是____(填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HC1O氧化NO生成Cl和NO3-,其离子方程式为_______。
②NaClO溶液的初始pH越小,NO转化率越高,其原因是_______。
龙海二中2019-2020学年上学期第二次月考
高三化学答题卷
(考试时间:90分钟 总分:100分)
一、选择题(每题3分,共48分)
题号
1
2
3
4
5
6
7
8
答案
题号
9
10
11
12
13
14
15
16
答案
第Ⅱ卷(非选择题 共52分)
17、(12分)
17. (1)① 。 ② 。
③
(2)
18、18、(12分)
(1)
(2)①
②
③ L
19、(12分)
(1)_____ ( (2) v(SO2)=__ _mol/(L·min); KP=__ _
(填“大于”“小于”或“等于”)
20. (共16分,其中(2)②两空每空2分,其余每空3分)
(1) 。
(2)① 。②_ _____________; 。
(3)①__________________________________________________________。
②______________ _____________________________________。
龙海二中2019-2020学年上学期第二次月考
高三化学参考答案
一、选择题(每小题3分,共48分)
题号
1
2
3
4
5
6
7
8
答案
C
B
C
B
D
D
C
D
题号
9
10
11
12
13
14
15
16
答案
C
D
B
C
C
D
D
D
第Ⅱ卷(非选择题 共52分)
17.(12分)
(1)① > ② 0.04mol/(L·S)
③ 温度升高,反应速率加快,达到平衡所需时间缩短
(2)增加氧气的通入量或增加起始时c(Fe3+)
18、(12分)
(1)4H2O+2CN−+O2=2HCO+2NH3↑
(2)① 2H2O-4e−=4H++O2↑
② 阳极H2O放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室,A−从阴极通过阴离子交换膜进入浓缩室,H++A−=HA,乳酸浓度增大
③ 6.72
19、(12分)
(1)2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) ΔH=-937.4kJ/mol
(2)0.4 ; 1.5 ; 等于
20、(共16分,其中(2)②两空每空2分,其余每空3分)
(1)2NH3+2O2N2O+3H2O
(2)① B 。 ② NaNO3 ; NO
(3)① 3HClO + 2NO + H2O = 3C1− + 2NO + 5H+
② 溶液pH越小溶液中HClO的浓度越大氧化NO的能力越强