- 546.50 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2019学年高一化学上学期12月月考试题
(时间:60分钟 满分:100分)
可能用到的相对原子质量H 1 O 16 Na 23 Cu 64 N14 Cl 35.5 C 12
一、单选题(本题共16小题,每小题3分,共48分)
1.将一小粒钠投入氯化铜溶液中,待反应停止后,观察到的现象是( )
A. 有蓝色沉淀 B. 有蓝色沉淀和气体产生
C. 有气体产生,无沉淀生成 D. 无沉淀和有气体产生
2.下列各组中的两种物质作用时,反应条件(温度、反应物用量)改变,不会引起产物种类变化的是( )
A. Na和O2 B. Ca(OH)2和CO2 C. Fe和HCl D. C和O2
3.下列物质充分反应后,滴加KSCN溶液显红色的是( )
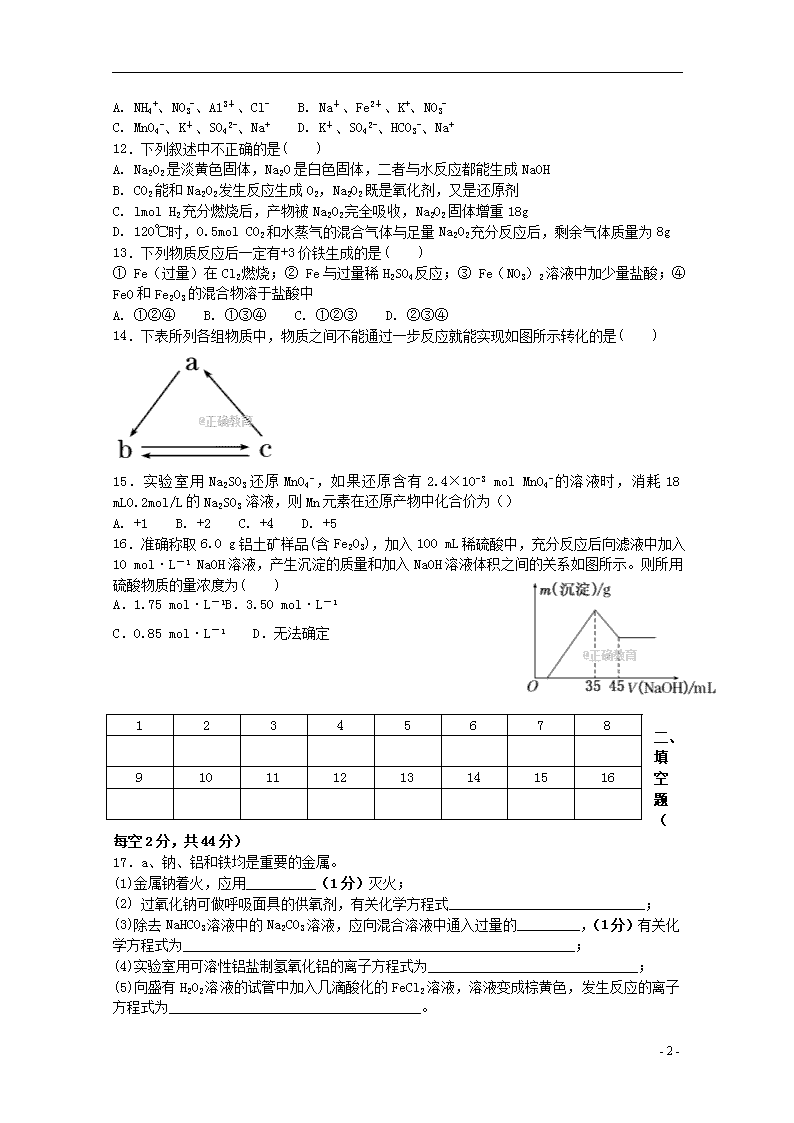
A. FeO +盐酸 B. 铁+稀硫酸 C. FeCl2(溶液)+Cl2 D. Fe+CuSO4(溶液)
4.把一块生锈的铁片投入盛有稀硫酸的烧杯里,待铁片完全溶解后,往烧杯里滴加氢氧化钠溶液至过量,然后过滤,并充分灼烧不溶物,则最终留下的固体是( )
A. Na2O B. Fe2O3和Fe C. Fe2O3 D. Fe2O3和NaOH
5.有关Na2CO3和NaHCO3的性质,下列叙述错误的是( )
A. 相同温度下,等浓度的Na2CO3和NaHCO3溶液的碱性比较,前者更强
B. 常温时水溶性:Na2CO3>NaHCO3
C. 在酒精灯加热的条件下,前者不分解,后者分解
D. 将澄清的石灰水分别加入Na2CO3和NaHCO3溶液中,前者产生沉淀,后者无现象6.设NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A. 标准状况下,22.4 L由NH3和CH4组成的混合气体,所含分子数为NA
B. 常温常压下,28 g CO中所含碳原子数为NA
C. 1 L 0.5 mol·L-1 MgCl2溶液中,含有Cl-的个数为NA
D. NA个氯气分子的体积为22.4 L
7.下列离子方程式书写正确的是( )
A.钠投入到CuSO4溶液中:2Na+Cu2+===2Na++Cu
B.AlCl3溶液中加入足量氨水:Al3++3OH-===Al(OH)3↓
C.三氯化铁溶液中加入铁粉:Fe3++Fe===2Fe2+
D.FeCl2溶液与Cl2反应:2Fe2++Cl2===2Fe3++2Cl-
8.下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①金属钠投入FeCl3溶液中;②过量NaOH溶液和明矾溶液混合;
③少量Ca(OH)2投入过量NaHCO3溶液中;④向AlCl3溶液中滴加过量氨水;
⑤向饱和Na2CO3溶液中通入足量CO2
A. ①③④⑤ B. 只有①④ C. 只有②③ D. 只有③④⑤
9.已知有关物质的还原性强弱顺序是SO2>I->Fe2+>Br->Cl-,则以下反应能够发生的有( )
① I2+SO2+2H2O=H2SO4+2HI ② FeCl2+ C12=2FeCl3
③ FeC13+2HI=2FeCl2+2HCl+I2④ FeCl3+2HBr=2FeCl2+2HCl+ Br2
A. ①②③ B. ①③ C. ②④ D. ①②③④
10.在5NH4NO3═ 2HNO3+4N2↑+9H2O中,发生氧化反应的氮原子和发生还原反应的氮原子的质量比是( )
A. 1:1 B. 3:5 C. 5:3 D. 2:8
11.在某无色透明的酸性溶液中,能共存的离子组是( )
- 5 -
A. NH4+、NO3-、A13+、Cl- B. Na+、Fe2+、K+、NO3-
C. MnO4-、K+、SO42-、Na+ D. K+、SO42-、HCO3-、Na+
12.下列叙述中不正确的是( )
A. Na2O2是淡黄色固体,Na2O是白色固体,二者与水反应都能生成NaOH
B. CO2能和Na2O2发生反应生成O2,Na2O2既是氧化剂,又是还原剂
C. lmol H2充分燃烧后,产物被Na2O2完全吸收,Na2O2固体增重18g
D. 120℃时,0.5mol CO2和水蒸气的混合气体与足量Na2O2充分反应后,剩余气体质量为8g
13.下列物质反应后一定有+3价铁生成的是( )
① Fe(过量)在Cl2燃烧;② Fe与过量稀H2SO4反应;③ Fe(NO3)2溶液中加少量盐酸;④ FeO和Fe2O3的混合物溶于盐酸中
A. ①②④ B. ①③④ C. ①②③ D. ②③④
物质
选项
a
b
c
A
Al2O3
AlCl3
Al(OH)3
B
CuO
Cu(OH)2
CuCl2
C
Fe
FeCl3
FeCl2
D
CO2
NaHCO3
Na2CO3
14.下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
15.实验室用Na2SO3还原MnO4-,如果还原含有2.4×10-3 mol MnO4-的溶液时,消耗18 mL0.2mol/L的Na2SO3 溶液,则Mn元素在还原产物中化合价为()
A. +1 B. +2 C. +4 D. +5
16.准确称取6.0 g铝土矿样品(含Fe2O3),加入100 mL稀硫酸中,充分反应后向滤液中加入10 mol·L-1 NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为( )
A.1.75 mol·L-1B.3.50 mol·L-1
C.0.85 mol·L-1 D.无法确定
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
二、填空题(每空2分,共44分)
17.a、钠、铝和铁均是重要的金属。
(1)金属钠着火,应用__________(1分)灭火;
(2) 过氧化钠可做呼吸面具的供氧剂,有关化学方程式____________________________;
(3)除去NaHCO3溶液中的Na2CO3溶液,应向混合溶液中通入过量的_________,(1分)有关化学方程式为________________________________________________________;
(4)实验室用可溶性铝盐制氢氧化铝的离子方程式为______________________________;
(5)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为____________________________________。
- 5 -
(6)检验溶液中含Fe2+的操作方法______________________________________________。
(7)向装FeCl2溶液的试管中滴加NaOH溶液的现象为_____________________________
___________,有关氧化还原反应方程式为_____________________________________。
b、我国古代炼丹中经常使用到丹红,俗称铅丹。其化学式Pb3O4可写成2PbO.PbO2,结合氧化物的分类可知PbO是碱性氧化物,而PbO2不是碱性氧化物。
(1)写出PbO(难溶于水)与盐酸反应的离子方程式______________________________;
(2)已知PbO2与浓盐酸混合后可得到PbCl2、黄绿色气体等物质,请写出相应的化学方程式_______________________________________;当生成2.24L(标准状况下)黄绿色气体时,转移的电子数目为_____NA。
18.现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出金属元素A的原子结构示意图:_______________。
(2)写出下列反应的离子方程式:反应③
反应⑤
(3) 检验物质G中阳离子的操作方法_________________________________________。
(4)保存物质F的溶液时,要加入,目的是。
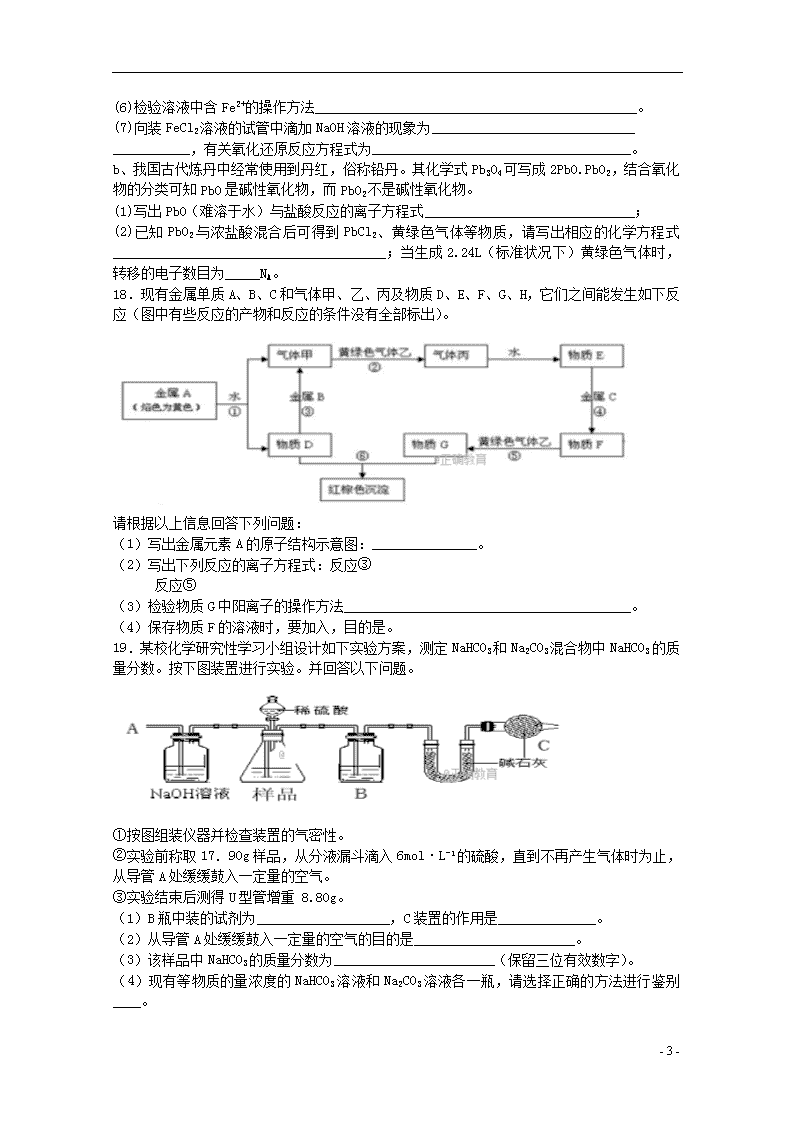
19.某校化学研究性学习小组设计如下实验方案,测定NaHCO3和Na2CO3混合物中NaHCO3的质量分数。按下图装置进行实验。并回答以下问题。
①按图组装仪器并检查装置的气密性。
②实验前称取17.90g样品,从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止,从导管A处缓缓鼓入一定量的空气。
③实验结束后测得U型管增重 8.80g。
(1)B瓶中装的试剂为___________________,C装置的作用是______________。
(2)从导管A处缓缓鼓入一定量的空气的目的是_______________________。
(3)该样品中NaHCO3的质量分数为_______________________(保留三位有效数字)。
(4)现有等物质的量浓度的NaHCO3溶液和Na2CO3溶液各一瓶,请选择正确的方法进行鉴别____。
- 5 -
A.加热法:产生使澄清石灰水变浑浊气体的是NaHCO3
B.沉淀法:加入BaCl2溶液,产生沉淀的是Na2CO3溶液
C.气体法:逐滴加入盐酸,立即产生气泡的是NaHCO3溶液
D.测pH法:用pH试纸测其pH,pH大的是Na2CO3溶液
三、计算题(共8分)
20.把19.2 g Cu放入足量的稀硝酸中,微热至Cu完全反应。(已知方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O )
求:(1)生成的NO在标准状况下的体积。
(2)被还原的硝酸的质量。
- 5 -
- 5 -