- 2.39 MB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第四章 非金属及其化合物
第三节 硫和氮的氧化物
第
2
课时
新课标人教版高中化学课件系列
化学 必修
1
俗语:
雷雨肥庄稼?大家知道什么意思吗
?
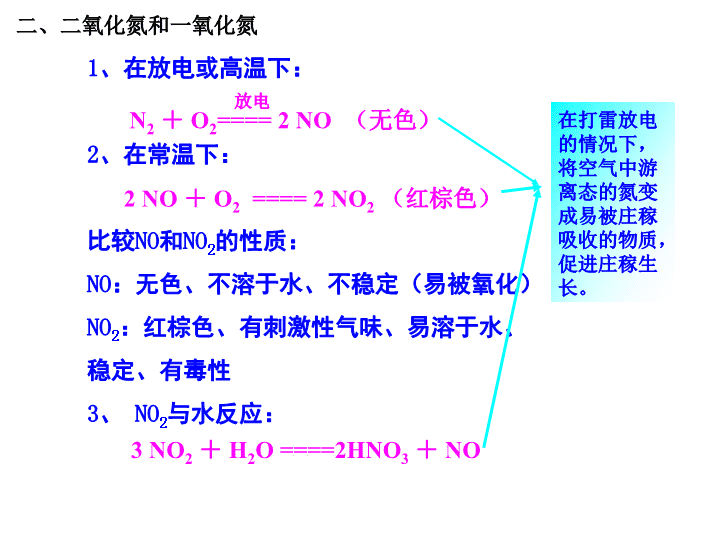
二、二氧化氮和一氧化氮
1
、在放电或高温下:
2
、在常温下:
比较
NO
和
NO
2
的性质:
NO
:无色、不溶于水、不稳定(易被氧化)
NO
2
:红棕色、有刺激性气味、易溶于水、
稳定、有毒性
3
、
NO
2
与水反应:
放电
N
2
+
O
2
==== 2 NO
(无色)
2 NO
+
O
2
==== 2 NO
2
(红棕色)
3 NO
2
+
H
2
O ====2HNO
3
+
NO
在打雷放电的情况下,将空气中游离态的氮变成易被庄稼吸收的物质,促进庄稼生长。
二、二氧化氮和一氧化氮
3NO
2
+H
2
O====2HNO
3
+NO
+4
+5
+2
NO
2
中有
2/3
的氮元素化合价升高,被氧化;有
1/3
的氮元
素化合价降低,被还原。
NO
2
既是氧化剂又是还原剂。
二、二氧化氮和一氧化氮
明星分子
NO
1998
年诺贝尔奖获得者伊格纳罗发现少量的
NO
在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆等功能,成为当前生命科学的研究热点,
NO
亦称为
“
明星分子
”
。
实验步骤
现 象
解释(反应式)
1
2
3
1
、请你设计实验,要求尽可能多的
NO
2
被水吸收。
将充满
NO
2
的试
管倒立在水槽中
红棕色逐渐消失,试管水位上升到
试管容积
2/3
处
4 NO
2
+ 2H
2
O + O
2
= 4HNO
3
继续通入氧气
水逐渐充满试管
3NO
2
+H
2
O=2HNO
3
+NO
2NO+O
2
=2NO
2
往试管通入
O
2
无色气体变成红棕色;水位继续上升,红棕色又消失
3NO
2
+H
2
O=2HNO
3
+NO
科学探究
二、二氧化氮和一氧化氮
在这个过程中要通入多少的
O
2
,
NO
2
才能完全转变成
HNO
3
呢?
2NO+O
2
=2NO
2
3NO
2
+
H
2
O
=
2HNO
3
+
NO
4NO
2
+
O
2
+
2H
2
O
=
4HNO
3
NO
2
与
O
2
以
4
:
1
的体积比(摩尔比)混合,与足量的水反应就可以完全转变成硝酸。
二、二氧化氮和一氧化氮
假如是
NO
和
O
2
混合呢?当体积比是多少的时候跟足量的水反应才能完全转变成硝酸呢?
2NO+O
2
=2NO
2
3NO
2
+
H
2
O
=
2HNO
3
+
NO
4NO
+
3O
2
+
2H
2
O
=
4HNO
3
二、二氧化氮和一氧化氮
2
、你的设计对工业上生产硝酸有什么启示?
工业生产硝酸,将尾气(
NO
)吸收通入适量的氧气后再溶解于水,经过多次循环氧化、溶解,可充分利用原料,并减少
NO
的排放,有利于保护环境。
二、二氧化氮和一氧化氮
【
科学视野
】
:火箭为什么能飞上天?
二、二氧化氮和一氧化氮
二、二氧化氮和一氧化氮
1
、二氧化硫和二氧化氮是主要的大气污染物。
2
、污染物的来源:
(
1
)
SO
2
主要
来自于化石燃料(如煤与石油)的燃烧、含硫金属的冶炼以及制造硫酸、磷肥等产生的废气。
(
2
)
NO
2
主要来自于汽车尾气。
二、二氧化硫和二氧化氮对大气的污染
二、二氧化硫和二氧化氮对大气的污染
著名的杭州灵隐寺的
“
摩崖石刻
”
近年经酸雨侵蚀,佛像眼睛、鼻子、耳朵等剥蚀严重,面目皆非,修补后,古迹不
“
古
”
。
受酸雨伤害的水稻
未受酸雨伤害的水稻
酸雨:
主要指
pH
小于
5.6
的雨水
,
其主要含有硫酸和硝酸。
正常雨水
(
含雨、霜、露、雹、雾等
)
由于存在
CO
2
原因其
pH
值约为
5.6
。在水中当
pH
值小于
5.5
时
,
大部分鱼类难以生存
;
当降到小于
5
时
,
各种鱼类和两栖动物及昆虫、水草及浮游生物面临灭绝。
酸雨的形成
石油
煤 金属矿物
酸雨
燃 烧
CO
2
SO
2
NO
x
雨水、霜、雹、露等
酸雨的危害主要有:
1
、对人体的直接危害,首先是它的刺激性,其次是它会
形成硫酸雾和硫酸盐雾
,
其毒性
比
SO
2
大
,
能浸入人的肺部
,
引起肺水肿等疾病而使人死亡
;
2
、引起河流、湖泊的水体酸化,严重影响水生动物生长;
3
、破坏土壤、植被、森林;
4
、腐蚀金属、油漆、皮革、纺织品及建筑材料等;
5
、渗入地下,可引起地下水酸化,酸化后的地下水中铝、铜、锌、镉等对人体有害金属元素的含量会偏高。
酸雨的危害实例录
:
1
、
50
年前
,
故宫太和殿台阶的栏杆上雕刻着各式各样精美浮雕花纹还清晰可见
,
而现在却已大多模糊不清
,
部分已成光板
……
2
、巫山在一场大雨过后
,
整个山体上暴露的石块全部被腐蚀近
1
厘米
……
3
、
2003
年
,
几场酸雨过后
,
我国四川奉节县
12
万亩华山松全部枯死
,
重庆面山的
3
万亩马尾松死亡过半。
资料卡片:防止酸雨的措施
1
、改善燃料种类,积极开发新能源。
2
、对煤(其中含硫为
0.3%-5%
)进行处理
,
如选洗加工、综合开发、在煤中加入适量的生石灰、对排放的烟进行处理以回收
SO
2
。
3
、种植能够吸收
SO
2
的有关树木
(
如臭椿、垂柳、柳杉)等。
1972
年
6
月
5
日,具有历史意义的人类环境会议在瑞典首都斯德哥尔摩召开,通过了著名的
《
人类环境宣言
》
,并确定每年
6
月
5
日为“世界环境日”。从
1974
年起,每年联合国环境规划署确定一个主题,开展“世界环境日”活动,其中
1983
的主题是“防治酸雨”。
1
、马斯河谷烟雾事件(
1930
年
12
月),原因是
SOx
和
MnO
微粒作用生成
SO
2
--SO
3
进入人体。
2
、多诺拉烟雾事件(
1948
年
10
月),原因是
SO
2
和烟尘作用生成硫酸盐,吸入人体肺部。
3
、伦敦烟雾事件(
1952
年
12
月),原因是粉尘中
Fe
2
O
3
使
SO
2
反应生成硫酸铁附在粉尘上,吸入人体肺部。
4
、洛衫机光化学烟雾事件(
1943
年
5--9
月),原因是石油工业和汽车废气在紫外线作用下生成光化学烟雾。
1.“
酸雨”的形成主要是由于( )
A.
森林遭乱砍滥伐,破坏生态平衡
B.
工业上大量燃烧含硫燃料
C.
大气中
CO
2
的含量增多
D.
汽车排出大量尾气
B
2.
下列污染现象主要与
SO
2
有关的是( )
A
.臭氧层空洞
B
.酸雨
C
.光化学烟雾
D
.温室效应
B
课堂训练
3.
现有以下几种措施:① 对燃烧煤时产生的尾气进行除硫处理,② 少用原煤做燃料,③ 煤燃烧时鼓入足量空气,④ 开发清洁能源。其中能减少酸雨产生的措施是( )
A
.①②③
B
.②③④
C
.①②④
D
.①③④
4.
下列污染现象主要与
NO
2
有关的是
( )
A
.臭氧层空洞
B
.水体富营养化
C
.光化学烟雾
D
.温室效应
C
C
5.
飘尘是物质燃烧时产生的粒状漂浮物,颗粒很小,不易沉降。它与空气中的
SO
2
和
O
2
接触时,
SO
2
会部分转化为
SO
3
,使空气的酸度增加,环境污染更为严重。其中飘尘所起的作用可能是 ( )
A
.氧化剂
B
.还原剂
C
.催化剂
D
.载体
C
6.
在新疆与青海交界处有一山谷,人称魔鬼谷。每当人畜进入后,经常电闪雷鸣,狂风暴雨,把人畜击毙。然而谷内却是牧草茂盛,四季常青。请解释原因。
N
2
+ O
2
=
=
==
2NO
放电或高温
2NO
+ O
2
= 2NO
2
3NO
2
+ H
2
O = 2HNO
3
+ NO
雷雨发庄稼
7.
氯气和二氧化硫皆可做漂白剂,若用两者(
1:1
) 一起漂白一种 物质时,漂白效果会( )
A.
增强
B.
不变
C.
减弱
D.
难确定
SO
2
+ Cl
2
+ 2 H
2
O = H
2
SO
4
+ 2HCl
C
Thanks
谢谢您的观看!