- 68.29 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第1课时 浓度、压强对化学反应速率的影响
课后篇巩固提升
基础巩固
1.下列影响化学反应速率的主要因素是( )
A.压强 B.浓度
C.接触面积 D.反应物的性质
解析 影响化学反应速率大小的主要因素是反应物的性质。
答案 D
2.下列说法正确的是( )
①活化分子间的碰撞一定能发生化学反应
②普通分子有时也能发生有效碰撞
③升高温度会增大反应速率,原因是增加了单位时间内活化分子的有效碰撞次数
④增大反应物浓度会增大反应速率的原因是单位体积内有效碰撞的次数增多
⑤化学反应的发生是活化分子有合适取向时的有效碰撞
A.①②⑤ B.③④⑤ C.①②③ D.②③④
解析 ①活化分子间的碰撞不一定为有效碰撞,活化分子间的碰撞不一定能发生化学反应,还与其分子取向有关,故错误;②普通分子不具有反应所需的能量,则普通分子不能发生有效碰撞,故错误;③升高温度,提供了分子需要的能量,活化分子百分数增大,则增加了单位时间内活化分子的有效碰撞次数,反应速率增大,故正确;④增大反应物浓度,活化分子数目增多,单位体积内有效碰撞的次数增多,反应速率增大,故正确;⑤活化分子有合适取向时发生有效碰撞,即发生了化学反应,故正确。
答案 B
3.用3 g块状大理石与30 mL 3 mol·L-1盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
①再加入30 mL 3 mol·L-1盐酸 ②改用30 mL 6 mol·L-1盐酸 ③改用3 g粉末状大理石
A.①② B.②③
C.①③ D.①②③
解析 对反应CaCO3(s)+2HCl(aq)CaCl2(aq)+CO2(g)+H2O(l)而言,将块状大理石改为粉末状大理石、增大盐酸浓度等均可增大反应速率。
答案 B
4.将盐酸滴到碳酸钠粉末上,能使反应的最初速率加快的是( )
A.盐酸浓度不变,使用量增大一倍
B.盐酸浓度增加一倍,用量减至一半
C.增大Na2CO3粉末的量
D.把盐酸换为浓硫酸
解析 Na2CO3粉末为固体,改变固体的量不影响反应速率,需要改变盐酸的浓度或改变温度。浓硫酸中c(H+)非常小,和Na2CO3粉末反应非常慢。
答案 B
5.在通常条件下的密闭容器中存在下列四个平衡体系,增大容器的容积对化学反应速率没有影响的是( )
A.2SO2(g)+O2(g)2SO3(g)
B.CO(g)+H2O(g)CO2(g)+H2(g)
C.CO2(g)+H2O(l)H2CO3(aq)
D.Fe3+(aq)+3SCN-(aq)Fe(SCN)3(aq)
解析 D选项反应物与生成物中无气体,改变压强对反应速率无影响。
答案 D
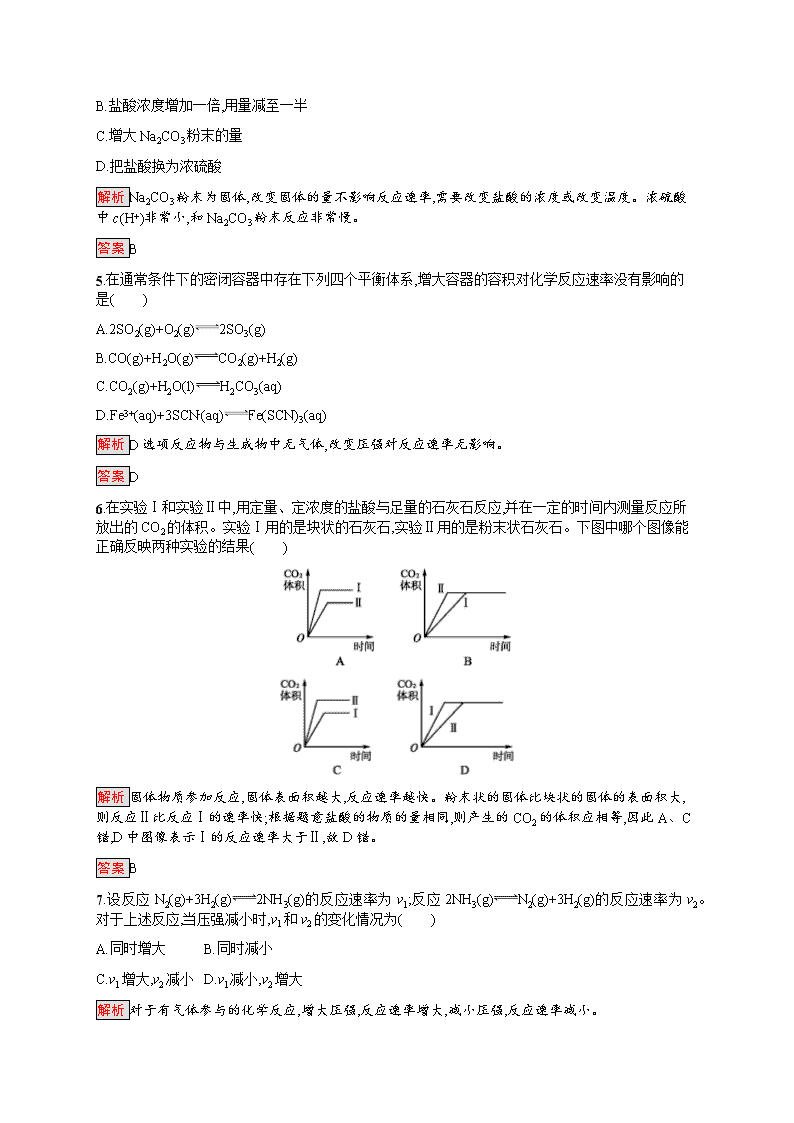
6.在实验Ⅰ和实验Ⅱ中,用定量、定浓度的盐酸与足量的石灰石反应,并在一定的时间内测量反应所放出的CO2的体积。实验Ⅰ用的是块状的石灰石,实验Ⅱ用的是粉末状石灰石。下图中哪个图像能正确反映两种实验的结果( )
解析 固体物质参加反应,固体表面积越大,反应速率越快。粉末状的固体比块状的固体的表面积大,则反应Ⅱ比反应Ⅰ的速率快;根据题意盐酸的物质的量相同,则产生的CO2的体积应相等,因此A、C错,D中图像表示Ⅰ的反应速率大于Ⅱ,故D错。
答案 B
7.设反应N2(g)+3H2(g)2NH3(g)的反应速率为v1;反应2NH3(g)N2(g)+3H2(g)的反应速率为v2。对于上述反应,当压强减小时,v1和v2的变化情况为( )
A.同时增大 B.同时减小
C.v1增大,v2减小 D.v1减小,v2增大
解析 对于有气体参与的化学反应,增大压强,反应速率增大,减小压强,反应速率减小。
答案 B
8.反应C(s)+H2O(g)CO(g)+H2(g)在一密闭容器中进行,下列条件的改变能使反应速率减小的是( )
A.减少碳的量
B.将容器的体积缩小一半
C.保持体积不变,增加水蒸气的量
D.保持压强不变,充入Ne
解析 碳为固态反应物,减少碳的量,对反应速率几乎没有影响,A项错误;将容器容积缩小一半,压强增大,反应物浓度增大,反应速率增大,B项错误;保持体积不变,增加水蒸气的量,增大了水蒸气的浓度,反应速率增大,C项错误;保持压强不变,充入Ne,使容器体积增大,反应物浓度减小,反应速率减小,D项正确。
答案 D
9.反应3Fe(s)+4H2O(g)Fe3O4(s)+4H2(g),在一可变容积的密闭容器中进行,试回答:
(1)增加Fe的量,其正反应速率 (填“增大”“不变”或“减小”,下同)。
(2)将容器的体积缩小一半,其正反应速率 ,逆反应速率 。
(3)保持体积不变,充入N2使体系压强增大,其正反应速率 ,逆反应速率 。
(4)保持压强不变,充入N2使容器的体积增大,其正反应速率 ,逆反应速率 。
解析 (1)铁为固体,其浓度为常数,增加Fe的量,其正反应速率不变;(2)将容器的体积缩小一半,水蒸气、氢气的浓度均加倍,其正反应速率增大,逆反应速率增大;(3)保持体积不变,充入N2使体系压强增大,与反应相关的各物质的物质的量不变,浓度不变,其正反应速率不变,逆反应速率不变;(4)保持压强不变,充入N2使容器的体积增大,水蒸气、氢气的浓度减小,其正反应速率减小,逆反应速率减小。
答案 (1)不变 (2)增大 增大
(3)不变 不变 (4)减小 减小
能力提升
10.100 mL 6 mol·L-1的硫酸与过量锌粉反应,在一定温度下,为了减小反应速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
A.硫酸钠固体 B.碳酸钠固体
C.水 D.硝酸钾溶液
解析 硫酸钠不与硫酸或锌反应,不改变溶液的体积,对反应速率无影响;碳酸钠能与硫酸反应,使生成氢气的量减小;加入水使硫酸的浓度变小,可以减小化学反应速率;加入硝酸钾时相当于Zn与硝酸反应,不生成氢气。
答案 C
11.某探究小组利用反应CH3COCH3+Br2CH3COCH2Br+HBr来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
实验
序号
初始浓度c/(mol·L-1)
溴颜色消失
所需时间t/s
CH3COCH3
HCl
Br2
①
0.80
0.20
0.001 0
290
②
1.60
0.20
0.001 0
145
③
0.80
0.40
0.001 0
145
④
0.80
0.20
0.002 0
580
分析实验数据所得出的结论不正确的是( )
A.增大c(CH3COCH3),v(Br2)增大
B.实验②和③的v(Br2)相等
C.增大c(HCl),v(Br2)增大
D.增大c(Br2),v(Br2)增大
解析 从表中数据看,①④中CH3COCH3、HCl的浓度是相同的,而④中Br2的浓度是①中的2倍,但溴颜色消失所需时间,④是①的2倍,D项错误。
答案 D
12.加0.1 mol MnO2粉末于50 mL过氧化氢溶液中,在标准状况下放出气体的体积和时间的关系如图所示。
(1)实验时放出气体的总体积是 。
(2)A、B、C、D各点反应速率由快到慢的顺序为 。
(3)解释反应速率变化的原因 。
解析 (1)发生的反应为2H2O22H2O+O2↑,由图像知,当t=4 min时,H2O2分解完全,生成V(O2)=60 mL。
(2)因为随着反应的进行,c(H2O2)逐渐减小,反应逐渐变慢,因而反应由快到慢的顺序为D>C>B>A。
答案 (1)60 mL (2)D>C>B>A
(3)随着反应的进行,c(H2O2)逐渐减小,反应速率逐渐减小