- 508.00 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2017-2018学年江苏省海安高级中学高二下学期期中考试
化学
注意事项:
1.本试卷包括第Ⅰ卷选择题和第Ⅱ卷非选择题两部分。满分120分,考试时间100分钟。
2.作答选择题,必须用2B铅笔把答题卡上对应选项的方框涂满涂黑;作答非选择题,必须用书写黑色字迹的0.5毫米签字笔写在答题卡上的指定位置,在其它位置作答一律无效。交卷时只交答题卡。
3.可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5 Cu 64 Ag 108
第Ⅰ卷(选择题,共40分)
单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意。
1.“绿水青山就是金山银山”。下列做法与上述理念相违背的是
A.推广煤改气集中供暖 B.加快石油等化石燃料的开采和使用
C.开发太阳能等新能源汽车 D.将秸秆进行加工转化为乙醇燃料
2.下列有关化学用语表示正确的是
A.羟基的电子式: B.对硝基甲苯的结构简式:
C.乙炔的比例模型: D.2-乙基-1,3-丁二烯的键线式:
3.有4种碳架如下的烃,下列判断正确的是
a b c d
A.c和d是同分异构体 B.b和c是同系物
C.a和d都能发生加成反应 D.只有b和c能发生取代反应
4.下列有机物的命名不正确的是
A. 2-乙基丙烷 B. 3-甲基-1-丁炔
C. 2-丁醇 D. 邻甲基苯酚
5. 下列有关物质的性质与用途具有对应关系的是
A.乙醇具有还原性,75%乙醇溶液常用于医疗消毒
B.丙三醇具有很强的吸湿性,可用于配制汽车防冻液
C.乙炔燃烧放出热量,常用来焊接或切割金属
D.氟氯代烃(氟利昂)不溶于水,曾被广泛用作制冷剂
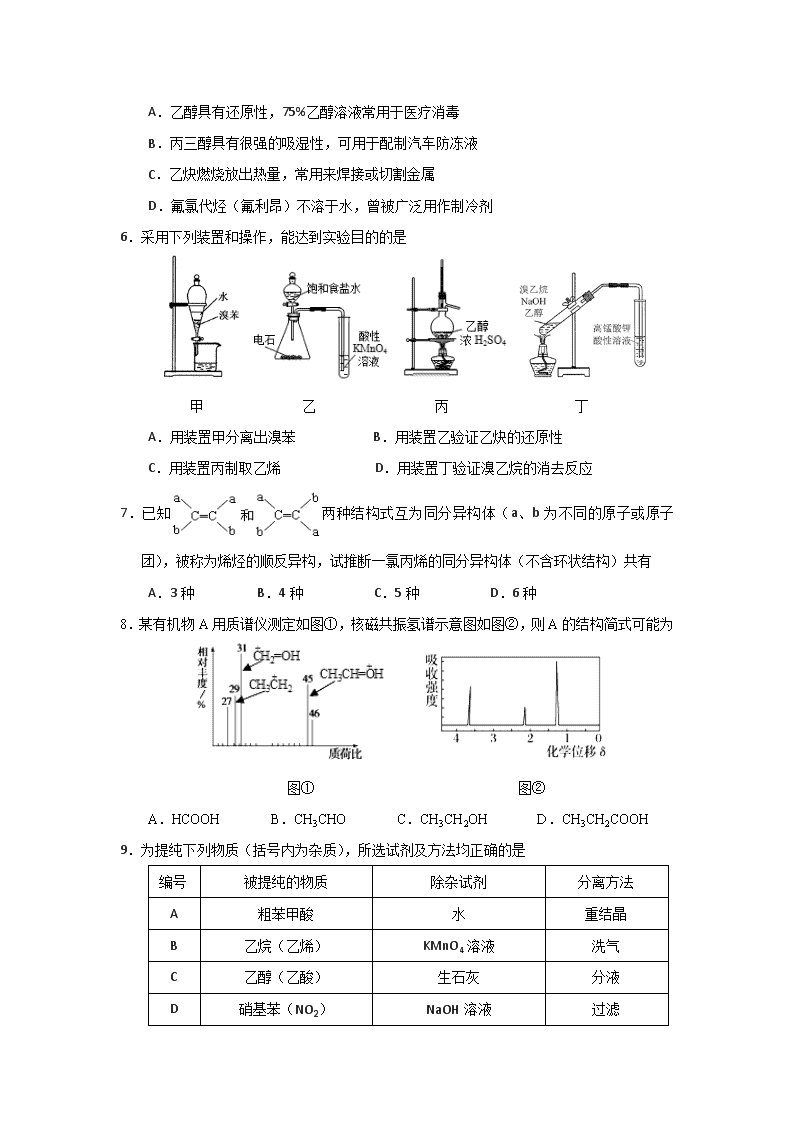
6.采用下列装置和操作,能达到实验目的的是
甲 乙 丙 丁
A.用装置甲分离出溴苯 B.用装置乙验证乙炔的还原性
C.用装置丙制取乙烯 D.用装置丁验证溴乙烷的消去反应
7.已知两种结构式互为同分异构体(a、b为不同的原子或原子团),被称为烯烃的顺反异构,试推断一氯丙烯的同分异构体(不含环状结构)共有
A.3种 B.4种 C.5种 D.6种
8.某有机物A用质谱仪测定如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为
图① 图②
A.HCOOH B.CH3CHO C.CH3CH2OH D.CH3CH2COOH
9.为提纯下列物质(括号内为杂质),所选试剂及方法均正确的是
编号
被提纯的物质
除杂试剂
分离方法
A
粗苯甲酸
水
重结晶
B
乙烷(乙烯)
KMnO4溶液
洗气
C
乙醇(乙酸)
生石灰
分液
D
硝基苯(NO2)
NaOH溶液
过滤
10.已知:乙醇可被强氧化剂直接氧化为乙酸。由经过三步反应可制得,设计最合理的三步反应类型依次是
A.加成、氧化、水解 B.加成、水解、氧化
C.水解、氧化、加成 D.水解、加成、氧化
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分。
11.莽草酸可用于合成药物达菲,其结构简式如图。下列关于莽草酸的说法正确的是
A.每个莽草酸分子中含有3个手性碳原子
B.莽草酸分子中所有的碳原子都在同一个平面上
C.1mol莽草酸最多能和4mol NaOH发生中和反应
D.一定条件下莽草酸可发生氧化、加成、消去反应
12.有机结构理论中有一个重要的观点:有机化合物分子中,原子(团)之间相互影响,从而导致化学性质不同。以下事实中,不能够说明此观点的是
A.乙烯能发生加成反应,乙烷不能发生加成反应
B.甲苯能使酸性高锰酸钾溶液褪色,甲烷不能使酸性高锰酸钾溶液褪色
C.乙酸能与NaHCO3溶液反应放出气体,而乙醇不能
D.苯硝化反应一般生成硝基苯,而甲苯硝化反应生成三硝基甲苯(TNT)
13.下列设计的实验方案,不能达到预期实验目的的是
A.用1-氯丙烷与氢氧化钠乙醇溶液共热制取丙烯时,1-氯丙烷中混有少量的2-氯丙烷
B.实验室制乙烯时,在酒精和浓硫酸的混合液中,放入几片碎瓷片,加热使液体温度迅速升到140℃
C.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置,待液体分层后,滴加硝酸银溶液
D.验证某有机物属于烃的含氧衍生物,可以测定该试样的质量及其试样完全燃烧后生成CO2和H2O的质量
14.煤的气化是煤高效、洁净利用的方向之一。右图为加热某地煤样所得煤气组成及体积分数随温度变化的曲线图。
下列说法正确的是
A.煤中只含有碳、氢两种元素
B.该煤气中所含的有机物是CH4、CnHm、CO
C.该煤气中CO体积分数小于CH4体积分数
D.低温有助于提高H2的含量
15.下列各组有机物无论以何种比例混合,只要混合物的总物质的量一定,则完全燃烧时消耗氧气的量恒定不变的是
A.C2H4和C2H6O2 B.C4H6和C3H8
C.C5H10和C7H6O2 D.C3H6O和C3H8O2
第Ⅱ卷(非选择题,共80分)
16.(12分)烃可以看作是有机化合物的母体,烃的来源有石油、天然气和煤等。
(1)下表是在1.013×105Pa下测得的几种烃的沸点:
结构简式
沸点/℃
结构简式
沸点/℃
CH3CH3
-88.6
CH2=CH2
-103.7
CH3CH2CH3
-42.2
CH2=CHCH3
-47.4
CH3CH2CH2CH3
-0.5
CH3CH2CH=CH2
-6.3
-11.7
-6.9
CH3CH2CH2CH2CH3
36.1
CH3CH2CH2CH=CH2
30
27.8
①从表中数据分析, 在1.013×105Pa、25℃时的状态是 ▲ (填气态、液态或固态)。
②醇类物质的沸点明显高于相对分子质量相近的烃,其原因是 ▲ 。
(2)石油裂解是一个复杂的过程,其产物为混合物。例如:
①上述烷烃和环烷烃裂解反应中,产物M的化学式为 ▲ ,N的化学式为 ▲ 。
②下列关于 的说法正确的是 ▲ 。(填序号)
A. 不溶于水且密度比水小
B.可用溴水区别 和
C.等质量的 和 完全燃烧时的耗氧量相同
(3)工业上裂解反应的产物都是气态小分子烷烃和烯烃的混合物,将它们逐一分离的方法是 ▲ 。
17.(15分)肉桂酸甲酯(代号M)是常用于调制具有草莓、葡萄、香子兰等香味的食用香精。用质谱法测得其相对分子质量为162,分子中C、H、O原子个数比为5∶5︰1,且分子中只含有1个苯环,苯环上只有一个取代基。现测出M的核磁共振氢谱谱图有6个峰,其面积之比为1︰2︰2︰1︰1︰3。利用红外光谱仪可初步检测有机化合物中的某些基团,现测得M分子的红外光谱如图1所示。
图1 图2
试回答下列问题:
(1)肉桂酸甲酯(M)的结构简式为 ▲ 。
(2)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如图2所示(图中球与球之间连线表示单键或双键)。G的结构简式为 ▲ 。
(3)用芳香烃A 为原料合成G的路线如下:
① A的结构简式为 ▲ 。
② F中所含官能团名称为 ▲ 。
③ C→D的反应类型为 ▲ 。
④写出同时满足下列条件的E的一种同分异构体的结构简式: ▲ 。
Ⅰ.属于芳香化合物,且含有醚键; Ⅱ.分子中有4种不同化学环境的氢。
⑤写出B→C的化学方程式: ▲ 。
18.(12分)0.2mol有机物A和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(气),产物通过浓硫酸,浓硫酸质量增加10.8g;再通过灼热CuO,充分反应后,CuO质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g。
(1)通过计算确定有机物A的分子式。(写出计算过程)
(2)若0.2mol有机物A恰好与9.2g金属钠完全反应,试确定有机物A的结构简式并命名。
19.(15分)实验室制乙烯并验证其性质,请回答下列问题:
(1)写出以乙醇为原料制取乙烯的化学方程式: ▲ 。
(2)某同学欲使用如图1所示装置制取乙烯。
①请你改正其中的错误: ▲ 。
②实验过程中发现烧瓶中出现黑色固体,这会导致生成的乙烯中含有杂质气体,请写出生成杂质气体的化学方程式: ▲ 。
(3)要验证乙烯的化学性质(装置如图2所示,尾气处理装置已略去),请将虚线框中的装置补充完整并标出所盛试剂。
(4)有些同学提出以溴乙烷为原料制取乙烯。
①该反应的化学方程式为: ▲ 。
②若以溴乙烷为原料,图2中虚线框内的装置 ▲ 省略(填“能”或“不能”),请说明理由: ▲ 。
20.(14分)立方烷()具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点。下面是立方烷衍生物I的一种合成路线:
回答下列问题:
(1)C的结构简式为 ▲ 。
(2)⑤的反应类型为 ▲ 。
(3)化合物A可由环戊烷经三步反应合成:
反应1的试剂与条件为 ▲ ;
反应3的化学方程式为 ▲ 。
(4)在I的合成路线中,互为同分异构体的化合物是 ▲ 。(填化合物代号)
(5)I与碱石灰共热可转化为立方烷。立方烷的核磁共振氢谱中有 ▲ 个峰。
(6)立方烷经硝化可得到六硝基立方烷,其可能的结构有 ▲ 种。
21.(12分)有机化学的核心思想是“结构决定性质”。回答下列问题:
(1)烯烃、炔烃在一定条件下都能与H2、HCN等发生加成反应,试从分子结构的特点解释其原因是 ▲ 。
(2)有机物 在不同条件下可能发生有机反应类型有:①取代 ②加成 ③消去 ④氧化 ⑤酯化 ⑥加聚,其中因分子结构中含-OH而可能发生的反应有 ▲ 。(填序号)
(3)乙炔是有机合成工业的一种原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。
①正四面体烷的分子式为 ▲ 。
②关于乙烯基乙炔和环辛四烯的说法错误的是 ▲ 。(填序号)
a.乙烯基乙炔分子中含有两种官能团
b.环辛四烯能使酸性KMnO4溶液褪色
c.1mol乙烯基乙炔最多能与2mol Br2发生加成反应
d.乙烯基乙炔分子中的所有原子一定共平面
③写出与苯互为同系物且一氯代物只有两种的物质的结构简式 ▲ 。
④工业上曾用CaC2与水反应生成乙炔,写出该反应的化学方程式 ▲ 。
高二化学(选修)参考答案和评分标准
单项选择题(本题包括10小题,每小题2分,共20分)
1.B 2.D 3.B 4.A 5.C 6.A 7.B 8.C 9.A 10.D
不定项选择题(本题包括5小题,每小题4分,共20分)
11.AD 12.A 13.BC 14.C 15.CD
16.(12分,每空2分)
(1)①气态
②醇类分子间存在氢键
(2)①H2 C5H8
②AB
(3)降低温度
17.(15分,除第⑶题④外,其余每空2分)
(1)
(2)
(3)①
②碳碳双键、羧基 (各1分)
③氧化反应
④ 等(合理答案均给分) (3分)
⑤
18.(12分)
(1)有机物A燃烧生成水10.8g,n(H2O)==0.6mol (1分)
CuO + CO Cu + CO2 固体减少△m
1mol 16g
n(CO) 3.2g
解得 n(CO)=0.2mol (1分)
根据碳元素守恒可知,CO与CuO反应生成的CO2的质量为0.2mol×44g/mol=8.8g
则有机物A燃烧生成的CO2的质量为17.6g-8.8g=8.8g
n(CO2)==0.2mol (1分)
1mol有机物A中含有:n(C)==2mol (1分)
n(H)==6mol (1分)
根据氧元素守恒可知,1mol有机物A中含有:
n(O)==2mol (2分)
所以有机物A的分子式为C2H6O2 (1分)
(2)HOCH2CH2OH 乙二醇 (各2分)
19.(15分,除第⑸题外,其余每空2分)
(1)CH3CH2OHCH2=CH2↑+H2O
(2)①将温度计水银球插入反应液中控制温度
②C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
(3)
(4)CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
(5)不能 (1分) 挥发的乙醇蒸汽也能使酸性高锰酸钾溶液褪色 (2分)
20.(14分,每空2分)
(1)
(2)消去反应
(3)Cl2/光照
(4)G和H
(5)1
(6)3
21.(12分,每空2分)
(1)分子结构中都有不饱和键(或π键)
(2)①③④⑤
(3)①C4H4
②c
③ 或
④CaC2+2H2O→Ca(OH)2+C2H2↑