- 275.50 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
陕西省西安中学2018-2019学年高二(理科班)上学期期末考试化学试题
1. 下列各组物质中,都是强电解质的是( )
A. HBr、HCl、BaSO4
B. NH4Cl、CH3COOH、Na2S
C. NaOH、Ca(OH)2、NH3·H2O
D. HClO、NaF、Ba(OH)2
【答案】A
【解析】
在溶液中能完全电离的电解质是强电解质,A正确.醋酸/一水合氨和次氯酸都是弱电解质.答案选A.
2.由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为
A. 0.15 mol·L-1 B. 0.2 mol·L-1 C. 0.3 mol·L-1 D. 0.4 mol·L-1
【答案】C
【解析】
pH=1,得:c(H+)="0.1" mol·L-1
利用电荷守恒:3c(Al3+)+ c(K+)+ c(H+)= 2c(SO42-),代入数据,求得C正确
3.下列方程式书写正确的是
A. HCO3-在水溶液中的电离方程式:HCO3-+H2OH3O++CO32-
B. H2SO4的电离方程式H2SO42H++SO42-
C. CO32-的水解方程式:CO32-+2H2OH2CO3+2OH-
D. CaCO3的电离方程式:CaCO3Ca2++CO32-
【答案】A
【解析】
【分析】
强电解质在水溶液中是完全电离,电离方程式用“=”表示,弱电解质则是部分电离,电离方程式用“”表示,多元弱酸水解分步进行,据此分析作答。
【详解】A. 碳酸氢根离子在溶液中电离出碳酸根离子和氢离子,可表示为:HCO3-+H2OH3O++CO32-,或HCO3-H++CO32-,故A项正确;
B. 硫酸为二元强酸,在水溶液中发生完全电离,其电离方程式为:H2SO4 = 2H++SO42-,故B项错误;
C. 碳酸根离子水解生成碳酸氢根离子和氢氧根离子,其水解过程分两步进行,以第一步为主,水解方程式为:CO32-+H2OHCO3-+OH-,故C项错误;
D. 碳酸钙为强电解质,其电离方程式为:CaCO3 = Ca2++CO32-,故D项错误;
答案选A。
【点睛】本题侧重考查强弱电解质的电离方程式及盐类的水解方程式的正确书写,其中D选项是学生的易错易混点,有些难溶性的盐如碳酸钙、硫酸钡等,在熔融状态下能够完全电离出阴阳离子,属于强电解质。其是否是强弱电解质要根据定义进行判断,而不可和物质的溶解性混为一谈,学生要加以识别并记忆。
4.难溶电解质AB2饱和溶液中,c(A2+)=xmol·L-1,c(B-)=ymol·L-1,则Ksp值为
A. 1/2xy2 B. xy C. xy2 D. 4xy2
【答案】C
【解析】
【分析】
难溶电解质AB2的电离方程式为:AB2(s) ⇌ A2+(aq) + 2B-(aq),Ksp = c(A2+)·c2(B-),据此分析解答。
【详解】难溶电解质AB2的电离方程式为AB2(s) ⇌ A2+(aq) + 2B-(aq),
AB2饱和溶液中,c(A2+)= x mol•L-1,c(B-)= y mol•L-1,
则Ksp = c(A2+)·c2(B-) = xy2,故C项正确;
答案选C。
5. 下列叙述正确的是( )
A. 将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)>c(NH4+)
B. 两种醋酸溶液的物质的量浓度分别为c1和c2,pH的别为a和a+1,则c1=10c2
C. pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D. 向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大
【答案】C
【解析】
由电荷守恒可知c(NH4+)+c(H+)=2c(SO42-)+c(OH-),当pH=7时,c(NH4+)=2c(SO42-),故A项错;醋酸是弱酸,浓度越大,电离程度越小,当两溶液pH相差1时,c1≠10c2,B项错;pH=11的NaOH与pH=3的醋酸等体积混合后溶液显酸性,滴入石蕊试液呈红色,C项对;氨水存在电离平衡:NH3·H2ONH4++OH-,加(NH4)2SO4固体,平衡左移,导致减小,D项错。
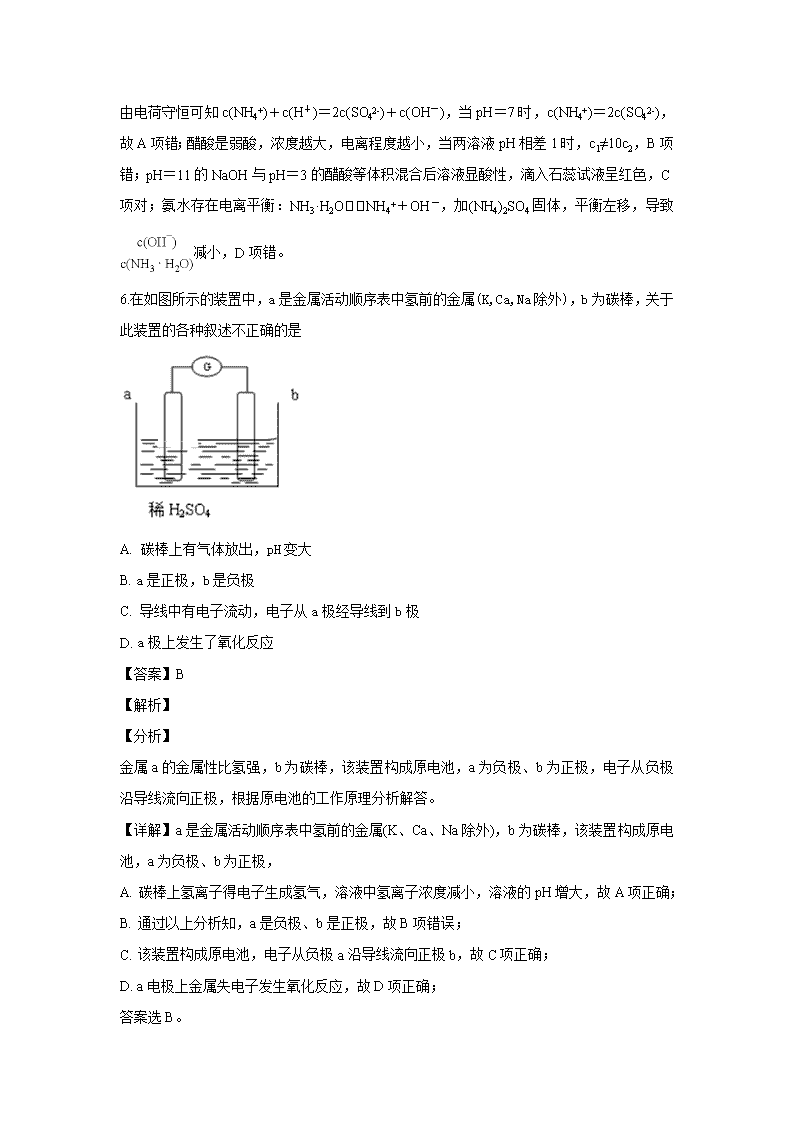
6.在如图所示的装置中,a是金属活动顺序表中氢前的金属(K,Ca,Na除外),b为碳棒,关于此装置的各种叙述不正确的是
A. 碳棒上有气体放出,pH变大
B. a是正极,b是负极
C. 导线中有电子流动,电子从a极经导线到b极
D. a极上发生了氧化反应
【答案】B
【解析】
【分析】
金属a的金属性比氢强,b为碳棒,该装置构成原电池,a为负极、b为正极,电子从负极沿导线流向正极,根据原电池的工作原理分析解答。
【详解】a是金属活动顺序表中氢前的金属(K、Ca、Na除外),b为碳棒,该装置构成原电池,a为负极、b为正极,
A. 碳棒上氢离子得电子生成氢气,溶液中氢离子浓度减小,溶液的pH增大,故A项正确;
B. 通过以上分析知,a是负极、b是正极,故B项错误;
C. 该装置构成原电池,电子从负极a沿导线流向正极b,故C项正确;
D. a电极上金属失电子发生氧化反应,故D项正确;
答案选B。
【点睛】原电池工作的原理口诀可概括为“两极一液一连线,活泼金属最优先,负失氧正得还,离子电极同性恋”,可加深学生对原电池的理解与记忆。本题的C选项,要注意导线中有电子流动,电子从a极经导线到b极,而不是经过电解质溶液到b极,学生要火眼金睛,提高做题正答率。
7.蓄电池放电时是起原电池的作用,在充电时起电解池的作用。下式是爱迪生蓄电池分别在充电、放电时的反应: Fe + NiO2+ 2H2OFe(OH)2+ Ni(OH)2下列有关爱迪生电池的各种推断中不正确的是
A. 放电时铁做负极,NiO2做正极
B. 充电时阴极上的电极反应为:
C. 放电时,电解质溶液中的阴离子是向正极方向移动
D. 蓄电池的两个电极必须浸入在碱性溶液中
【答案】C
【解析】
试题分析:放电时,负极发生氧化反应,正极发生还原反应,根据放电反应方程式,铁发生氧化反应,所以放电时铁做负极,NiO2做正极,故A正确;充电时阴极为放电时的负极,充电时阴极上的电极反应为,故B正确;放电时是原电池,原电池中阴离子移向负极,故C错误;若用酸性电解液,会破坏电池,故D正确。
考点:本题考查化学电源。
8.常温下,下列各组离子在指定溶液中能大量共存的是
A. 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I-
B. pH值为1的溶液:Cu2+、Na+、Mg2+、NO3-
C. 水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+
D. 所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+
【答案】B
【解析】
【分析】
A. 滴加石蕊试液显红色的溶液,显酸性,离子之间发生氧化还原反应;
B. pH值为1的溶液,显酸性;
C. 水电离出来的c(H+)=10-13 mol/L的溶液,为酸或碱溶液;
D. 离子之间相互促进水解,发生双水解。
【详解】A. 滴加石蕊试液显红色的溶液,显酸性,Fe3+、I−发生氧化还原反应,其离子方程式为:2Fe3++ 2I− = 2Fe2+ + I2,则不能共存,故A项错误;
B. pH值为1的溶液,显酸性,该组离子之间不反应,可大量共存,故B项正确;
C. 水电离出来的c(H+)=10-13 mol/L的溶液,为酸或碱溶液,酸溶液中不能大量存在HCO3−,碱溶液中HCO3−、OH−、Ba2+反应生成沉淀和水,故C项错误;
D. CO32−、Al3+相互促进水解,不能共存,故D项错误;
答案选B。
9.对于常温下pH为1的硝酸溶液,下列叙述正确的是
A. 该溶液l0mL稀释至1000mL后,pH等于4
B. 向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和
C. 该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-12
D. 该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的的100倍
【答案】B
【解析】
【分析】
A. 硝酸溶液中硝酸完全电离,溶液稀释100倍,溶液pH增大2个单位;
B. pH为13的氢氧化钡溶液,氢氧根的浓度是0.1 mol/L;
C. 常温下pH为1的硝酸溶液中,水电离出的氢氧根离子浓度和氢离子浓度相同为10-13 mol/L,故该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-1:10-13=1012;
D. 常温下pH为1的硝酸溶液中酸中氢离子浓度为10-13 mol/L,pH为3的硝酸水电离出的氢离子浓度为10-11 mol/L,故后者是前者的100倍。
【详解】A. 硝酸溶液中硝酸完全电离,溶液稀释100倍,溶液pH增大2个单位,pH等于3,故A项错误;
B. pH为13的氢氧化钡溶液,氢氧根的浓度是0.1 mol/L,pH为1的硝酸溶液氢离子浓度是0.1 mol/L,等体积混合,酸碱的物质的量相同,则恰好中和溶液呈中性,故B项正确;
C. 常温下pH为1的硝酸溶液中,水电离出的氢氧根离子浓度和氢离子浓度相同为10−13 mol/L,故该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10−1:10−13 = 1012,故C项错误;
D. 常温下pH为1的硝酸溶液中水电离出的c(H+)为10−13 mol/L,pH为3的硝酸水电离出的
c(H+)为10−11 mol/L,故后者是前者的100倍,故D项错误,
答案选B。
10.下列操作中,能使电离平衡H2OH++OH-向右移动且溶液呈酸性的是
A. 向水中加入NaHSO4溶液 B. 将水加热到100℃,使pH=6
C. 向水中加入Na2CO3溶液 D. 向水中加入Al2(SO4)3固体
【答案】D
【解析】
A. 向水中加入NaHSO4溶液,硫酸氢钠完全电离:NaHSO4═Na++H++SO42−,溶液中氢离子浓度增大,水的电离平衡向左移动,故A错误;B. 升高温度,水的电离程度增大,但是溶液中氢离子浓度等于氢氧根离子浓度,溶液显中性,故B错误;C. 向水中加入碳酸钠溶液,碳酸根离子水解促进水的电离,使溶液呈碱性,故C错误;D. 向水中加入硫酸铝固体,铝离子水解促进水的电离,使溶液呈酸性,故D正确;答案选D
点睛:本题考查水的电离平衡及影响因素。能使水的电离H2O⇌H++OH-平衡向右移动,说明加入的物质能和氢离子或氢氧根离子反应而促进水的电离;溶液呈酸性,说明加入的物质造成了溶液中氢氧根离子浓度小于氢离子浓度,据此分析解答该题即可。
11. 为了降低某水库的铁闸门被腐蚀的速率,可以采取如右图所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A. 铜 B. 钠 C. 锌 D. 石墨
【答案】C
【解析】
由图可知该防护属于牺牲阳极的阴极保护法,所以材料R的活泼性应强于铁的,因为金属钠极易和水反应,所以不能选择B选项,正确的答案是C。
12.将pH=3的盐酸溶液和pH=11的氨水等体积混合后,溶液中离子浓度关系正确的是
A. c(NH4+)>c(Cl–)>c(H+)>c(OH–) B. c(NH4+)>c(Cl–)>c(OH–)>c(H+)
C. c(Cl–)>c(NH4+)>c(H+)>c(OH–) D. c(Cl–)>c(NH4+)>c(OH–)>c(H+)
【答案】B
【解析】
氨水是弱碱,所以pH=11的氨水的浓度大于0.001mol/L,因此在反应中氨水是过量的,溶液显碱性,答案选B。
13.用1.0 mol·L-1 NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积V关系如右图所示。原硫酸溶液的物质的量浓度和反应后溶液的总体积是
A. 1 mol·L-160 mL B. 0.5 mol·L-1 80 mL
C. 0.5 mol·L-1 60 mL D. 1 mol·L-1 80 mL
【答案】B
【解析】
【分析】
根据硫酸溶液的pH确定氢离子浓度,再根据硫酸和氢离子之间的关系式确定硫酸浓度;根据硫酸和氢氧化钠反应的关系式计算氢氧化钠溶液的体积,硫酸和氢氧化钠溶液体积就是完全反应后溶液的总体积。
【详解】根据图象知,硫酸的pH=0,则c(H+) = 1 mol/L c(H2SO4) = c(H+) = 0.5 mol/L;完全反应时氢氧化钠溶液的体积为40 mL,根据反应中氢氧化钠和硫酸的关系式得:n(NaOH) = 2n(H2SO4) = 2×0.5 mol/L×0.04 L = 1 mol/L×V,所以V(NaOH) = = 40 mL,则混合溶液体积 = 40mL×2 = 80 mL,故B项正确,
答案选B。
14.准确量取25.00 mL高锰酸钾溶液,可选用的仪器是( )
A. 50 mL量筒 B. 50 mL酸式滴定管
C. 10 mL量筒 D. 50 mL碱式滴定管
【答案】B
【解析】
【分析】
量筒只能估读到0.1,滴定管是精密仪器,可估读到0.01,高锰酸钾是强氧化剂,需选用酸式滴定管,据此分析作答。
【详解】A. 50 mL量筒只能估读到0.1 mL,所以50 mL量筒不能精确地量取25.00 mL高锰酸钾溶液,故A项错误;
B. 滴定管是能精确计量的仪器,准确量取25.00mL溶液,应用50mL滴定管量取,高锰酸钾具有强氧化性,腐蚀橡胶,应该用酸式滴定管量取,故B项正确;
C. 10 mL量筒量度太小,且精确度不够,故C项错误;
D. 碱式滴定管的下端有一段橡皮管,高锰酸钾具有强氧化性,腐蚀橡胶,要用酸式滴定管不能用碱式滴定管量取,故D项错误;
答案选B。
【点睛】准确量取25.00 mL高锰酸钾溶液,需要用精密量具,精确到0.1,估读到0.01,学过的量具中,滴定管与移液管是能精确计量的仪器,要注意高锰酸钾溶液的强氧化性。
15. 下列说法不正确的是 ( )
A. 使用滴定管时,滴定管必须用待装液润洗2~3次
B. 滴定操作中,若用待测液润洗锥形瓶,将导致测定结果偏高
C. 用10 mL的量筒量取8.58 mL 0.10 mol·L-1的稀盐酸
D. 稀释浓硫酸时,将浓硫酸缓缓加入水中,并不断用玻璃棒搅拌
【答案】C
【解析】
C项,10 mL的量筒只能精确到0.1 mL,故不能量取8.58 mL的稀盐酸。
16. 常温下,一定量的醋酸与氢氧化钠溶液发生中和反应。下列说法正确的是
A. 当溶液中c(CH3COO-)=c(Na+)时,醋酸与氢氧化钠恰好完全反应
B. 当溶液中c(CH3COO-)=c(Na+)时.一定是氢氧化钠过量
C. 当溶液中c(CH3COO-)=c(Na+)>c(H+)=c(OH-)时,一定是醋酸过量
D. 当溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)时,一定是氢氧化钠过量
【答案】C
【解析】
试题分析:A.若醋酸和氢氧化钠恰好反应,由于生成物醋酸钠水解,溶液显碱性,故A错误;B.氢氧化钠过量时,溶液呈碱性,则c(CH3COO-)<c(Na+
),故B错误;C.根据电荷守恒c(CH3COO-)+c(OH-)=c(Na+)+c(H+)可知,当c(CH3COO-)=c(Na+)时,c(OH-)=c(H+),即溶液显中性,此时醋酸应该是过量的,故C正确;D.也可能是二者恰好反应,故D错误;故选C。
考点:考查了酸碱混合的定性判断以及离子浓度大小比较的相关知识。
17.分离下列物质时可用重结晶法的是( )
A. 蔗糖中含有泥沙 B. 汽油中含有水
C. 硫粉和铁粉 D. 氯化钠和硝酸钾混合物
【答案】D
【解析】
【分析】
重结晶是将晶体溶于溶剂或熔融以后,又重新从溶液或熔体中结晶的过程,适用于分离两种溶解度随温度变化差异较大的物质。
【详解】A. 蔗糖易溶于水,泥沙不溶于水,不能用重结晶方法分离,可以用过滤的方法分离,故A项错误;
B. 汽油与水互不相溶,通常用分液的方法分离,故B项错误;
C. 硫粉和铁粉均为固体难溶于水,不能用重结晶的方法分离,故C项错误;
D. 氯化钠和硝酸钾都易溶于水,但是二者溶解度随温度变化差异较大,可以用重结晶的方法分离,故D项正确;
答案选D。
18.一定量的某有机物完全燃烧后,将燃烧产物通过足量的石灰水,经过滤可得沉淀10 g,但称量滤液时,其质量只减少2.9 g,则此有机物不可能是( )
A. 乙烷 B. 乙烯 C. 乙醇 D. 乙二醇
【答案】B
【解析】
m(CaCO3)=10g,称量滤液时质量只减少2.9克,即:m(石灰水)−m(滤液)=2.9g,根据质量守恒,m(CO2)+m(H2O)+m(石灰水)=m(滤液)+m(CaCO3),所以m(CO2)+m(H2O)=10g−2.9g=7.1g,而10gCaCO3对应的m(CO2)=10g÷100×44=4.4g,所以m(H2O)=7.1−4.4=2.7g,4.4gCO2中n(C)=4.4g÷44g∙mol-1= 0.1mol,2.7gH2O中n(H)=2.7g÷18g∙mol-1×2=0.3mol,所以原子个数比为1:3,不可能是乙烯。故选B。
点睛:本题考查有机物的推断,题目难度不大。通过计算得出燃烧产物的质量,可求得碳氢比,从而推断可能的结果,利用差量法计算水的质量为解题的关键。
19.在核磁共振氢谱中出现两组峰,其氢原子数之比为3∶2的化合物是( )
【答案】D
【解析】
A中有2组峰,其氢原子数之比为3∶1。B中有3组峰,其氢原子数之比为3∶1∶1。C中有3组峰,其氢原子数之比为3∶1∶4。所以答案是D。
20. 用相对分子质量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为
A. 3种 B. 4种 C. 5种 D. 6种
【答案】D
【解析】
试题分析:相对分子质量为43的烷基为:—CH2CH2CH3和—CH(CH3)2,分别取代苯环上甲基的邻位,间位、对位,共6中同分异构体。
考点:同分异构体的书写。
21.某烷烃主链上有4个碳原子的同分异构体有2种,含有相同碳原子数且主链上也有4个碳原子的单烯烃的同分异构体有( )
A. 2种 B. 4种
C. 5种 D. 7种
【答案】B
【解析】
【分析】
先根据烷烃的条件,确定烷烃的分子式,然后再根据官能团位置异构确定单烯烃的同分异构体。
【详解】第一步:确定该烷烃碳原子个数,
①主链为4个碳原子的烷烃,其支链只能是甲基(不可能是乙基,否则主链超过4个碳原子).
②主链为4个碳原子的烷烃,支链数最多4个(下面的0,是指该物质只有一种,没有同分异构体)
甲基的个数同分异构体
1个 0
2个 2
3个 0
4个 0
③结论:该烷烃总共有6个碳原子,
第二步:分析烯烃的同分异构体数目
①双键在1号位,,有以下3种:2−乙基丁烯、2,3−二甲基丁烯、3,3−二甲基丁烯
②双键在2号位,,有1种:2,3−二甲基−2−丁烯
结论:共有4种,故B项正确;
答案选B。
22.对于苯乙烯的下列叙述:①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯中;⑤能与浓硝酸发生取代反应;⑥所有的原子可能共平面,其中正确的是( )
A. 仅①②④⑤ B. 仅①②⑤⑥
C. 仅①②④⑤⑥ D. 全部正确
【答案】C
【解析】
【分析】
苯乙烯中含有苯环和碳碳双键,则具备苯和烯烃的化学性质,且苯环为平面结构、乙烯为平面结构,以此来解答。
【详解】①苯乙烯中含有碳碳双键,则能使酸性KMnO4溶液褪色,故①正确;
②苯乙烯中含有碳碳双键,则可发生加聚反应,故②正确;
③苯乙烯为有机物,不溶于水,故③错误;
④根据相似相溶可知,苯乙烯可溶于苯中,故④正确;
⑤苯环能与浓硝酸发生取代反应,则苯乙烯能与浓硝酸发生取代反应,故⑤正确;
⑥苯环为平面结构、乙烯为平面结构,且苯环中的C
原子与乙烯中的碳原子直接相连,则所有的原子可能共平面,故⑥正确;
故C项正确;
答案选C。
23.1 mol乙烯与氯气发生加成反应后,再与氯气发生完全取代反应,整个过程中消耗氯气( )
A. 3 mol B. 4 mol C. 5 mol D. 6 mol
【答案】C
【解析】
【分析】
乙烯和氯气发生加成反应生成二氯乙烷,1mol双键加成需要1mol的氯气;有机物中的氢原子被氯原子取代时,氯气的物质的量与取代的氢原子的物质的量相等,所以最多消耗的氯气为这两部分之和。
【详解】C2H4+Cl2CH2ClCH2Cl,所以1 mol乙烯与氯气发生加成反应需要氯气1 mol;
所以1 mol CH2ClCH2Cl与氯气发生取代反应,最多需要4 mol氯气,这两部分之和为1 mol+4 mol = 5 mol,故C项正确;
答案选C。
24. 进行一氯取代反应后,生成4种沸点不同的有机产物的是( )
A. 2,2-二甲基丁烷 B. 2,2,3-三甲基戊烷
C. 2,3-二甲基戊烷 D. 2,2-二甲基-3-乙基戊烷
【答案】D
【解析】
试题分析:A、2,2-二甲基丁烷有3种氢原子,则一氯取代反应后,生成3种沸点不同的有机产物,A错误;B、2,2,3-三甲基戊烷有5种氢原子,则一氯取代反应后,生成5种沸点不同的有机产物,B错误;C、2,3-二甲基戊烷有6种氢原子,则一氯取代反应后,生成6种沸点不同的有机产物,C错误;D、2,2-二甲基-3-乙基戊烷有4种氢原子,则一氯取代反应后,生成4种沸点不同的有机产物,D正确。答案选D。
考点:同分异构体
25.有A,B两种烃,含碳的质量分数相同,关于A和B的关系的下列说法正确的是( )
A. A和B一定是同分异构体
B. A和B一定不是同系物
C. A和B分子中含氢元素质量分数相同
D. A和B各amol完全燃烧生成CO2的质量一定相同
【答案】C
【解析】
分析:根据烃中只有碳氢两种元素,利用碳的质量分数、氢的质量分数求出最简式,最简式相同,可能是同分异构体,也可能是同系物,据此回答问题。
详解:A、因烃中只有碳氢两种元素,碳质量分数相同,所以氢的质量分数也相同,则最简式相同,可能是同分异构体,还可能是同系物,故A错误;
B、因烃中只有碳氢两种元素,碳质量分数相同,所以氢的质量分数也相同,则最简式相同,可能是同系物,故B错误;
C、因烃中只有碳氢两种元素,碳质量分数相同,所以氢的质量分数也相同,则最简式一定相同,所以C选项是正确的;
D、A和B的最简式相同,各amol完全燃烧生成二氧化碳的物质的量取决于分子中碳原子的数目,只有互为同分异构体时生成的二氧化碳的质量才相等,故D错误。
所以C选项是正确的。
26.(1)相同物质的量浓度的下列各溶液:NaX、NaY、NaZ,其PH值依次为9、11、10,则HX、HY、HZ的酸性由强到弱的顺序为:___________________。
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是________________ 。
(3)把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池。若a b相连,a为负极;c d相连,c为负极;a c相连,c为正极;b d相连,b为正极,则四种金属的活动性由强到弱顺序为:_____________________________。
(4)某温度时,水的离子积常数Kw = 10-13,将该温度下pH=11的Ba(OH)2溶液a L与pH = 1的H2SO4溶液b L混合(设混合溶液体积为两者之和,固体体积忽略不计),若所得混合溶液为中性,则a∶b =_________________;若a∶b = 9∶2,则所得溶液pH=_______。
【答案】 (1). HX>HZ>HY (2). Al2O3 (3). a>c>d>b (4). 10∶1 (5). 2
【解析】
【分析】
(1)根据酸根离子水解程度越大,对应的酸越弱来解答;
(2)先判断是否水解及水解产物,再根据水解产物判断灼烧时的分解产物;
(3)原电池中,负极材料为较活泼的金属,发生氧化反应,正极为较不活泼的金属,发生还原反应,以此判断金属的活动性;
(4)水的离子积常数KW=10-13,pH=11的Ba(OH)2溶液中氢氧根离子浓度为0.01mol/L,pH=1的H2SO4溶液中氢离子浓度为0.1mol/L,若所得混合液为中性,酸碱恰好完全反应,据此列式计算出a:b的值;先根据上述计算结果判断酸过量,然后计算出混合液中氢离子浓度及溶液的pH。
【详解】(1)因pH越大,说明酸根离子水解程度较大,其对应的酸越弱。NaX、NaY、NaZ,其pH值依次为9、11、10,则HX、HY、HZ的酸性由强到弱的顺序:HX>HZ>HY,
故答案为:HX>HZ>HY;
(2)AlCl3是强酸弱碱盐,能水解生成氢氧化铝和氯化氢,AlCl3+3H2O⇌Al(OH)3+3HCl,HCl具有挥发性,所以在加热蒸发、蒸干,灼烧过程中挥发消失;灼烧Al(OH)3,Al(OH)3能分解生成氧化铝和水2Al(OH)3Al2O3+3H2O,水在加热过程中蒸发掉,所以最后得到的白色固体是Al2O3,
故答案为:Al2O3;
(3)若a、b相连时,a为溶解,则a为负极,活动性a>b;c、d相连时c为负极,活动性c>d;a、c相连时c为正极,a为负极,活动性a>c;b、d相连时b为正极,d为负极,活动性d>b;则金属的活动性由强到弱顺序为:a>c>d>b,
故答案为:a>c>d>b;
(4)某温度时,水的离子积常数KW = 10-13,pH=11的Ba(OH)2溶液中氢氧根离子浓度为0.01mol/L,pH=1的H2SO4溶液中氢离子浓度为0.1mol/L,若所得混合液为中性,酸碱恰好完全反应,则有:n(H+)=n(OH-),即:0.01 mol/L×a L=0.1 mol/L×b L,则a:b=0.1:0.01=10:1;当a:b=10:1时二者恰好反应,则a:b=9:2,说明酸过量,混合后的溶液中
c(H+) =,将a = b带入可得,c(H+) = 0.01 mol/L,则溶液pH = 2,
故答案为:10:1;2。
27.Ⅰ.某同学将一试管斜立倒置于水槽中,并在试管内放了一枚铁钉,放置数天后观察:
(1)若试管内液面上升,则发生_____________腐蚀,正极反应式为________。
(2)若试管内液面下降,则发生______________腐蚀,正极反应式为_________。
Ⅱ.如图所示装置,两玻璃管中盛满滴有酚酞的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
(1)接通S1 后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。此时该装置中发生的化学方程式________________________________ 。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,此时:
(2)该装置名称为_______________________。
(3)C(Ⅱ)的电极名称是______________________(填写正极或负极)
(4)C(Ⅰ)电极反应式是:_______________________________。
【答案】 (1). 吸氧 (2). O2+2H2O+4e- = 4OH- (3). 析氢 (4). 2H++2e- = H2↑ (5). 2NaCl+2H2O2NaOH+H2↑+Cl2↑ (6). 原电池 (7). 正极 (8). H2-2e-+2OH- = 2H2O
【解析】
【分析】
Ⅰ.(1)根据试管内液面上升,说明试管中气体减少,则发生了吸氧腐蚀,Fe作负极失电子,O2作正极得电子生成氢氧根离子;
(2)根据试管内液面下降,说明试管中气体增加,则发生了析氢腐蚀,正极上氢离子得电子生成氢气;
Ⅱ.接通S1后,该装置是电解池,C(Ⅰ)附近溶液变红,则C
(Ⅰ)电极附近氢离子放电生成氢氧化钠和氢气,说明C(Ⅰ)电极是阴极,C(Ⅱ)是阳极,而阳极上氯离子放电生成氯气;断开S1,接通S2,电流表的指针发生偏转,该装置构成原电池,C(Ⅱ)电极上氯气得电子发生还原反应,为原电池正极,则C(Ⅰ)为原电池负极,据此分析作答。
【详解】Ⅰ.生铁中含有碳,铁、碳和合适的电解质溶液构成原电池,
(1)若试管内液面上升,说明试管内气体因和水反应而使其压强减小,发生的是吸氧腐蚀,铁作负极,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e- = 4OH-,
故答案为:吸氧;O2+2H2O+4e- = 4OH-;
(2)若试管内液面下降,说明金属的腐蚀中生成气体导致压强增大,则金属发生的是析氢腐蚀,正极上氢离子得电子发生还原反应,电极反应式为:2H++2e- = H2↑,
故答案为:析氢;2H++2e- = H2↑。
Ⅱ.(1)接通S1 后,C(Ⅰ)附近溶液变红,则C(Ⅰ)电极附近水中的氢离子放电生成氢氧化钠和氢气,说明C(Ⅰ)电极是阴极,C(Ⅱ)是阳极,而阳极上氯离子放电生成氯气,其电解反应方程式为:2NaCl+2H2O2NaOH+H2↑+Cl2↑,
故答案为:2NaCl+2H2O2NaOH+H2↑+Cl2↑;
(2)断开S1,接通S2,电流表的指针发生偏转,氢气和氯气发生自发的氧化还原反应,该装置构成原电池,
故答案为:原电池;
(3)原电池反应中,C(Ⅱ)电极上氯气得电子发生还原反应,为原电池正极,
故答案为:正极;
(4))原电池反应中,C(Ⅰ)电极原电池负极,氢气失电子发生氧化反应,电解质溶液为氢氧化钠,其反应式是:H2-2e-+2OH- = 2H2O,
故答案为:H2-2e-+2OH- = 2H2O。
【点睛】本题侧重考查电化学腐蚀及其电化学反应基本原理,关于电化学基础的综合题型是学生做题的难点,在解题主要抓住以下几个方面:
(1)先判断是原电池原理还是电解池原理;
(2)若为原电池,则考虑正负极反应、电子的转移及其反应现象等,根据电解质溶液的酸碱性会书写电极反应式;
(3
)若为电解池,则需要先看是惰性电极还是活性电极,如果是惰性电极,则根据阴阳极的放电顺序进行解答;相反,若为活性电极,需要注意阳极的金属电极要先失电子变成金属阳离子,阴极则直接利用阳离子的放电顺序分析即可,这就要求学生必须熟记电解池原理的阴阳极放电顺序,做题时才能游刃有余,分析到位。
28.苯和溴的取代反应的实验装置如下图所示,其中A为带支管口的试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉。填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):____________________。
(2)试管C中苯的作用是__________________________________________________。反应开始后,观察D和E两试管,D中看到的现象为_____________________________,E中看到的现象为_____________________________。
(3)反应2 min~3 min后,在B中可观察到的现象是__________________________________________。
(4)在上述整套装置中,具有防倒吸的仪器有________(填字母)。
【答案】 (1). (2). 除去HBr气体中混有的溴蒸气 (3). 紫色变红 (4). 淡黄色沉淀 (5). 瓶底有无色油状液体产生 (6). D、E、F
【解析】
【分析】
(1)苯和液溴在Fe作催化剂条件下能发生取代反应生成溴苯与HBr;
(2)溴易挥发,易溶于有机溶剂;溴化氢溶于水得到强酸,且与硝酸银反应生成淡黄色AgBr沉淀,据此分析作答;
(3)反应生成的溴苯密度比水大;
(4)根据防倒吸的原理进行分析。
【详解】(1)苯和液溴在Fe作催化剂条件下能发生取代反应生成溴苯与HBr,反应方程式为:,
故答案为:
;
(2)溴易挥发,易溶于有机溶剂,用苯可除去HBr气体中混有的溴蒸气Br2蒸气,防止对D和E装置中反应的干扰;
故答案为:除去HBr气体中混有的溴蒸气;
(3)新生成的溴苯为无色油状液体,密度比水大,故反应2 min~3 min后,在B中可观察到的现象是:瓶底有无色油状液体产生,
故答案为:瓶底有无色油状液体产生;
(4)C装置导管插入液面中,不能起到防倒吸功能,而D、E装置中,导管没有插入吸收液中,而是悬于上方,利用易溶于吸收液的气体下冲动力使气体被吸收,可起到防倒吸的作用;F装置中导管内压强减少,吸收液上升到漏斗中,由于漏斗容积较大,导致烧杯中液面下降,使漏斗口脱离液面,漏斗中的吸收液受自身重力的作用又流回烧瓶内,从而防止吸收液的倒吸,故答案为:D、E、F,
故答案为:D、E、F。
29.Ⅰ.有机物A由碳、氢、氧三种元素组成,现取3 g A与4.48 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸质量增加3.6 g,碱石灰质量增加4.4 g,则该有机物的分子式为__________。
Ⅱ.有机物A的相对分子质量为74,其红外光谱图(示意图)如图,则该分子的结构简式为____________,按照官能团分类,该物质属于__________。
Ⅲ.常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH
溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
实验
编号
HA的物质的量浓度(mol·L-1)
NaOH的物质的量浓度(mol·L-1)
混合后溶液的pH
甲
0.1
0.1
pH=a
乙
0.12
0.1
pH=7
丙
0.2
0.1
pH>7
丁
0.1
0.1
pH=10
(1)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是________。
(2)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=________ mol/L。
(3)某二元酸(分子式用H2B表示)在水中的电离方程式是:
H2B===H++HB- HB-H++B2-
在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)=0.1 mol/L B.c(B2-)+c(HB-)+c(H2B)=0.1 mol/L
C.c(OH-)=c(H+)+c(HB-) D.c(Na+)+c(OH-)=c(H+)+c(HB-)
【答案】 (1). C3H8O (2). CH3CH2—O—CH2CH3 (3). 醚 (4). c(Na+)>c(A-)>c(OH-)>c(H+) (5). 10-4-10-10 (6). A、C
【解析】
【分析】
Ⅰ.氧气的质量 = ×32 g/mol = 6.4 g,根据质量守恒确定一氧化碳的物质的量,再结合原子守恒确定C、H、O三种原子的物质的量之比;根据有机物中分子中C、H、O原子个数比确定该有机物中碳原子是否达到饱和状态来判断其分子式;
Ⅱ.该有机物的相对原子质量为74,红外光谱图显示存在对称的甲基、对称的亚甲基和醚键可得分子结构;
Ⅲ. (1)混合溶液的溶质为等物质的量的HA和NaA,pH>7则说明A-的水解大于HA的电离,结合电荷守恒判断;
(2)由电荷守恒关系式变形得c(Na+)-c(A-)=c(OH-)-c(H+);
(3)根据二元酸的电离方程式H2B═H++HB-,HB-⇌H++B2-可知,B2-只发生第一步水解,结合电荷守恒和物料守恒分析解答。
【详解】Ⅰ. 氧气的质量= ×32 g/mol = 6.4 g,浓硫酸吸收的是水,水的物质的量= = 0.2 mol,碱石灰吸收的是二氧化碳,二氧化碳的物质的量 = = 0.1 mol,根据质量守恒知,一氧化碳的物质的量 = = 0.05 mol,
根据原子守恒得n(H) = 2n(H2O) = 0.4 mol,n(C) = n(CO2) + n(CO) = (0.1+0.05) mol = 0.15 mol,
则3 g A中,n(H) = 0.4 mol,n(C) = 0.15 mol,
n(O) = 2n(CO2) + n(CO) + n(H2O) − 2n(O2) = 2×0.1 mol + 0.05 mol + 0.2 mol − 2×0.2 mol = 0.05mol
则该有机物的分子中,C、H、O原子的物质的量之比n(C):n(H):n(O) = 0.15 mol :0.4 mol :0.05mol = 3:8:1,
又氢原子已使碳达饱和,所以该有机物的分子式为C3H8O,
故答案为:C3H8O;
Ⅱ. 该有机物的相对原子质量为74,红外光谱图显示存在对称的甲基、对称的亚甲基和醚键,可得该分子的结构简式为:CH3CH2OCH2CH3,按照官能团分类,该物质属于醚,
故答案为:CH3CH2OCH2CH3;醚;
Ⅲ. (1)混合溶液的溶质为等物质的量的HA和NaA,混合溶液的pH>7,说明A−的水解大于HA的电离,所以其离子浓度由大到小的顺序为c(Na+)>c(A-)>c(OH-)>c(H+),
故答案为:c(Na+)>c(A-)>c(OH-)>c(H+);
(2)由电荷守恒关系式可知,c(Na+) + c(H+) = c(OH−) + c(A−),变形得c(Na+) −c(A−) = c(OH−)−c(H+) = (10−4−10−10) mol⋅L−1,
故答案为:10−4−10−10·;
(3)在Na2B中存在水解平衡:B2−+H2O⇌HB−+OH−,HB−不会进一步水解,
A. 由物料守恒得:c(B2−)+c(HB−) = 0.1 mol⋅L−1,故A项正确;
B. HB−不会进一步水解,所以溶液中没有H2B分子,故B项错误;
C. 根据溶液中质子守恒得:c(OH−)=c(H+)+c(HB−),故C项正确;
D. 溶液中电荷守恒为:c(Na+)+c(H+)=c(OH−)+c(HB−)+2c(B2−),故D项错误;
故答案为:A、C。
【点睛】Ⅲ.(3)是本题的难点,学生准确读取题设信息是解题的关键,根据溶液的三大守恒进行解题是基础。其中C选项的质子守恒规律可借助电荷守恒与物料守恒关系式间接求出。