- 147.00 KB
- 2021-07-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
湖南省长沙市长沙县2019-2020学年高一下学期6月联考试卷
可能用到的相对原子质量:H-1C-12N-14O-16Na-23Al-27 S-32Cl-35.5Fe-56
一、单项选择题:(每题只有1个选项符合要求,本部分22题,每题2分,共44分)。
1. 在科学史上每一次重大的发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于( )
A. 提出了元素周期律 B. 开发了合成氨的生产工艺
C. 揭示了燃烧的本质 D. 提取了治疟药物青蒿素
2I可用于治疗甲状腺疾病。该原子的质子数是( )
A. 53 B. 78 C. 131 D. 184
3.下列化学用语表示正确的是( )
A. 乙酸的结构简式:C2H4O2 B. N2的电子式:N ::: N
C. S2-的结构示意图: D. KCl的电离方程式:KCl = K++ Cl-
4.下列选项描述的过程能实现化学能转化为热能的是( )
A. 光合作用 B. 烧炭取暖 C. 风力发电 D. 电解冶炼
5.下列物质属于共价化合物的是( )
A. H2O B. MgO C. CaCl2 D. KBr
6. 下列物质不属于高分子化合物的是( )
A. 蛋白质 B. 聚乙烯 C. 油脂 D. 淀粉
7.将等质量的下列各烃,完全燃烧生成CO2和H2O,耗氧量最大的是( )
A. CH4 B. C2H4 C. C6H6 D. C3H6
8 .已知一定温度时:2SO2(g)+O2(g)2SO3(g),当生成2mol SO3时,放出热量197kJ,在相同温度和压强下,向密闭容器中通入2mol SO2和1molO2,达到平衡时放出热量Q,则下列关系式中正确的是( )
A. Q=197 kJ B. Q<197×2 kJ C. Q<197 kJ D. Q>197 kJ
9. 近日,我国渤海探明超千亿立方的天然气田。天然气的主要成分为( )
A. H2 B. CH4 C. CO2 D. NH3
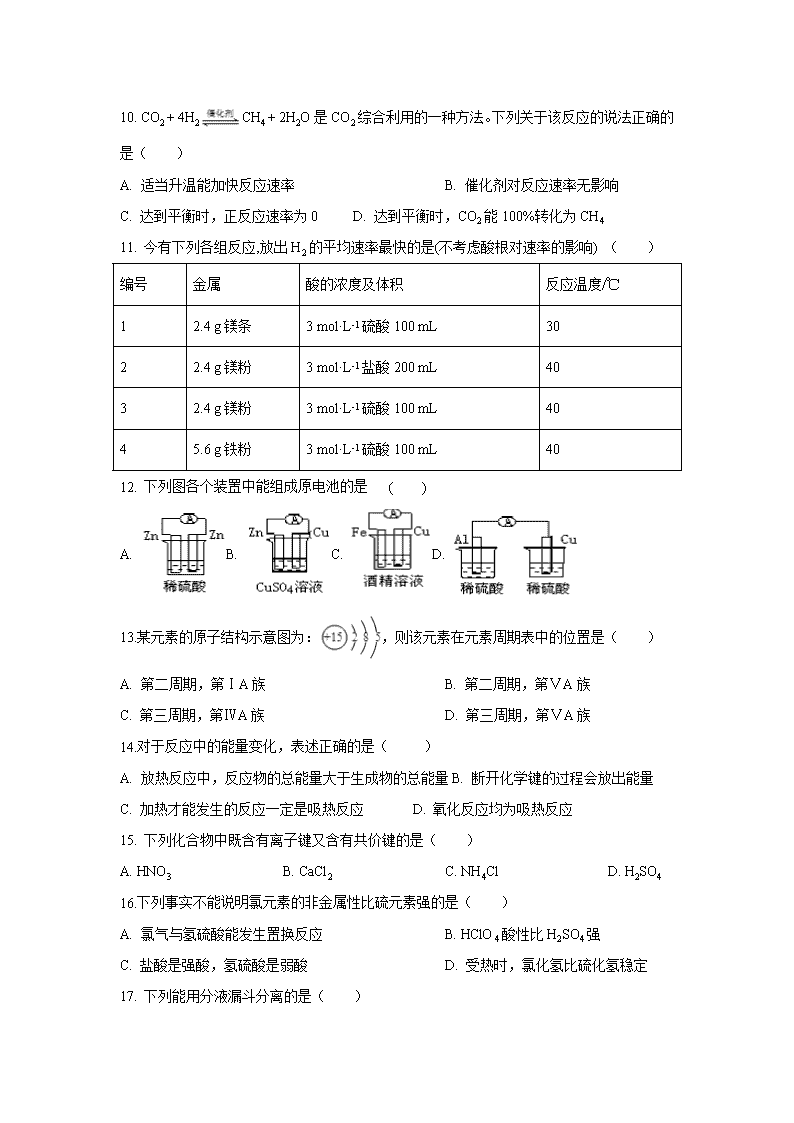
10. CO2 + 4H2CH4 + 2H2O是CO2综合利用的一种方法。下列关于该反应的说法正确的是( )
A. 适当升温能加快反应速率 B. 催化剂对反应速率无影响
C. 达到平衡时,正反应速率为0 D. 达到平衡时,CO2能100%转化为CH4
11. 今有下列各组反应,放出H2的平均速率最快的是(不考虑酸根对速率的影响) ( )
编号
金属
酸的浓度及体积
反应温度/℃
1
2.4 g镁条
3 mol·L-1硫酸100 mL
30
2
2.4 g镁粉
3 mol·L-1盐酸200 mL
40
3
2.4 g镁粉
3 mol·L-1硫酸100 mL
40
4
5.6 g铁粉
3 mol·L-1硫酸100 mL
40
12. 下列图各个装置中能组成原电池的是 ( )
A. B. C. D.
13.某元素的原子结构示意图为:,则该元素在元素周期表中的位置是( )
A. 第二周期,第ⅠA族 B. 第二周期,第ⅤA族
C. 第三周期,第ⅣA族 D. 第三周期,第ⅤA族
14.对于反应中的能量变化,表述正确的是( )
A. 放热反应中,反应物的总能量大于生成物的总能量B. 断开化学键的过程会放出能量
C. 加热才能发生的反应一定是吸热反应 D. 氧化反应均为吸热反应
15. 下列化合物中既含有离子键又含有共价键的是( )
A. HNO3 B. CaCl2 C. NH4Cl D. H2SO4
16.下列事实不能说明氯元素的非金属性比硫元素强的是( )
A. 氯气与氢硫酸能发生置换反应 B. HClO4酸性比H2SO4强
C. 盐酸是强酸,氢硫酸是弱酸 D. 受热时,氯化氢比硫化氢稳定
17. 下列能用分液漏斗分离的是( )
A. 植物油和乙醇 B. 乙酸乙酯和水 C. 乙酸和乙醇 D. 汽油和煤油
18. 下列关于淀粉的说法正确的是( )
A. 化学式为C6H12O6 B. 不属于糖类
C. 不能发生水解反应 D. 常温下其水溶液遇碘变蓝
19. 有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为:( )
A. A>B>C>D B. A>C>D>B C. C>A>B>D D. B>D>C>A
20.一定温度下,反应N2(g)+3H2(g) 2NH3(g)达到化学平衡状态的标志是( )
A. N2、H2和NH3的质量分数不再改变
B. c(N2)∶c(H2)∶c(NH3)=1∶3∶2
C. 断裂1 mol N≡N键的同时,形成6 mol N—H键
D. N2与H2的物质的量之和是NH3的物质的量的2倍
21. 下列物质互为同分异构体的一组是( )
A. 35Cl和37Cl B. CH3CH2OH和CH3OCH3 C. O2和O3 D. H2O和H2O2
22.下列有机反应属于加成反应的是( )
A. C3H8 + 5O2 3CO2 + 4H2O
B. CH2 = CH2 + Br2 →
C. 2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
D. + HNO3 + H2O
二、非选择题(本部分3题,除特别注明外2分/空 共56分)。
23(18分).如图是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题。(除特别注明外,其他一律用化学式表示)
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为____________。
(2)元素E的最高价氧化物的电子式是________________。
(3)某元素二价阳离子的核外有10个电子,该元素是____________ (填元素名称)。
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序: _________________。
(5)H、J、K的最高价氧化物的水化物的酸性由强到弱的顺序: ______________。
(6)元素B的最高氧化物的水化物的电子式是______________,化合物类型为________________(填“离子化合物”或“共价化合物”)。
(7)元素I的氢化物的结构式为____________;该氢化物常温下和元素K的单质反应的化学方程式为_____________________。
24. (12分)I:已知:反应aA(g)+bB(g)cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
(1)经测定前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式_______________________
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1; 乙:v(B)=0.12 mol·L-1·s-1; 丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为__________________(用甲、乙、丙表示)。
Ⅱ: 某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
时间/min
1
2
3
4
5
6
氢气体积/mL
50
120
224
392
472
502
(3)哪一时间段反应速率最大 __(填0~1、1~2、2~3、3~4、4~5、5~6 min,下同),原因是___________________________________________
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是__________(填字母)
A.CH3COONa B.NaNO3溶液C.KCl溶液 D.Na2CO3溶液
Ⅲ:(5)下列说法可以证明H2(g)+I2(g)2HI(g)已达平衡状态的是_________
A.单位时间内生成n mol H2的同时,生成n mol HI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=v(HI)
E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化
25. (16分) (1)烃是一类重要的有机化合物,其结构与性质密切相关。
①下列有机化合物与甲烷互为同系物的是______(填字母) (1分)。
a.乙烯 b.乙烷 c.乙炔
②下列试剂可用于鉴别乙烷和乙烯的是______(填字母) (1分)。
a.水 b.四氯化碳 c.酸性KMnO4溶液
③下列有机化合物易溶于水的是________(1分)。
a..苯 b.乙烷 c.乙醇
(2) CH2=CH2、、CH3CH2OH、CH3COOCH2CH3、CH3COOH、葡萄糖,其中:
①能通过化学反应使溴水褪色的是____________(1分)。
②能发生水解反应的是____________(1分)。
③能与新制Cu(OH)2悬浊液反应生成砖红色沉淀的是____________(1分)。
(3)以淀粉为主要原料合成一种具有果香味的物质C合成路线如图所示。
请回答下列问题:
①A的结构简式为____________,②B分子中的官能团名称为________。
③反应⑤方程式___________________________;
(4)乙烯是石油化工的重要基础原料,工业上可由乙烯与水反应制乙醇,该反应类型为_______,其化学方程式为___________________。
【参考答案】
一、单项选择题:(每题只有1个选项符合要求,本部分22题,每题2分,共44分)。
题序
1
2
3
4
5
6
7
8
9
10
11
答案
A
A
D
B
A
C
A
C
B
A
C
题序
12
13
14
15
16
17
18
19
20
21
22
答案
B
D
A
C
C
B
D
B
A
B
B
二、非选择题(本部分3题,除特别注明外2分/空 共56分)。
23(18分) (2). (3). 镁 (4). H2O>NH3>PH3
(5). HClO4>H2SO4>H3PO4 (6). . 离子化合物
(7). H-O-H . Cl2+H2O=HCl+HClO
24. (12分)
I: (1). 3A(g)+B(g) 2C(g) (2). 乙>甲>丙
Ⅱ: (3). 3~4min 因该反应是放热反应,此时温度高,温度对反应速率占主导作用 (4). AC
Ⅲ: (5). BC
25. (16分)
(1). ①b (1分) ② c (1分) ③. c (1分)
(2)..①CH2=CH2 (1分) ②CH3COOCH2CH3 (1分) ③ 葡萄糖(1分) (1分)
(3) ①CH3CHO ② 羧基 ③. CH3COOH+C2H5OH CH3COOC2H5+H2O
(4). 加成反应 CH2=CH2+H2OCH3CH2OH