- 301.00 KB
- 2021-07-03 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
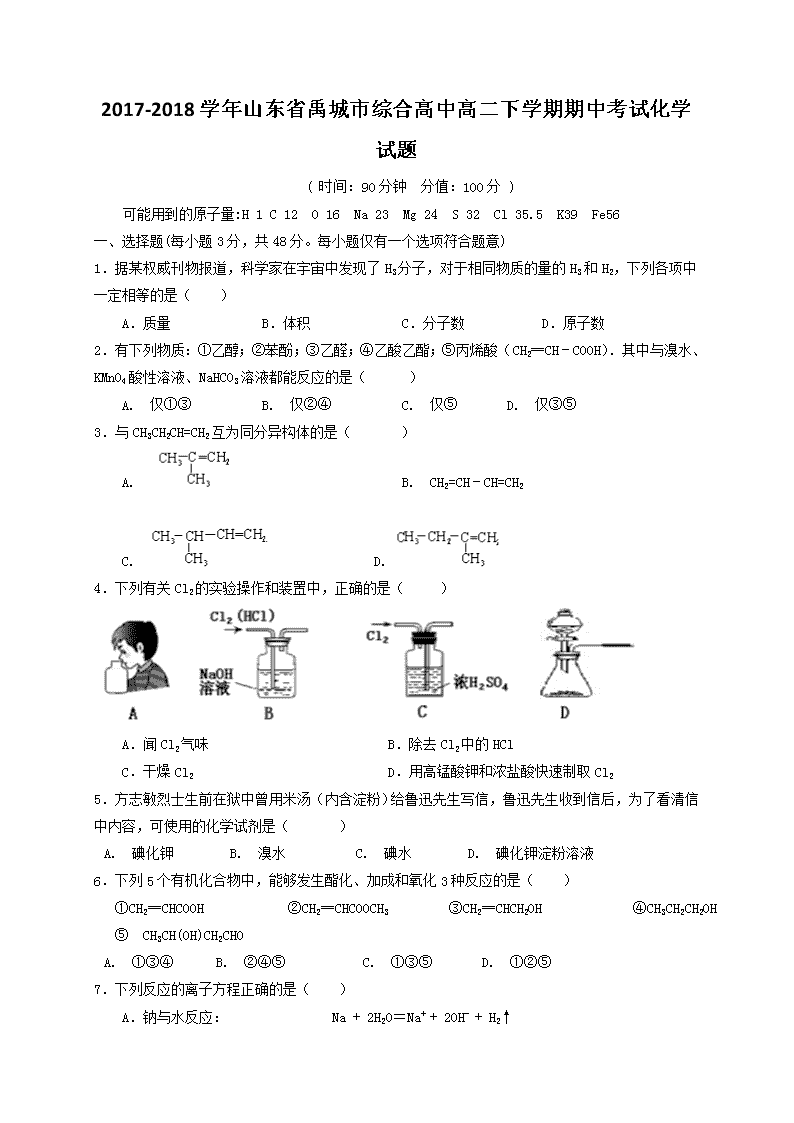
2017-2018学年山东省禹城市综合高中高二下学期期中考试化学试题
( 时间:90分钟 分值:100分 )
可能用到的原子量:H 1 C 12 O 16 Na 23 Mg 24 S 32 Cl 35.5 K39 Fe56
一、选择题(每小题3分,共48分。每小题仅有一个选项符合题意)
1.据某权威刊物报道,科学家在宇宙中发现了H3分子,对于相同物质的量的H3和H2,下列各项中一定相等的是( )
A.质量 B.体积 C.分子数 D.原子数
2.有下列物质:①乙醇;②苯酚;③乙醛;④乙酸乙酯;⑤丙烯酸(CH2═CH﹣COOH).其中与溴水、KMnO4酸性溶液、NaHCO3溶液都能反应的是( )
A. 仅①③ B. 仅②④ C. 仅⑤ D. 仅③⑤
3.与CH3CH2CH=CH2互为同分异构体的是( )
A. B. CH2=CH﹣CH=CH2
C. D.
4.下列有关Cl2的实验操作和装置中,正确的是( )
A.闻Cl2气味 B.除去Cl2中的HCl
C.干燥Cl2 D.用高锰酸钾和浓盐酸快速制取Cl2
5.方志敏烈士生前在狱中曾用米汤(内含淀粉)给鲁迅先生写信,鲁迅先生收到信后,为了看清信中内容,可使用的化学试剂是( )
A. 碘化钾 B. 溴水 C. 碘水 D. 碘化钾淀粉溶液
6.下列5个有机化合物中,能够发生酯化、加成和氧化3种反应的是( )
①CH2═CHCOOH ②CH2═CHCOOCH3 ③CH2═CHCH2OH ④CH3CH2CH2OH ⑤ CH3CH(OH)CH2CHO
A. ①③④ B. ②④⑤ C. ①③⑤ D. ①②⑤
7.下列反应的离子方程正确的是( )
A.钠与水反应: Na + 2H2O=Na+ + 2OH- + H2↑
B.FeCl3溶液中加入足量的氨水:Fe 3++ 3OH-= Fe (OH)3↓
C.钠与CuSO4溶液反应: 2Na+Cu2+=Cu +2Na+
D.用小苏打治疗胃酸过多病: HCO3-+H+=CO2↑+H2O
8.下列说法正确的是( )
A.苯中含有的苯酚杂质可通过加入足量溴水后过滤的方法而除去
B.苯乙烯中至少有8个碳原子在同一个平面
C.等质量的乙烯和聚乙烯完全燃烧,产生的二氧化碳的质量之比为1:1
D.分子式为C5H10O2且可与氢氧化钠溶液反应的有机化合物有14种
9.根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是( )
I2+SO2+2H2O=H2SO4+2HI 2FeCl2+Cl2=2FeCl3 2FeCl3+2HI=2FeCl2+2HCl+I2
A.I一>Fe2+>C1一>SO2 B.C1一> Fe2+> SO2> I一
C.Fe2+>I一> C1一>SO2 D.SO2>I一>Fe2+> C1一
10.下列关于有机物的说法中正确的是( )
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③有机物完全燃烧后都只能生成二氧化碳和水
④除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
⑤塑料、橡胶和光导纤维都是合成高分子材料
⑥石油的分馏、裂化和煤的干馏都是化学变化.
A. ①⑤⑥ B. ②④ C. ①②③⑤ D. ③④⑤⑥[]
11. 某有机物的化学式为C5H10O,它能发生银镜反应和加成反应.若将它与H2加成,所得产物结构式可能是( )
A.(CH3)3COH B.(CH3CH2)2CHOH
C.CH3(CH2)3CH2OH D.CH3CH2C(CH3)2OH
12.用NA代表阿伏加德罗常数,下列说法正确的是( )
A.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
B.标准状况下,11.2 L H2O 所含的分子数为0.5NA
C.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA
D.18g H2O 和H2O2 的混合物含有的分子数为1NA
13.化学实验室中常将溶液或试剂进行酸化,下列酸化处理正确的是( )
A.检验氯乙烷中的氯元素,加碱溶液加热后,用稀硫酸酸化后,再检验
B.鉴别溶液中是否有SO42﹣,用盐酸酸化
C.为抑制Fe2+的水解,用稀硝酸酸化
D.为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化
14.下列说法错误的是( )
A.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸
B.在KI-淀粉溶液中通入氯气,溶液变蓝,是因为生成的单质碘与淀粉发生显色反应
C.在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中一定含SO
D.实验室可用氯化铵与氢氧化钙加热制取氨气
15.24mL浓度为0.05mol·L-1 Na2SO3 溶液恰好与20mL 浓度为0.02mol·L-1 的K2X2O7 溶液完全反应,已知Na2SO3 可被K2X2O7 氧化为Na2SO4 ,则元素X 在还原产物中的化合价为( )
A. +2 价 B. +3 价 C. +4价 D. +5价
16.天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
A.分子中有三个苯环 B. 可溶于有机溶剂
C.1mol维生素P可以和6molBr2反应
D.1mol维生素P可以和4molNaOH反应
二.非选择题(共52分)
17. (2分)下列说法正确的是________
①残留在试管内壁上的碘,用热水洗涤
②盛放过苯酚的试剂瓶中残留的苯酚,用酒精洗涤
③做银镜反应后试管壁上银镜,用稀氨水洗涤
④沾附在试管内壁上的油脂,用热碱液洗涤
⑤天然纤维、合成纤维和人造纤维统称化学纤维
⑥用油脂在酸性条件下水解,可以生产甘油和肥皂
⑦淀粉与纤维素分子式都为(C6H10O5)n而结构不同,所以它们互为同分异构体
⑧将乙炔通入酸性高锰酸钾溶液中,溶液褪色属于加成反应.
18.(10分)某有机物A的相对分子质量为62.为进一步测定A 的化学式,现取3.1g A完全燃烧,得到二氧化碳和水蒸气.将产物先后通过足量的浓硫酸和碱石灰,两者分别增重2.7g和4.4g(假设每步反应完全).
(1)该有机物的实验式是________;分子式是________.
(2)红外光谱显示有“C﹣C”键和“O﹣H”键的振动吸收,若核磁共振氢谱只有2个吸收峰且峰面积之比为1:2,推断该有机物的结构简式是________,官能团的名称为________.
(3)该有机物与金属钠反应的化学方程式是____________________________。
19.(16分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,
还可制备硫及铁的化合物。冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2。
(1)若CuFeS2中Fe的化合价为+2,反应中被还原的元素是__________(填元素符号)。
(2)用稀H2SO4浸泡上述反应制取铜后剩余的固体残渣,取少量所得溶液,检验溶液中存在Fe3+的方法是 (注明试剂、现象)。
(3)上述冶炼过程产生大量SO2。下列处理方案中合理的是 (填代号)
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(4)验证黄铜矿冶炼铜的反应后气体中含有SO2的方法是
(5)实验室制备,收集干燥的SO2,所需仪器如下。
①其中装置A产生SO2 ,反应的化学方程式为 。
②请按气流方向连接各仪器接口,顺序为a → → → → → f ,装置D的作用是 。装置E中NaOH溶液的作用是 。
20.(10分)现通过以下步骤由 制备
(1)写出B的结构简式: ___________,写出④步的反应类型为 _____________。
(2)写出反应A→B所需的试剂和条件:___________________
(3)写出④和⑤的化学方程式______________________________,______________________________
21.(14分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
已知:RX ROH;
RCHO+CH3COOR′ RCH=CHCOOR′
请回答:
(1)乙烯的电子式为______ ,E中官能团的结构简式为________.
(2)B+D→F的化学方程式______________________________,反应类型是_______
(3)X的结构简式_______________.
(4)对于化合物X,下列说法正确的是 .
A. 能发生水解反应 B. 不与浓硝酸发生取代反应
C. 能使Br2/CCl4溶液褪色 D. 能发生银镜反应.
(5) 与D互为同分异构体的芳香族化合物有_______种
高二期中考试化学答案
1-5 CCADC 6-10 CDCDB 11-15 CABCB 16 A
17. (2分) ②④
18. (10分,每空2分)(1) CH3O; C2H6O2
(2)HOCH2CH2OH 羟基 (3)HOCH2CH2OH+2Na→NaOCH2CH2ONa+H2↑
19. (16分,每空2分) (1)Cu、O
(2)取少量溶液,滴加KSCN溶液,溶液变红,证明存在Fe3+。
(3)bc
(4)将气体通入品红溶液中,如果品红溶液褪色,加热后又变红,则证明有SO2。
(5)①Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
②d e c b; 安全瓶,防止倒吸; 吸收多余的SO2,防止污染空气。
20. (10分,每空2分)(1) 消去反应
(2)NaOH的醇溶液,加热
(3)+2NaOH+2NaCl+2H2O
21.(14分,每空2分)
(1) -CHO
(2)CH3COOH+ +H2O 酯化(取代)反应
(3)
(4)AC
(5)4