- 2.03 MB
- 2021-07-03 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
孝感市八所重点高中教学协作体
2016—2017学年联合考试
高二化学试卷
命题学校:大悟一中
考试时间:2017年6月30日 上午8:00—9:30 试卷满分:100分
可能用到相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 Mg 24 Si 28 P 31 S 32 Cl 35.5 K 39 Fe 56 Cu 64
第Ⅰ卷 选择题(48分)
一、选择题(本题包括16小题,每小题3分,共48分。每小题只有一个选项符合题意)
1.下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.放热反应在常温下一定很容易发生
C.判断反应是放热还是吸热必须看反应物和生成物具有的总能量的相对大小
D.已知石墨(s)比金刚石(s)稳定,则石墨(s)转化为金刚石(s)要放出能量
2.下列说法正确的是( )
A.食用白糖的主要成分是蔗糖 B.淀粉、纤维素和油脂都是属于天然高分子化合物
C.植物油的主要成分是高级脂肪酸 D.蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖
3.下列各组中的反应,属于同一反应类型的是( )
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C.由氯代环已烷制环已烯;由丙烯制1,2二溴丙烷
D.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
4.下列八种物质中,既能使酸性高锰酸钾溶液褪色又能因反应使溴的四氯化碳溶液褪色的是( )
①甲烷 ②苯 ③聚乙烯 ④聚异戊二烯 ⑤2-丁炔 ⑥环己烷 ⑦邻二甲苯 ⑧环己烯
A.②③④⑤⑥ B.①④⑤⑦⑧ C.④⑤⑧ D.③④⑤⑦⑧
5.分子式为C7H14O2的有机物Q在稀硫酸溶液中加热可转化为乙醇与另一种酸性物质,则Q的结构最多有( )
A.6种 B.4种 C.3种 D.2种
6.发射“神六”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ·mol-1 ②N2H4(g)+O2(g)= N2(g) +2H2O(g) △H=-534kJ·mol-1下列关于肼和NO2反应的热化学方程式中,正确的是( )
A.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l) △H= -1135.7kJ·mol-1
B.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H= -1000.3kJ·mol-1
C.N2H4(g)+NO2(g)= N2(g)+2H2O(l) △H= -500.15kJ·mol-1
△
D.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H= -1135.7kJ·mol-1
7.一定温度下,可逆反应2NO2(g) 2NO(g)+O2(g)在容积固定的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2,同时生成2n molNO2
②单位时间内生成n molO2,同时生成2n molNO
③用NO2、NO、O2的物质的量浓度变化的反应速率之比为2:2:1
④混合气体的压强不再改变
⑤混合气体的颜色不再改变
⑥混合气体的平均相对分子质量不再改变
A.①④⑤⑥ B.①②③⑤ C.②③④⑥ D.以上全部
8.锌-空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,
反应为2Zn+O2+4OH-+2H2O=2Zn(OH)42-。下列说法正确的是( )
A.充电时,电解质溶液中K+向阳极移动
B.充电时,电解质溶液中c(OH-)逐渐减小
C.放电时,负极反应为Zn+4OH—2e- =Zn(OH)42-
D.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
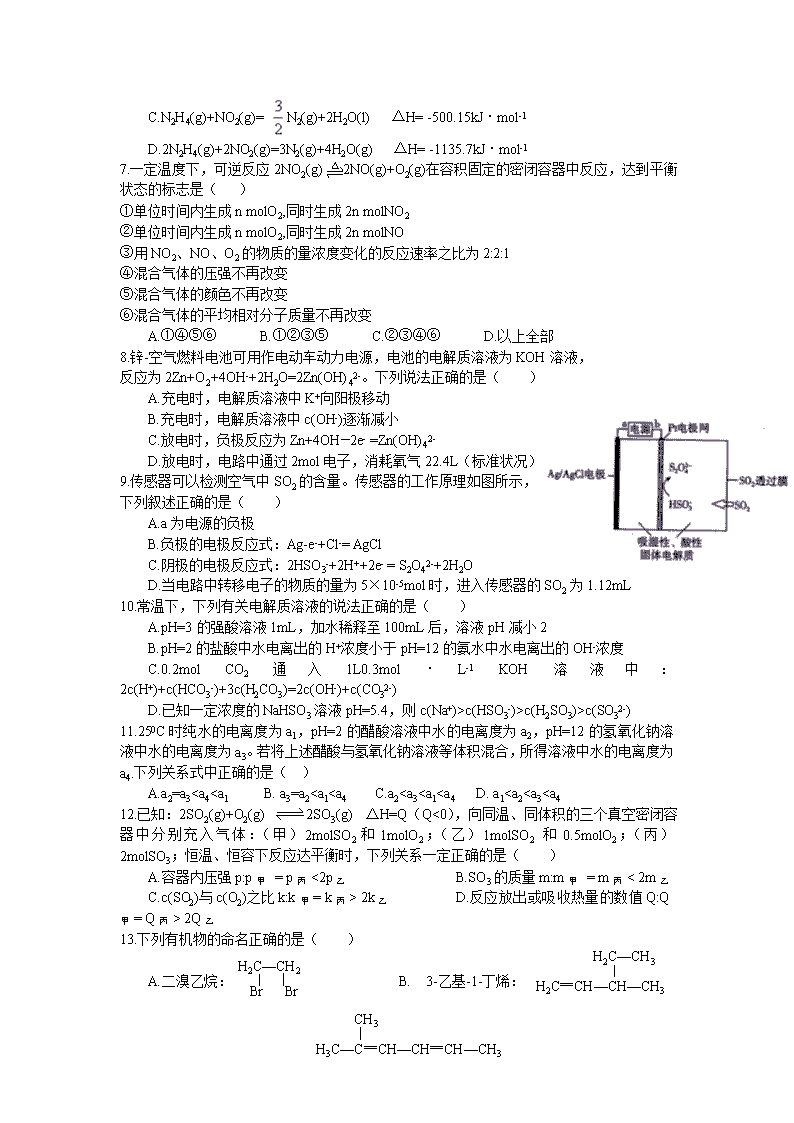
9.传感器可以检测空气中SO2的含量。传感器的工作原理如图所示,
下列叙述正确的是( )
A.a为电源的负极
B.负极的电极反应式:Ag-e-+Cl-= AgCl
C.阴极的电极反应式:2HSO3-+2H++2e- = S2O42-+2H2O
D.当电路中转移电子的物质的量为5×10-5mol时,进入传感器的SO2为1.12mL
10.常温下,下列有关电解质溶液的说法正确的是( )
A.pH=3的强酸溶液1mL,加水稀释至100mL后,溶液pH减小2
B.pH=2的盐酸中水电离出的H+浓度小于pH=12的氨水中水电离出的OH-浓度
C.0.2mol CO2通入1L0.3mol·L-1 KOH溶液中:2c(H+)+c(HCO3-)+3c(H2CO3)=2c(OH-)+c(CO32-)
D.已知一定浓度的NaHSO3溶液pH=5.4,则c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-)
11.250C时纯水的电离度为a1,pH=2的醋酸溶液中水的电离度为a2,pH=12的氢氧化钠溶液中水的电离度为a3。若将上述醋酸与氢氧化钠溶液等体积混合,所得溶液中水的电离度为a4.下列关系式中正确的是( )
A.a2=a3 2k乙 D.反应放出或吸收热量的数值Q:Q甲 = Q丙 > 2Q乙
H2C═CH—CH—CH3
H2C—CH3
13.下列有机物的命名正确的是( )
H2C—CH2
Br Br
A.二溴乙烷: B. 3-乙基-1-丁烯:
H3C—C═CH—CH═CH—CH3
CH3
C.2-甲基-2,4-已二烯:
H3C—C—CH2—CH—CH3
CH3
CH3
CH3
D.2,2,3-三甲基戊烷:
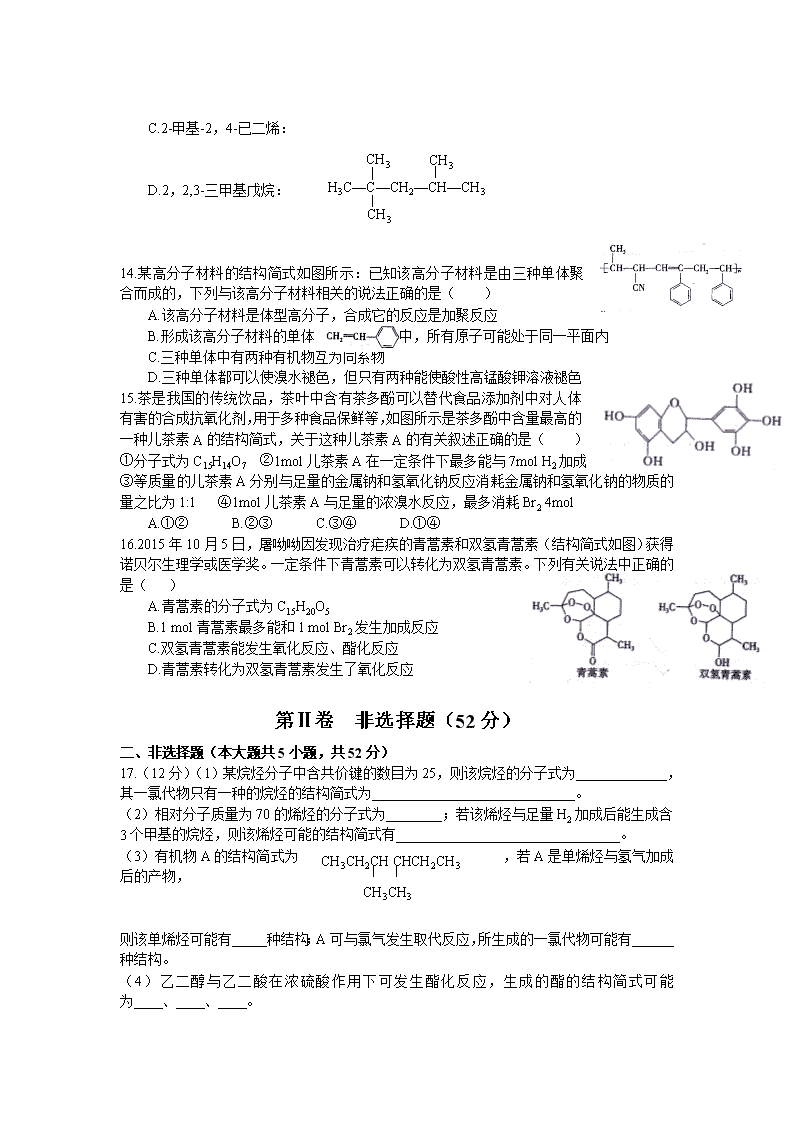
14.某高分子材料的结构简式如图所示:已知该高分子材料是由三种单体聚合而成的,下列与该高分子材料相关的说法正确的是( )
A.该高分子材料是体型高分子,合成它的反应是加聚反应
B.形成该高分子材料的单体 中,所有原子可能处于同一平面内
C.三种单体中有两种有机物互为同系物
D.三种单体都可以使溴水褪色,但只有两种能使酸性高锰酸钾溶液褪色
15.茶是我国的传统饮品,茶叶中含有茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )
①分子式为C15H14O7 ②1mol儿茶素A在一定条件下最多能与7mol H2加成 ③等质量的儿茶素A分别与足量的金属钠和氢氧化钠反应消耗金属钠和氢氧化钠的物质的量之比为1:1 ④1mol儿茶素A与足量的浓溴水反应,最多消耗Br2 4mol
A.①② B.②③ C.③④ D.①④
16.2015年10月5日,屠呦呦因发现治疗疟疾的青蒿素和双氢青蒿素(结构简式如图)获得诺贝尔生理学或医学奖。一定条件下青蒿素可以转化为双氢青蒿素。下列有关说法中正确的是( )
A.青蒿素的分子式为C15H20O5
B.1 mol青蒿素最多能和1 mol Br2发生加成反应
C.双氢青蒿素能发生氧化反应、酯化反应
D.青蒿素转化为双氢青蒿素发生了氧化反应
第Ⅱ卷 非选择题(52分)
二、非选择题(本大题共5小题,共52分)
17.(12分)(1)某烷烃分子中含共价键的数目为25,则该烷烃的分子式为_____________,其一氯代物只有一种的烷烃的结构简式为_____________________________。
(2)相对分子质量为70的烯烃的分子式为________;若该烯烃与足量H2加成后能生成含3个甲基的烷烃,则该烯烃可能的结构简式有________________________________。
CH3CH2CH CHCH2CH3
CH3CH3
(3)有机物A的结构简式为 ,若A是单烯烃与氢气加成后的产物,
则该单烯烃可能有_____种结构;A可与氯气发生取代反应,所生成的一氯代物可能有______种结构。
(4)乙二醇与乙二酸在浓硫酸作用下可发生酯化反应,生成的酯的结构简式可能为 、 、 。
18.(8分)工业上一般在恒容密闭容器中采用下列反应合成甲醇:
CO(g)+2H2(g) CH3OH(g) △H
(1)下表所列数据是反应在不同温度下的化学平衡常数(K)
温度/0C
270
300
350
K
2.041
0.270
0.012
①由表中数据判断该反应的△H_______0(填“>”“=”或“<”)
②某温度下,将2 molCO和6 mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol·L-1,则CO的转化率为___________,此时的温度为___________。
(2)要提高CO的转化率,可以采取的措施是____________(填序号)。
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2加压
e.加入惰性气体加压 f.分离出甲醇
(3)3000C时,在2L的密闭容器中充入2 mol CO,2mol CH3OH,6mol H2,则此时正__逆(填“>”“<”“=” )
(4)寻找合适的催化剂来改善上述合成甲醇的条件一直是研究课题的重点。现分别对X、Y、Z三种催化剂进行如下实验(其他条件均相同):
①X在T10C时催化效率最高,能使正反应速率加快约3×105倍;
②Y在T20C时催化效率最高,能使正反应速率加快约3×105倍;
③Z在T30C时催化效率最高,能使正反应速率加快约3×106倍;
已知:T1>T2>T3,根据上述信息,写出你认为在生产中应该选择的适宜催化剂并简述理由:_______________。
19.(12分)已知甲酸(HCOOH)是最简单的羧酸,它具有羧酸的性质,在实验室里常用甲酸在浓硫酸的作用下制取少量一氧化碳。现用甲酸与甲醇反应制取甲酸甲酯来验证甲酸能发生酯化反应,装置如下图所示。回答下列问题:
(1)实验过程中选用试剂及用品有浓硫酸、甲醇、甲酸,还有____________、___________两种物质。
(2)大试管中溶液的作用有溶解甲醇、吸收甲酸,还有_____________。
(3)若大试管中溶液是NaOH溶液,则收集到的产物比预期的少,其原因是______
(4)生成甲酸甲酯的反应的化学方程式为__________。
(5)在实验过程中导管b___(填“能”或“不能”)直接与大气相通,理由为______。
20.(8分)(1)990C时,Kw=1.0×10-12mol2·L-2,该温度下测得0.1 mol·L-1 Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为______________________.
②该温度下,将0.01 mol· L-1 H2A溶液稀释到20倍后,溶液的pH=________。
③体积相等、pH均为1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气______(填字母)
A.盐酸多 B.H2A多 C.一样多 D.无法确定
电解
(2)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O CH3CH2OH +CH3COOH实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入_______(填化学式),电极反应式为_______。
②在实际工艺处理中,阴极区乙醛的去除率可达80%。若在两极区分别注入1m3
乙醛含量为3000mg·L-1的废水,可得到乙醇_____kg(计算结果保留小数点后1位)
21.(12分)有机物A是制造新型信息材料的中间体,B是制备血管紧张素抑制剂卡托普利的原料,它们有如图所示的转化关系:
试回答下列问题:
(1)B的名称是_________________________,C含氧的官能团名称是___________________。
(2)F→D的化学方程式为__________,C→E的反应类型是______________。
(3)E的结构简式为________________________________________。
(4)写出与F具有相同官能团的F的所有同分异构体:CH3CHCH2COOH、CH3CH2CHCOOH _____、______。
Cl Cl
高二化学试卷参考答案
题号
1
2
3
4
5
6
7
8
选项
C
A
D
C
B
D
A
C
题号
9
10
11
12
13
14
15
16
选项
C
C
A
A
C
B
D
C
(CH3)3CC(CH3)3
CH2=C CH2CH3
CH3
CH3
CH3C= CH CH3
CH3
C8H18
17.(12分)(1) (1分) (2分)
C5H10
CH3 CHCH=CH2
(2) (各1分)
(3) (各1分) 4 4
COOCH2
COOCH2
HOOCCOOCH2CH2OH
(4) (1分) (1分)
HO [ OCCOOCH2CH2O ] nH (1分)
18.(8分)(1) ① < (1分) ② 80% (2分) 270℃ (1分)
(2) df (1分) (3) > (2分)
(4)选Z,温度要求低,反应速率快。(1分)
19.(12分)(1)饱和Na2CO3溶液 (1分) 碎瓷片(1分)
(2)降低酯的溶解度,有利于酯析出(2分)
(3)甲酸甲酯在碱性条件下水解了一部分(2分)
(4)HCOOH+CH3OH
△
浓硫酸
HCOOCH3+H2O(2分)
(5)不能(2分) CO和CH3OH都是有毒物质,对环境有污染(2分)
20.(8分)(1) ① H2A=2H+ + A2- ② 3 ③ C (各1分)
(2) ① CH4 (1分) CH4+10OH- - 8e- = (2分)
② 2.5 (2分)
CH3-CH-COOH + 2NaOH
CH2-Cl
CH2=C—COONa + NaCl+ 2H2O
CH3
21.(12分)(1) 2-甲基丙烯酸 (1分) 羟基 (1分)
(2)
(2分)
取代反应 (1分)
C COOH
Cl
CH3
CH3
(3)HOCH2CHCH2OH (3分)
CH3
(4) ClCH2CH2CH2COOH (各2分)