- 303.84 KB
- 2021-07-05 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
化学反应速率
一、选择题(本题共9小题,每小题7分,共63分。每小题只有一个选项符合题目要求)
1.下列有关化学反应速率的判断正确的是( )
A.块状大理石、粉末状大理石分别与0.1 mol·L-1的盐酸反应的速率相同
B.物质的量浓度相同的稀盐酸和稀硝酸分别与大小相同的大理石反应的速率相同
C.镁粉和铁粉分别与物质的量浓度相同的稀盐酸反应的速率相同
D.物质的量浓度相同的稀盐酸和稀醋酸分别与2 mol·L-1的NaOH溶液反应的速率相同
2.(2018海南华侨中学月考)在一密闭容器中充入一定量的N2和O2,在电火花作用下发生反应N2+O22NO,经测定前3 s用N2表示的反应速率为0.1 mol·L-1·s-1,则6s末NO的浓度为( )
A.1.2 mol·L-1
B.小于1.2 mol·L-1
C.大于1.2 mol·L-1
D.不能确定
3.在一定的条件下,某反应X(g)Y(g)+Z(g)分解的部分实验数据如下:
反应时间/min
0
10
20
30
40
50
c(X)/(mol·L-1)
0.100
0.090
0.080
0.070
0.060
0.050
反应时间/min
60
70
80
90
100
c(X)/(mol·L-1)
0.040
0.030
0.020
0.010
0.000
下列有关说法正确的是( )
A.X的浓度越大,反应速率越大
B.X的浓度越大,消耗一半时所用的时间越短
C.X分解的速率与其浓度无关
D.X的分解速率先快后慢
4.一定温度下,在某密闭容器中发生反应:2HI(g)H2(g)+I2(g) ΔH>0,若15 s内c(HI)由0.1 mol·L-1降到0.07 mol·L-1,则下列说法正确的是( )
A.0~15 s内用I2表示的平均反应速率为v(I2)=0.002 mol·L-1·s-1
B.c(HI)由0.07 mol·L-1降到0.05 mol·L-1所需的反应时间小于10 s
C.升高温度正反应速率加快,逆反应速率减慢
D.减小反应体系的体积,化学反应速率加快
5.从下列实验事实所引出的相应结论正确的是( )
选项
实验事实
结论
A
其他条件相同,Na2S2O3溶液浓度越大,析出S沉淀所需时间越短
当其他条件不变时,增大反应物浓度,化学反应速率加快
B
在化学反应前后,催化剂的质量和化学性质都没有发生改变
催化剂一定不参与化学反应
C
物质的量浓度相同的盐酸和醋酸分别与等质量的、形状相同的锌粒反应
反应开始时速率相同
D
在容积可变的密闭容器中发生反应H2(g)+I2(g)2HI(g),把容积缩小一半
正反应速率加快,逆反应速率不变
6.(2018贵州贵阳高三检测)在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)2HI(g) ΔH<0,下列说法正确的是( )
A.保持容器容积不变,向其中加入1 mol H2(g),反应速率一定加快
B.保持容器容积不变,向其中加入1 mol N2(N2不参加反应),反应速率一定加快
C.保持容器内气体压强不变,向其中加入1 mol N2(N2不参加反应),反应速率一定加快
D.保持容器内气体压强不变,向其中加入1 mol H2(g)和1 mol I2(g),再次平衡时反应速率一定加快
7.一定温度下,10 mL 0.40 mol·L-1 H2O2发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min
0
2
4
6
8
10
V(O2)/mL
0.0
9.9
17.2
22.4
26.5
29.9
下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6 min的平均反应速率:v(H2O2)≈3.3×10-2mol·L-1·min-1
B.6~10 min的平均反应速率:v(H2O2)<3.3×10-2mol·L-1·min-1
C.反应至6 min时,剩余的c(H2O2)=0.3 mol·L-1
D.反应至6 min时,H2O2分解了50%
8.(2018广州模拟)在稀硫酸与锌反应制取氢气的实验中,探究加入硫酸铜溶液的量对氢气生成速率的影响。实验中锌粒过量且颗粒大小相同,饱和硫酸铜溶液用量0~4.0 mL,保持溶液总体积为100.0 mL,记录获得相同体积(336 mL)的气体所需时间,实验结果如图所示(气体体积均转化为标准状况下)。据图分析,下列说法不正确的是( )
A.饱和硫酸铜溶液用量过多不利于更快收集氢气
B.a、c两点对应的氢气生成速率相等
C.b点对应的反应速率为v(H2SO4)=1.0×10-3mol·L-1·s-1
D.d点没有构成原电池,反应速率减慢
9.(2018浙江宁波十校模拟)某温度下,在容积为2 L的密闭容器中投入一定量的A、B发生反应3A(g)+bB(g)cC(g) ΔH=-Q kJ·mol-1(Q>0),12 s时反应达到平衡,生成C的物质的量为0.8 mol,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是( )
A.前12 s内,A的平均反应速率为0.025 mol·L-1·s-1
B.12 s后,A的消耗速率等于B的生成速率
C.化学计量数之比b∶c=1∶2
D.12 s内,A和B反应放出的热量为0.2Q kJ
二、非选择题(本题共2小题,共37分)
10.(17分)在一定条件下,二氧化硫和氧气发生反应:
2SO2(g)+O2(g)2SO3(g)。
(1)降低温度,化学反应速率 (填“增大”“减小”或“不变”)。
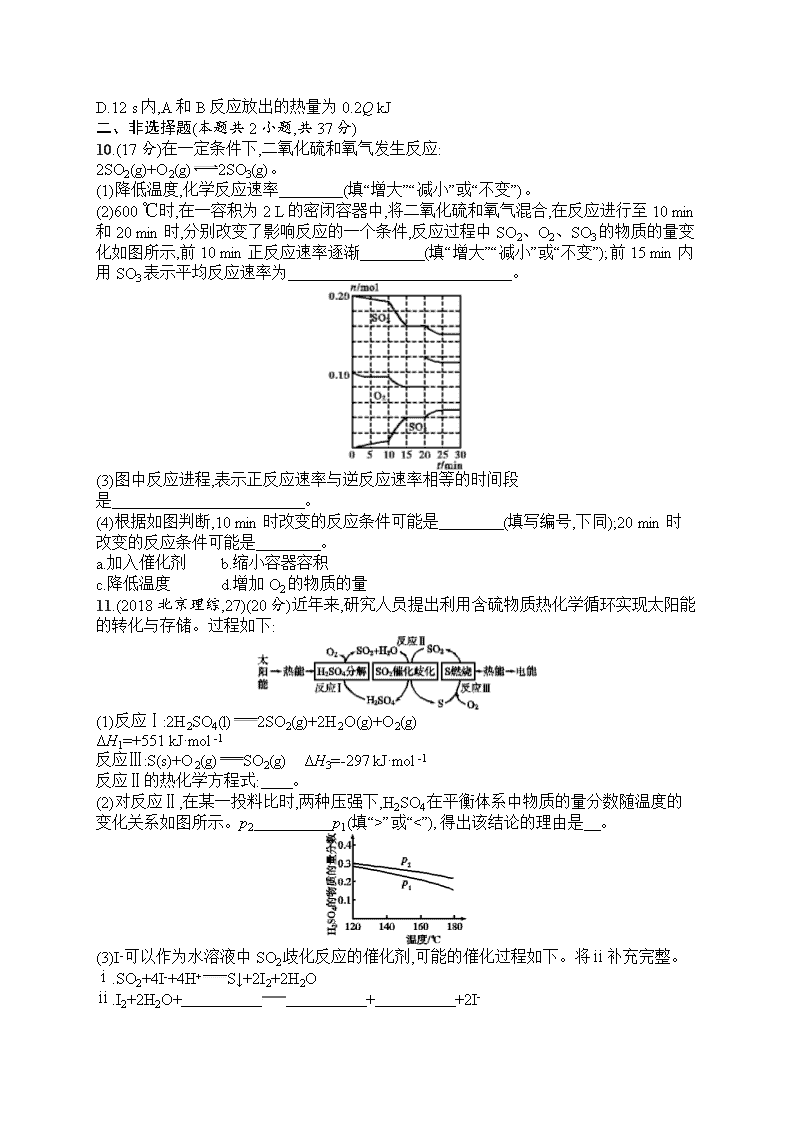
(2)600 ℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10 min和20 min时,分别改变了影响反应的一个条件,反应过程中SO2、O2、SO3的物质的量变化如图所示,前10 min正反应速率逐渐 (填“增大”“减小”或“不变”);前15 min内用SO3表示平均反应速率为 。
(3)图中反应进程,表示正反应速率与逆反应速率相等的时间段是 。
(4)根据如图判断,10 min时改变的反应条件可能是 (填写编号,下同);20 min时改变的反应条件可能是 。
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O2的物质的量
11.(2018北京理综,27)(20分)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
(1)反应Ⅰ:2H2SO4(l)2SO2(g)+2H2O(g)+O2(g)
ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式: 。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示。p2 p1(填“>”或“<”),得出该结论的理由是 。
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。
ⅰ.SO2+4I-+4H+S↓+2I2+2H2O
ⅱ.I2+2H2O+ + +2I-
(4)探究ⅰ、ⅱ反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号
A
B
试剂组成
0.4 mol·L-1 KI
a mol·L-1 KI
0.2 mol·L-1 H2SO4
实验现象
溶液变黄,一段时间后出现浑浊
溶液变黄,出现浑浊较A快
序号
C
D
试剂组成
0.2 mol·L-1 H2SO4
0.2 mol·L-1 KI
0.000 2 mol I2
实验现象
无明显现象
溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快
①B是A的对比实验,则a= 。
②比较A、B、C,可得出的结论是 。
③实验表明,SO2的歧化反应速率D>A,结合ⅰ、ⅱ反应速率解释原因: 。
课时规范练19 化学反应速率
1.B 块状大理石、粉末状大理石分别与盐酸反应时,接触面积不同,反应速率不同,A项错误;两种酸中的c(H+)浓度相同,反应速率相同,B项正确;铁和镁的活泼性不同,反应速率不同,C项错误;物质的量浓度相同的盐酸和醋酸中自由移动的c(H+)是不相同的,反应速率不同,D项错误。
2.B 前3 s用N2表示的反应速率为0.1 mol·L-1·s-1,即用NO表示的反应速率为0.2 mol·L-1·s-1。如果3~6 s的反应速率仍为0.2 mol·L-1·s-1,则6 s末NO的浓度为1.2 mol·L-1。由于随着反应进行,反应物浓度减小,反应速率减慢,故6 s末NO的浓度小于1.2 mol·L-1。
3.C X的分解速率是匀速的,与其浓度无关,A、D项错误,C项正确;X的分解速率不变;X的浓度越大,消耗一半时所用的时间越长,B项错误。
4.D 0~15 s内,v(I2)=12v(HI)=12×(0.1-0.07)mol·L-115 s=0.001 mol·L-1·s-1,A项错误;随着反应的进行,c(HI)减小,v(HI)减小,故c(HI)由0.07 mol·L-1降到0.05 mol·L-1所需时间大于10 s,B项错误;升高温度,正、逆反应速率均增大,C项错误;减小反应体系的体积,压强增大,反应速率加快,D项正确。
5.A 增大反应物浓度,化学反应速率加快,A项正确;催化剂参与反应,但反应前后质量和化学性质不变,B项错误;浓度相同的盐酸和醋酸溶液中起始氢离子浓度不同,因此开始时反应速率不同,C项错误;缩小容器容积,正、逆反应速率同时增大,D项错误。
6.A 增加反应物的浓度,反应速率加快,A项正确;加入氮气,因为容器容积不变,反应体系中各气体的浓度不变,故反应速率不变,B项错误;保持压强不变,加入氮气,容器容积增大,反应体系中各气体的浓度减小,反应速率减小,C项错误;保持压强不变,再次充入1 mol H2(g)和1 mol I2(g),则容器容积增大为原来的2倍,再次平衡反应体系中各气体的浓度不变,反应速率不变,D项错误。
7.C 在前6 min中生成O222.4 mL,即0.001 mol,根据化学方程式2H2O22H2O+O2↑可知,反应掉的H2O2为0.002 mol,故v(H2O2)=0.002mol0.01 L×6min≈3.3×10-2 mol·L-1·min-1,A项正确;由表格中的数据可知在相同的时间间隔中,生成的O2的体积越来越小,故6~10 min的平均反应速率要小于0~6 min的平均反应速率,B项正确;反应到6 min时,剩余的n(H2O2)=0.004 mol-0.002 mol=0.002 mol,故剩余的c(H2O2)=0.002mol0.01 L=0.2 mol·L-1,C项错误;反应到6 min时,H2O2分解率为0.002mol0.004mol×100%=50%,D项正确。
8.D 根据图像可知随着饱和硫酸铜溶液的增加,收集相同体积的气体所需时间先逐渐减少,然后又逐渐增加,因此饱和硫酸铜溶液用量过多不利于更快收集氢气,A项正确;根据图像可知a、c两点对应的时间都是250 s,所以生成氢气速率相等,B项正确;b点对应的时间是150 s,生成氢气的物质的量是0.015 mol,消耗稀硫酸的物质的量是0.015 mol,其浓度为0.015mol0.1 L=0.15 mol·L-1,所以反应速率v(H2SO4)=1.0×10-3mol·L-1·s-1,C项正确;d点锌也与硫酸铜溶液反应生成铜从而构成原电池,D项错误。
9.C 分析图像可知12 s内A的浓度变化为(0.8-0.2)mol·L-1=0.6 mol·L-1,反应速率v(A)=ΔcΔt=0.6mol·L-112 s=0.05 mol·L-1·s-1,A项错误;分析图像,12 s内B的浓度变化为(0.5-0.3) mol·L-1=0.2 mol·L-1,v(B)=0.2mol·L-112 s=160 mol·L-1·s-1,速率之比等于化学计量数之比,3∶b=0.05∶160,则b=1,3∶c=0.05∶0.8212,则c=2,A、B的化学计量数不同,12 s后达到平衡状态,A的消耗速率不等于B的生成速率,B项错误,C项正确;消耗3 mol A放热Q kJ,12 s内消耗A的物质的量为0.6 mol·L-1×2 L=1.2 mol,消耗1.2 mol A放出的热量为0.4Q kJ,D项错误。
10.答案 (1)减小 (2)减小 1.33×10-3mol·L-1·min-1
(3)15~20 min,25~30 min (4)ab d
解析 (1)降低温度,化学反应速率减小。(2)前10 min随着反应的不断进行,反应物SO2和O2的浓度不断减小,正反应速率减小,前15 min内用SO3表示的平均反应速率为0.04mol2 L×15min≈1.33×10-3mol·L-1·min-1。(3)反应过程中SO2、O2、SO3物质的量不随时间变化的时间段是15~20 min和25~30 min,反应处于平衡状态。(4)10~15 min三条曲线的斜率突然变化,根据图示可知反应速率突然加快,其原因可能是加入催化剂或缩小容器容积。反应进行至20 min时,曲线发生的变化是O2的物质的量突然增大,平衡发生移动,引起SO2、SO3的物质的量随之发生变化。
11.答案 (1)3SO2(g)+2H2O(g)2H2SO4(l)+S(s)
ΔH=-254 kJ·mol-1
(2)> 反应Ⅱ是气体分子数减小的反应,温度一定时,增大压强,化学平衡正向移动,H2SO4的物质的量分数增大
(3)SO2 4H+ SO42-
(4)①0.4 ②I-是SO2歧化反应的催化剂,且在H+存在下,催化速率加快;但H+单独存在时,不具有催化作用 ③反应ⅱ比反应ⅰ快,增大I2的浓度,反应ⅱ的反应速率加快,H+浓度增大,加强了I-的催化能力
解析 (1)由题给示意图可知,反应Ⅱ为二氧化硫发生歧化反应生成硫酸和硫,反应的化学方程式为3SO2(g)+2H2O(g)2H2SO4(l)+S(s),由盖斯定律可知,-(反应Ⅲ+反应Ⅰ)得反应Ⅱ,则ΔH=-(ΔH3+ΔH1)=-(-297 kJ·mol-1)-(+551 kJ·mol-1)=-254 kJ·mol-1,则热化学方程式为3SO2(g)+2H2O(g)2H2SO4(l)+S(s) ΔH=-254 kJ·mol-1;(2)反应Ⅱ为气态物质化学计量数减小的反应,增大压强,化学平衡正向移动,硫酸的物质的量分数增大,则p2大于p1;(3)由题意可知,I-为反应的催化剂,则反应ⅱ的反应物为I2、SO2和水,生成物为氢碘酸和硫酸,反应的离子方程式为I2+SO2+2H2O4H++2I-+SO42-;(4)①A与B是探究H+浓度对反应速率的影响,因此A和B中KI溶液浓度必须相同,则a为0.4;②对比A、B、C的实验现象可知,I-是SO2歧化反应的催化剂,且在H+存在下,催化速率加快;但H+单独存在时,不具有催化作用;③对比A、D实验现象可知,增大I2的浓度,反应ⅱ的反应速率加快,H+浓度增大,加强了I-的催化能力。