- 484.17 KB
- 2021-07-05 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
安徽省宣城市2019-2020学年高一上学期期末考试
化学试题
本试卷分第I卷(选择题)和第II 卷(非选择题)两部分,满分100分,考试时间100分钟。
考生注意事项:
1.答题前,考生先将自己的姓名。考号在答题卡指定位置填写清楚并将条形码粘贴在指定区域。
2.考生作答时,请将答案答在答题卡上。第I卷每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;第II卷请用0.5毫米的黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区城书写的答案无效。在试题卷、草稿纸上作答无效。
可能用到的相对原子质量:H-1 C-12 O-16 F-19 Na-23 A1-27 Cl-35.5 Fe-56
第I卷 (选择题 共54分)
一、选择题(本题包括18小题,每小题3分,共54分。在每小题給出的四个选项中,只有一个选项符合题意。)
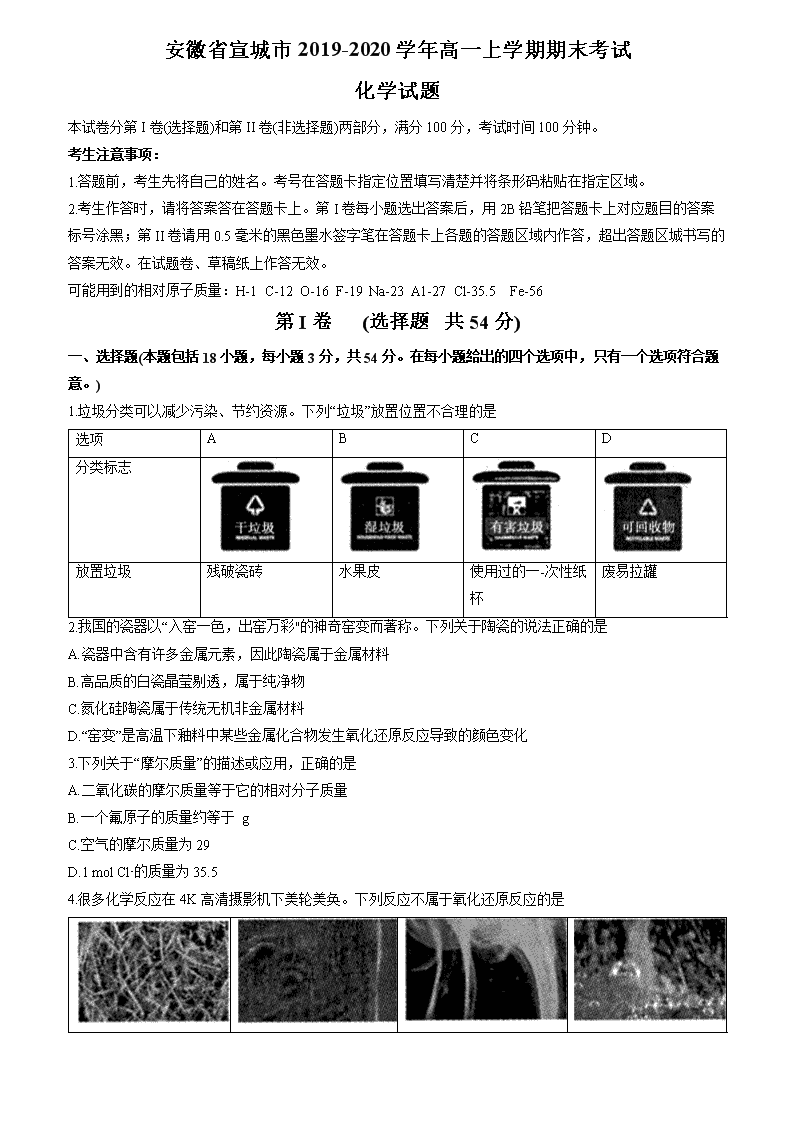
1.垃圾分类可以减少污染、节约资源。下列“垃圾”放置位置不合理的是
选项
A
B
C
D
分类标志
放置垃圾
残破瓷砖
水果皮
使用过的一-次性纸杯
废易拉罐
2.我国的瓷器以“入窑一色,出窑万彩"的神奇窑变而著称。下列关于陶瓷的说法正确的是
A.瓷器中含有许多金属元素,因此陶瓷属于金属材料
B.高品质的白瓷晶莹剔透,属于纯净物
C.氮化硅陶瓷属于传统无机非金属材料
D.“窑变”是高温下釉料中某些金属化合物发生氧化还原反应导致的颜色变化
3.下列关于“摩尔质量”的描述或应用,正确的是
A.二氧化碳的摩尔质量等于它的相对分子质量
B.一个氟原子的质量约等于 g
C.空气的摩尔质量为29
D.1 mol Cl-的质量为35.5
4.很多化学反应在4K高清摄影机下美轮美奂。下列反应不属于氧化还原反应的是
Al片投入AgNO3溶液中
Zn片投入CuSO4溶液中
AgNO3溶液滴入NaCl溶液中
Mg条投入盐酸中
A
B
C
D
5.下列物质在水溶液中的电离方程式书写正确的是
A. NaHCO3=Na++HCO3- B. KClO3=K++Cl5++3O2-
C. MgSO4= Mg+2+SO42- D. Ba(OH)2=Ba2++(OH)22-
6.下列物质的分类正确的是
选项
物质
类别
A
纯碱
碱
B
氯水
混合物
C
过氧化钠
碱性氧化物
D
硫酸铜溶液
电解质
7.以下是四位同学在学习了《化学必修一》后,对一些知识的认识,你认为正确的是
A.A B.B C.C D.D
8.相同状况下,体积相等的五个气球分别充满相应的气体,如下图所示。与氯化氢气球中所含原子数一定相等的是
9.有些物质既能与强酸溶液反应又能与强碱溶液反应,下列物质不具有此类性质的是
A.四氧化三铁 B.碳酸氢钠 C.铝 D.氢氧化铝
10.下列物质间的转化不能通过一步反应实现的是
A.Na2CO3→NaOH B. Fe→FeC]2
C.Fe(OH)2→Fe(OH)3 D.SiO2→H2SiO3
11.可以根据5I- +IO3-+6H+=3I2+3H2O检验食盐中是否存在IO3-。下列说法正确的是
A.I2是氧化产物,H2O是还原产物 B. IO3-得电子,被氧化
C.该条件下氧化性:IO3-强于I- D.每生成3 mol I2.转移6 mol电子
12.用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,22.4 L H2O含有的分子数为NA
B.常温常压下,1.06 g Na2CO3溶于水,溶液中Na+数目为0.02NA
C. NA个O2分子占有的体积约为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含Cl-数目为NA
13.下列离子组能大量共存且溶液为无色透明的是
A. K+、SO42-、H+、Cu2+ B. Na+、OH-、Cl-、SO42-
C. H+、Na+、Cl-、SiO32- D. Na+、Ba2+、NO3-、SO42-
14.下列反应的离子方程式书写不正确的是
A.金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑
B.氧气与水反应:Cl2+H2O=H++C1-+HClO
C.稀盐酸与碳酸钙反应:CaCO3+2H+=Ca2+ +CO2↑+H2O
D.稀硫酸与铁反应:6H++2Fe=2Fe3++3H2↑
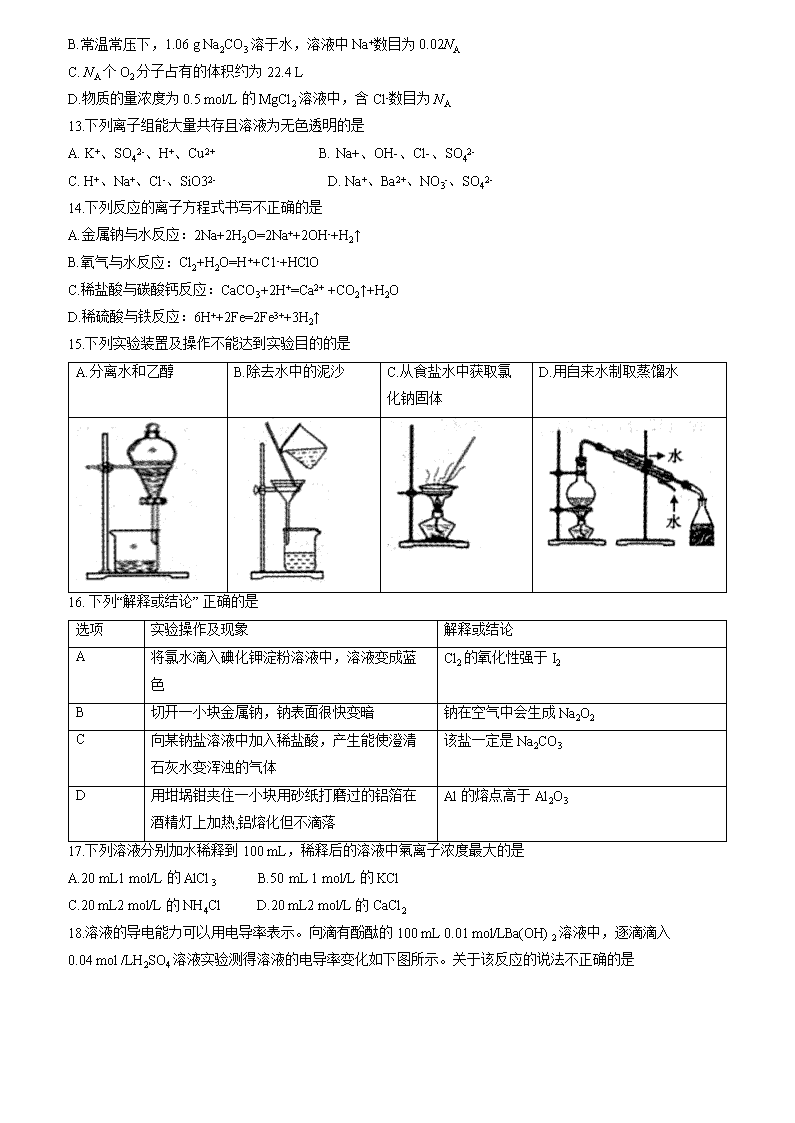
15.下列实验装置及操作不能达到实验目的的是
A.分离水和乙醇
B.除去水中的泥沙
C.从食盐水中获取氯化钠固体
D.用自来水制取蒸馏水
16. 下列“解释或结论” 正确的是
选项
实验操作及现象
解释或结论
A
将氯水滴入碘化钾淀粉溶液中,溶液变成蓝色
Cl2的氧化性强于I2
B
切开一小块金属钠,钠表面很快变暗
钠在空气中会生成Na2O2
C
向某钠盐溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体
该盐一定是Na2CO3
D
用坩埚钳夹住一小块用砂纸打磨过的铝箔在酒精灯上加热,铝熔化但不滴落
Al的熔点高于Al2O3
17.下列溶液分别加水稀释到100 mL,稀释后的溶液中氣离子浓度最大的是
A.20 mL1 mol/L的AlCl3 B.50 mL 1 mol/L的KCl
C.20 mL2 mol/L的NH4Cl D.20 mL2 mol/L的CaCl2
18.溶液的导电能力可以用电导率表示。向滴有酚酞的100 mL 0.01 mol/LBa(OH)2溶液中,逐滴滴入0.04 mol /LH2SO4溶液实验测得溶液的电导率变化如下图所示。关于该反应的说法不正确的是
A 0-85s观察到的现象:溶液中有白色沉淀生成,溶液红色逐渐变浅,最后变为无色
B. a→b过程中发生的离子反应为:H++SO42-+Ba2++OH-=BaSO3↓+H2O
C.滴至b点时消耗H2SO4溶液25 mL
D. b→c过程溶液的电导率变大是由于溶液中H+和SO42-浓度增大
第II卷 (非选择题 共46 分)
二、填空题(本题包括4小题,共46分)
19. (12 分)下图是地壳中含量较大的九种元素分布图,图中X.Y .Z分别表示不同元素。
回答下列问题:
(1)X的名称为_________________,硅元素在自然界以______ (填"游离态"或“化合态”)形式存在。
(2)Y的氧化物属于______氧化物, 硅的氧化物属于______氧化物(填“酸性”、 “两性”或“碱性" )。
(3)常用ZCl3溶液作为刻制印刷电路时的“腐蚀液" ,该反应的离子方程式为___________,区别ZCl3溶液和Z(OH)3胶体的方法是______________。
(4)由粗硅制备硅烷(SiH4)的基本流程如下图所示(反应条件均省略):
已知:反应I、II的化学方程式分别为Si+3HC1=SiHCl3+A,SiHCl3+B=Si+3HC1( 均已配平)。
①A的化学式为____________。
②反应I、II、III中,有_______个属于氧化还原反应。
③反应IV中生成的SiH4和NH3两种气体的物质的量之比为___________。
20. (10分)实验室用下图的实验装置模拟工业制漂白粉。回答下列问题:
(1)仪器a的名称是________________。
(2)写出A装置中反应的化学方程式并标出电子转移的方向和数目_______________。
(3)浓盐酸在反应中的作用是______________________,,饱和食盐水的作用是____________,D装置的作用是______________。
(4)C装置制取漂白粉的化学方程式是_____________________。
21. (12分)某同学用硫鉄ず焙斃后的焼溘(主要成分カFe2O3、SiO2、Al2O3。不考虑其它杂质)制取绿矾(FeSO4· 7H2O),設計了如下流程(部分物质巳略去)。
回答下列问题:
(1)硫铁矿的主要成分是FeS2,其中铁元素化合价为_________,焙烧产物之一的Fe2O3,俗称___________。
(2)固体A的主要成分是_________,固体X为_________________。
(3)写出①中Al2O3发生反应的高子方程式:_____________________。
(4)从溶液C到绿矾的过程中,須控制反应条件訪止变质,检验其变质所用的化学试剂是_________,步骤③所得Al(OH)3沉淀含有杂质,应如何洗涤?______________________。
22. (12分)某兴趣小组在处理污水样品吋,需将质量分数为37%的浓盐酸(密度为1.19g /cm3)配制成250 mL 0.3mol/L的盐酸。回答下列问题:
(1)配制此溶液除上图仪器外,逐需要的仪器是_____________,按使用的先后顺序,其作用分別是____和__________。
(2)A、B仪器的规格分別是______、________(填代号)。
①10 mL ②100 mL ③250 mL ④500 mL
(3)下列説法正确的是______ ( 填代号)。
A使用的容量瓶必须洁净,但不一定需要干燥
B.配制溶液肘,如果试样是固体,把称好的试样用紙条小心倒入容量瓶中,緩慢加水至接近刻度线1 – 2 cm处,改用胶头滴管加蒸馏水至刻度线
C实验所用的量筒、烧杯等都要洗涤2~3次,洗涤液要全部注入容量瓶
D.若定容时俯视液面,所配溶液的物貭的量浓度偏高
(4)求质量分数为37%的液盐酸的物貭的量依度(要求写出計算辻程,汁算结果保留两位小数)。
安徽省宣城市2019-2020学年高一上学期期末考试
化学试题参考答案
一、选择题(本题包括18小题,每小题3分,共54分。在每小题给出的四个选项中,只有一个选项符合题意。)
1-5:CDBCA 6-10:BCCAD 11-15:CBBDA 16-18:ADB
二.填空题(本题包括4小题,共46分)
19. (12分)
(1)氧(1分);化合态(1分)
(2)两性(1分);酸性(1分)
(3)2Fe3++Cu=2Fe2++Ca2+ (2 分)丁达尔效应(1分,其他合理答案均可)
(4)①H2(1分);②3(2分);③ 1:4(2分)
20. (10 分)
(1)分液漏斗(1分)
(2) (3分,或单线桥)
(3)酸性和还原性(1分);除去 Cl2中混有的HCl气体(1分);安全瓶, 防止E中溶液倒吸入C中(2分)
(4)2Cl2+2Ca( OH)2 =CaCl2+Ca( ClO)2+2H2O(2分)
21. (12分)
(1) +2(1分);铁红(1分)
(2)SiO2(2分);Fe(2分,其他合理答案也给分)
(3)Al2O3+6H+= 2Al3+ +3H2O(2分)
(4)KSCN溶液(2分);向过滤器(或漏斗)中加蒸馏水至浸没沉淀,待水流出后重复操作2-3次(2分)
22. (12分)
(1)玻璃棒(1分);搅拌(1分);引流(1 分)
(2)③(1分);①(2分)
(3)A、D(2分)
(4)12.06 mol/L (4分,要求写出计算过程并保留两位小数)
相关文档
- 【化学】甘肃省天水市2019-2020学2021-07-055页
- 内蒙古赤峰市宁城县2019-2020学年2021-07-0518页
- 【化学】湖南省长沙浏阳市2019-2022021-07-057页
- 2019-2020学年黑龙江哈尔滨市第三2021-07-054页
- 2018-2019学年河南省安阳市第三十2021-07-056页
- 【化学】陕西省西安电子科技大学附2021-07-0517页
- 2019-2020学年甘肃省静宁县第一中2021-07-0522页
- 2018-2019学年吉林省实验中学高一2021-07-059页
- 【化学】湖南省常德市2019-2020学2021-07-0518页
- 2018-2019学年福建省八县(市)一中高2021-07-059页