- 891.72 KB
- 2021-07-05 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
定远重点中学 2020 届高三下学期 6 月模拟考试
理科综合能力测试
本卷满分 300 分,考试用时 150 分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 K 39 Fe 56 Cu 64
第I卷(共126分)
一、选择题:本题共 13 小题,每小题 6 分,共 78 分。每小题给出的 4 个选项中
只有一项是符合题意要求的。
7.化学与科技、社会、生产密切相关,下列说法错误的是
A. 我国出土的青铜礼器司母戊鼎是铜和铁的合金
B. 高纯硅具有良好的半导体性能,可用于制光电池
C. 港珠澳大桥钢筋表面的环氧树脂涂层属于合成高分子材料
D. 火箭推进剂使用煤油-液氧比偏二甲肼-四氧化二氮的环境污染小
8.屠呦呦因发现治疗疟疾的青蒿素和双氢青蒿素(结构如图)获得诺贝尔生理学或
医学奖.一定条件下青蒿素可以转化为双氢青蒿素.下列有关说法中正确的是
A. 青蒿素的分子式为 C15H20O5
B. 双氢青蒿素能发生氧化反应、酯化反应
C. 1 mol 青蒿素最多能和 1 molBr2 发生加成反应
D. 青蒿素转化为双氢青蒿素发生了氧化反应
9.NA 为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,0.1molCl2 溶于水,转移的电子数目为 0.1NA
B. 标准状况下,6.72LNO2 与水充分反应转移的电子数目为 0.1NA
C. 1.0L1.0mo1·L-1 的 NaAlO2 水溶液中含有的氧原子数为 2NA
D. 常温常压下,14g 由 N2 与 CO 组成的混合气体含有的原子数目为 NA
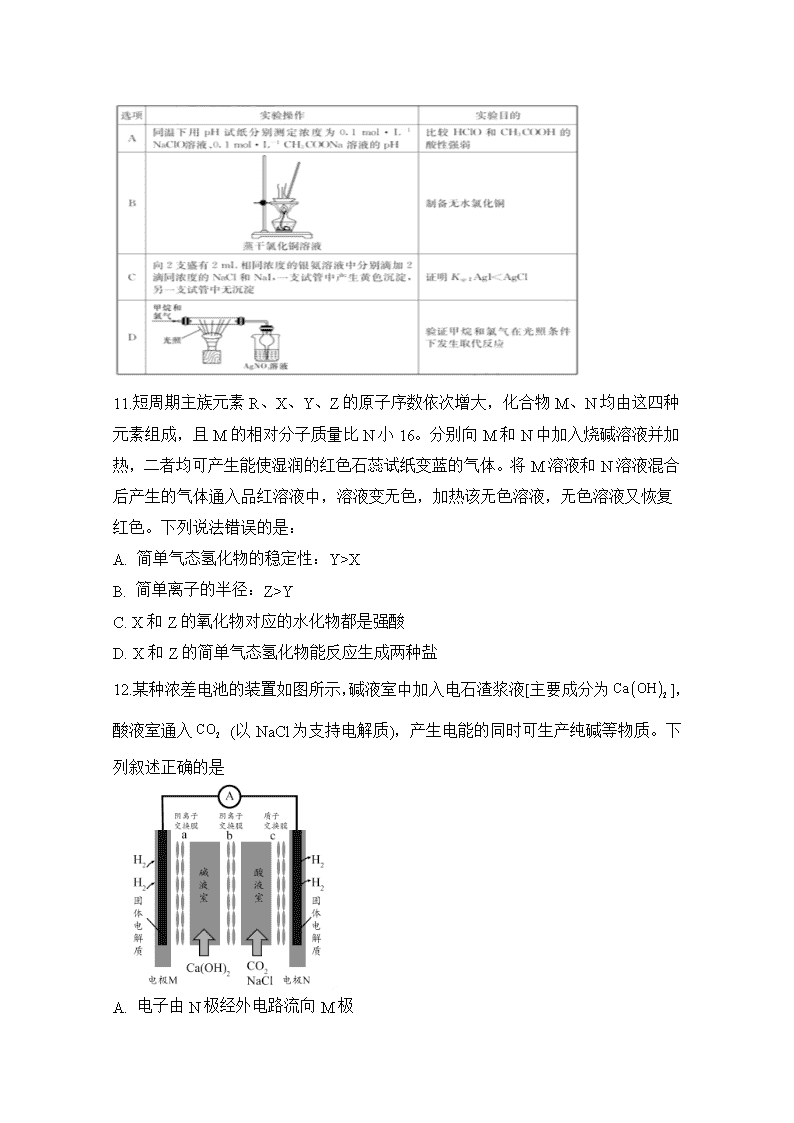
10.下列有关实验的叙述完全正确的是
11.短周期主族元素 R、X、Y、Z 的原子序数依次增大,化合物 M、N 均由这四种
元素组成,且 M 的相对分子质量比 N 小 16。分别向 M 和 N 中加入烧碱溶液并加
热,二者均可产生能使湿润的红色石蕊试纸变蓝的气体。将 M 溶液和 N 溶液混合
后产生的气体通入品红溶液中,溶液变无色,加热该无色溶液,无色溶液又恢复
红色。下列说法错误的是:
A. 简单气态氢化物的稳定性:Y>X
B. 简单离子的半径:Z>Y
C. X 和 Z 的氧化物对应的水化物都是强酸
D. X 和 Z 的简单气态氢化物能反应生成两种盐
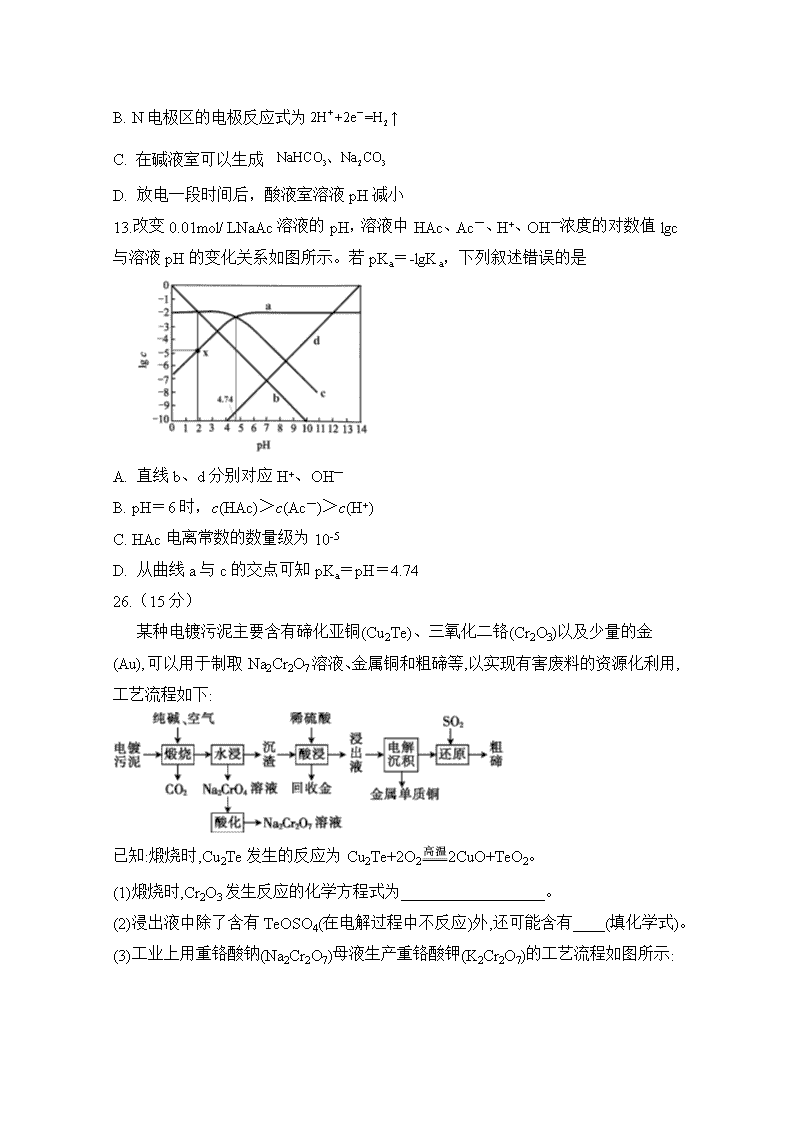
12.某种浓差电池的装置如图所示,碱液室中加入电石渣浆液[主要成分为
2Ca OH ],酸液室通入 2CO (以 NaCl 为支持电解质),产生电能的同时可生产纯碱
等物质。下列叙述正确的是
A. 电子由 N 极经外电路流向 M 极
B. N 电极区的电极反应式为 2
+2H +2e =H- ↑
C. 在碱液室可以生成 3 2 3 NaHCO Na CO、
D. 放电一段时间后,酸液室溶液 pH 减小
13.改变 0.01mol/LNaAc 溶液的 pH,溶液中 HAc、Ac-、H+、OH-浓度的对数值 lgc
与溶液 pH 的变化关系如图所示。若 pKa=-lgKa,下列叙述错误的是
A. 直线 b、d 分别对应 H+、OH-
B. pH=6 时,c(HAc)>c(Ac-)>c(H+)
C. HAc 电离常数的数量级为 10-5
D. 从曲线 a 与 c 的交点可知 pKa=pH=4.74
26.(15 分)
某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),
可以用于制取 Na2Cr2O7 溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺
流程如下:
已知:煅烧时,Cu2Te 发生的反应为 Cu2Te+2O2 2CuO+TeO2。
(1)煅烧时,Cr2O3 发生反应的化学方程式为__________________。
(2)浸出液中除了含有 TeOSO4(在电解过程中不反应)外,还可能含有____(填化学
式)。
(3)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:
通过冷却结晶能析出大量 K2Cr2O7 的原因是__________________。
(4)测定产品中 K2Cr2O7 含量的方法如下:称取产品试样 2.50 g 配成 250 mL 溶液,用
移液管取出 25.00 mL 于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用
0.1000 mol·L-1 硫酸亚铁铵(NH4)2Fe(SO4)2 标准液进行滴定,重复进行二次实验。(已
知 Cr2
2-
7O 被还原为 Cr3+)
①氧化还原滴定过程中的离子方程式为________________。
②若三次实验消耗(NH4)2Fe(SO4)2 标准液的平均体积为 25.00 mL,则所得产品中
K2Cr2O7 的纯度为_____%。[已知 M(K2Cr2O7)=294 g·mol-1,计算结果保留三位有效
数字]。
(5)上述流程中 K2Cr2O7 发生氧化还原反应后所得溶液中除含有 Cr3+外,还含有一定
浓度的 Fe3+杂质,可通过加碱调 pH 的方法使两者转化为沉淀。已知 c(Cr3+)=3×10-5
mol·L-1,则当溶液中开始析出 Cr(OH)3 沉淀时 Fe3+是否沉淀完全?____(填“是”或
“否”)。{已知:Ksp[Fe(OH)3]=4.0×10-38, Ksp[Cr(OH)3]=6.0×10-31}
27. (14 分)
氯化钠(NaCN)是一种基本化工原料,同时也是一种毒物质。一旦泄漏需要及
时处理,一般可以通过喷酒双氧水或过硫酸钠(Na2S2)溶液来处理,以减少对环境
的污染。
I.(1)NaCN 用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝
的气体,该反应的化学方程式是___________________________________。
II.工业制备过硫酸钠的反应原理如下所示
主反应:(NH4)2S2O8+2NaOH 55 C
Na2S2O8+2NH3↑+2H2O
副反应:2NH3+3Na2S2O8+6NaOH 90 C
6Na2SO4+N2+6H2O
某化学小组利用上述原理在实验室制备过硫酸,并用过硫酸钠溶液处理含氰化钠
的废水。
实验一:实验室通过如下图所示装置制备 Na2S2O8。
(2)装置中盛放(NH4)2S2O8 溶液的仪器的名称是____________。
(3)装置 a 中反应产生的气体需要持续通入装置 c 的原因是____________________。
(4)上述装置中还需补充的实验仪器或装置有______________(填字母代号)。
A.温度计 B 水浴加热装置
C.洗气瓶 D.环形玻璃搅拌棒
实验二:测定用过硫酸钠溶液处理后的废水中氯化钠的含量。
已知;①废水中氯化钠的最高排放标准为 0.50mg/L。
②Ag++2CN—===[Ag(CN)2]—,Ag++I—==AgI↓,AgI 呈黄色,CN—优先与 Ag+发
生反应。实验如下:取 1L 处理后的 NaCN 废水,浓缩为 10.00mL 置于锥形瓶中,
并滴加几滴 KI 溶液作指示剂,用 1.010—3mol/L 的标准 AgNO3 溶液滴定,消耗
AgNO3 溶液的体积为 5.00mL
(5)滴定终点的现象是___________________________________。
(6)处理后的废水中氰化钠的浓度为____________________mg/L.
Ⅲ.(7)常温下,含硫微粒的主要存在形式受 pH 的影响。利用电化学原理,用惰性
电极电解饱和 NaHSO4 溶液也可以制备过硫酸钠。已知在阳极放电的离子主要为
HSO4—,则阳极主要的反应式为_________________________。
28. (14 分)
研究处理 NOx、SO2,对环境保护有着重要的意义。回答下列问题:
(1)SO2 的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的 SO2。已
知吸收过程中相关反应的热化学方程式如下:① SO2(g) + NH3•H2O(aq)
=NH4HSO3(aq)
△
H1 = a kJ•mol-1;② NH3•H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq)
+ H2O(l)
△
H2 = b kJ•mol-1;③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq)
△
H3= c
kJ•mol-1,则反应 2SO2(g) + 4NH3•H2O(aq) + O2(g) =2(NH4)2SO4(aq) + 2H2O(l)
△
H =
______。
(2)NOx 的排放主要来自于汽车尾气,有人利用反应 C (s) + 2NO(g) N2(g) + CO2(g)
△
H=-34.0 kJ•mol-1,用活性炭对 NO 进行吸附。在恒压密闭容器中加入足量的活
性炭和一定量的 NO 气体,测得 NO 的转化率 α(NO)随温度的变化如图所示:
①由图可知,1050K 前反应中 NO 的转化率随温度升高而增大,原因是
_________________________; 在 1100K 时,CO2 的体积分数为______。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作 Kp)。
在 1050K、1.1×106Pa 时,该反应的化学平衡常数 Kp=________(已知:气体分压
=气体总压×体积分数)。
(3)在高效催化剂的作用下用 CH4 还原 NO2,也可消除氮氧化物的污染。在相同条
件下,选用 A、B、C 三种不同催化剂进行反应,生成 N2 的物质的量与时间变化
关系如图所示,其中活化能最小的是_________(填字母标号)。
(4)在汽车尾气的净化装置中 CO 和 NO 发生反应:2NO(g) + 2CO(g) N2(g) +
2CO2(g)
△
H2 =-746.8 kJ•mol-1。实验测得,υ正=k 正•c2(NO) •c2(CO) ,υ逆=k 逆•c(N2)
•c2(CO2) (k 正、k 逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k 正增大的倍数_____(填" >”、“< ”或“=”) k 逆增大的倍
数。
②若在 1L 的密闭容器中充入 1 mol CO 和 1 mol NO,在一定温度下达到平衡时,
CO 的转化率为 40%,则 k
k
正
逆
=_____(保留 2 位有效数字)。
29.(10 分)
图甲曲线表示某植物在其他条件适宜,恒温 30°C 时光合速率与光照强度的关
系,图乙是测定的一天内密闭玻璃罩中 CO2 浓度的变化情况.请据图回答下列问
题
(1)图甲曲线中 B 点对应光照强度下叶肉细胞中产生 ATP 的场所有______.C 点
对应的光照强度下,叶肉细胞将表现为 O2______(吸收、释放、不吸收也不释放)
(2)已知该植物光合作用和呼吸作用的最适温度分别为 25°C 和 30°C,在其他条
件不变的情况下,将温度调节到 25°C,甲图曲线中 E 点将向______移动.如果在
E 点条件下突然停止光照,叶肉细胞中 C3 含量将______.
(3)图甲曲线中 C 点与图乙曲线中______点的生理状态相同.根据图乙推测该植
株一天中积累有机物最多的时刻是______(用曲线上的点作答),一天内是否有有
机物的累积__________(是或否)。
(4)利用仪器测定密闭玻璃罩内 CO2 和绿色植物的有机物的变化量:给以 1h 的
充足光照,测得罩内 CO2 比光照前减少了 72mg,植株共合成葡萄糖 90mg,呼吸
底物和光合产物均为葡萄糖,则这一小时光照条件下植物呼吸作用产生 CO2 为
______mg.
30. (10 分)
有些果实在生长结束、成熟开始时,会出现呼吸强度突然升高的现象,称为“呼
吸高峰”。请回答下列有关植物代谢的问题:
(1)植物的生长发育过程,从根本上讲是__________________________的结果。
(2)研究发现在果实成熟过程中,细胞呼吸速率发生变化出现“呼吸峰值”,与乙
烯有关。若利用乙烯的合成抑制剂进一步验证该激素与出现“呼吸峰值”的关系,进
行如下实验,请补充实验步骤,并预测实验结果:
①挑选足量的无破损、生理状态一致的苹果,随机均分成 A、B 两组;
②A 组(对照组)在________________中浸泡,B 组在______________________中浸
泡,处理相同时间后取出;
③从 A、B 两组中取出等量的苹果,分别放入两个相同的密闭容器内;
④利用仪器监测实验开始及之后每隔一小时容器内_______的变化,记录数据并进
行比较。
实验结果:_________________________________________________________。
31. (9 分)
图甲表示某草原生态系统中的食物网简图,图乙代表某生态系统功能随时间的
变化曲线。请据图分析回答下列问题:
(1)生态系统营养结构是___________和___________。图甲的生物中,含能量最少的
是______。
(2)图甲的食物链中,草为兔提供了可以采食的信息,猫头鹰能够依据兔留下的气味
去猎捕,兔同样也可以依据猫头鹰的气味或行为特征去躲避猎捕,这说明了生物之
间的信息传递能够_________________。信息传递、_______________和
_____________共同构成生态系统三大主要功能。
(3)生态系统稳定性的基础是自我调节能力,_________(填“正”或“负”)反馈调节是该
能力的基础。图乙中 y 表示一个外来干扰对生态系统的影响,对 a、b 两个生态系统
施加相同强度的干扰,若ya>yb,则这两个生态系统的恢复力稳定性的关系为a____b。
(4)一般来说,增加生物的种类,可以提高该草原生态系统的抵抗力稳定性,这应用了
生态工程的____________原理。
32. (10 分)
己知某雌雄异株植物(2n=16,XY 型)的花色受两对等位基因(A 和 a、B 和 b)
控制,这两对基因与花色的关系如图所示,请回答下列问题:
(1)上图所示过程说明基因可通过控制酶的合成来控制_________,进而控制生物性
状。从基因结构上分析,基因 B 与 b 的根本区别是__________________。
(2)欲测定该种植物的基因组序列,需对_________条染色体的 DNA 进行测序。
(3)假如基因 A(a)、B(b)位于常染色体上,现有纯合的白花、粉花和红花植株若干,
欲通过一次杂交实验判断控制酶 B 合成的基因是 B 还是 b,则需选择_________进
行杂交,然后观察后代的表现型,若后代_________,则酶 B 是由基因 b 控制合成
的。
(4)假如基因 A、a 位于常染色体上,酶 B 是由基因 B 控制合成的,现有甲(含基因
B 的纯合白花雌株)、乙(纯合粉花雄株)、丙(纯合红花雄株),请设计实验判断基因
B/b 的位置(不考虑 XY 的同源区段):
①实验设计方案:_____________________________________________。
②若__________________,则支持基因 B/b 位于 X 染色体的非同源区段上。
(二)选考题:共 45 分。请考生从给出的 2 道物理题、2 道化学题、2 道生物题
中每科任选一题做答。
33.[物理—选修 3–3](15 分)
(1)(5 分)关于固体、液休和气体,下列说法正确的是______(填正确答案标号,
选对一个得 2 分,选对 2 个得 4 分,选对 3 个得 5 分。每选错一个扣 3 分,最低
得分为 0 分)
A.当分子间距离增大时,分子间作用力减小,分子势能增大
B.空气相对湿度越大时,空气中水蒸气压强就越接近饱和气压
C.由于液体表面层分子间距高大于液体内部分子间距离,故液体表面存在张力
D.单位时间内气体分子对容器壁单位面积上碰撞次数减少,气体的压强可能增大
E.利用氧气的摩尔质量、密度以及阿伏加德罗常数就可以估算出一个氧气分子的体
积
(2). (10 分)如图所示,一气缸内由光滑的活塞封闭着一定量的理想气体,气
缸(足够长)开口竖直向下。活塞下挂一个沙桶,活塞和沙桶的总质量为 m,平衡时
活塞离底部的距离为 h。现往沙桶内缓慢加人沙子,装满沙桶时活塞离底部的距离
高为 H、已知气缸壁的导热性能良好,活塞的横截面积为 S,在缸内可自由滑动且
不漏气;大气压强为 p0,环境温度不变,重力加速度为 g。求
①装入沙桶沙子的质量
△
m;
②若因外界环境温度降低,活塞又回到离底部距离为 h 处,且内能减小了
△
E,则
此过程需要向外界放出热量 Q。
34.. [物理一选修 3–4)(15 分)
(1)(5 分)平行玻璃砖底面涂有反射层,一束由 a、b 两种单色光组成的复合光以
45°人射角斜射到玻璃砖的上表面,经折射反射再折射后的光路如图所示。不考虑
光在玻璃砖上表面的反射则玻璃砖对单色光___________(填“a”或“b”)折射率大;单
色光___________(填“a”或“b”)在玻璃中传播的时间长;两束单色光从玻璃砖上表面
出射后相互___________(填“平行”或“不平行”)。
(2)一列沿简谐横波传播方向上依次有相距为 3m 的两个质点 A 和 B,如图所示
为 A 和 B 的振动图象。波长λ满足 1m<λ<3m,求:
(i)该波传播的速度 v;
(ii)波通过 A、B 两点的时间 t.
35.[化学-选修 3:物质结构与性质](15 分)
钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的钴、硅、
锰、磷、硫等元素。请回答下列有关问题:
(1)基态 Mn 原子的价电子排布式为___________。Mn2+与 Fe2+中,第一电离能较大
的是__________,判断的理由是_____________________________________。
(2)碳元素除可形成常见的氧化物 CO、CO2 外,还可形成 C2O3(结构式为
)。C2O3 中碳原子的杂化轨道类型为___________,CO2 分子的立体
构型为___________。
(3)酞菁钴分子的结构简式如图所示,分子中与钴原子通过配位键结合的氮原子的
编号是______(填“1” “2” “3”或“4”)其中 C、H、O 元素电负性由大到小的顺序是
_________________________
(4)碳酸盐的热分解是由于晶体中的阳离子结合碳酸根中的氧离子,是碳酸根分解
为 CO2 分子的结果。MgCO3 分解温度低于 CaCO3,请解释原因
_________________________。
(5)氧化亚铁晶胞与 NaCl 的相似,NaCl 的晶胞如图所示。由于晶体缺陷,某氧化
亚铁晶体的实际组成为 Fe0.9O,其中包含有 Fe2+和 Fe3+,晶胞边长为 apm,该晶体
的密度为ρg·cm-3,则 a=___________(列出计算式即可,用 NA 表示阿伏加德罗常
数的值)。
36. [化学-选修 5:有机化学基础](15 分)
由 A 和 C 为原料合成治疗多发性硬化症药物 H 的路线如下:
已知:
①A 能与 NaHCO3 溶液反应放出 CO2,其核磁共振氢谱显示有三组峰,峰面积比
为 2:2:1。
②NaBH4 能选择性还原醛、酮,而不还原—NO2。
回答下列问题:
(1)A 的化学名称为________,D 的结构简式为_______。
(2)H 的分子式为_______,E 中官能团的名称为_______。
(3)B→D、E→F 的反应类型分别为_______。
(4)F→G 的化学方程式为________。
(5)与 C 互为同分异构体的有机物的结构简式为_______(核磁共振氢谱为四组峰,
峰面积比为 6:3:1:1)。
(6)设计由 B 和 为原料制备具有抗肿瘤活性药物
的合成路线__________。
37.[生物—选修 1:生物技术实践] (15 分)
LB 液体培养基和 LB 固体培养基是微生物实验室中较常用的一种培养基,其配
方为 10g 蛋白胨、10g/L 酵母提取物、5g/L 氯化钠等,主要用于培养细菌、扩增菌
种数量。某研究组开展了氧气对微生物生长、繁殖的影响实验,请回答下列问题:
(1)要配制供微生物生长、繁殖的培养基,其中一般都含有
________________________________和无机盐等。有些微生物对某些特殊营养物
质及____________等条件有特殊要求。
(2)将各类微生物用____________从斜面培养基接种于灭菌过的 LB 液体培养基
中,进行扩大化培养。
(3)将含有 LB 固体培养基(LB 液体培养基中加 15g 琼脂粉,刚配好,尚未凝固)
的锥形瓶放入____________中进行灭菌。灭菌完成后将锥形瓶取出,待温度下降
到 60℃(不烫手的温度)时,用____________擦拭桌面和双手,在超净工作台中
的____________旁将锥形瓶中的 LB 培养基分装到一系列试管,并做标记。
(4)当试管温度下降到 40 ℃(培养基还是液态)时,用灭菌过的移液器吸取
0.1mL 的各类微生物悬液加入相应试管中并封口,双手快速搓动试管,使菌种均匀
分布于培养基内后迅速将封口的试管放置在___条件下使培养基凝固。
(5)将上述试管放置于常温条件下培养 48 小时后观察实验结果,下图中可表示
制作果酒的菌种的分布图的是____________。
38. [生物—选修 3:现代生物科技专题] (15 分)
根据所学知识回答下列问题:
(1)应用胚胎工程技术可培育出“试管牛”,试管牛的培育需经过体外受精、早期
胚 胎 培 育 以 及 在 母 体 中 发 育 和 产 出 等 过 程 , 胚 胎 工 程 的 最 终 环 节 是
________________。从供体母牛子宫内收集胚胎的方法叫____________,其生理
学基础是______________。
(2)用于核移植的供体细胞一般选用传代 10 代以内的细胞,原因是 10 代以内的
细胞一般能保持______________,可以保证供体细胞正常的遗传基础。
(3)蛋白质工程是通过______________,对______________进行改造,或制造一
种新的蛋白质。蛋白质工程中在获得特定的目的基因后,需要通过______________
技术来生产所需要的蛋白质。
(4)目前蛋白质工程成功的例子不多,主要原因是_____________________。
定远重点中学 2020 届高三下学期 6 月模拟考试
理科综合能力测试
生物答案
1 2 3 4 5 6
C C D A A A
1.C【解析】植物细胞中的液泡是一种细胞器,但其含有的色素与花和果实的颜色
有关,与光合作用无关,A 错误;蔗糖是植物细胞特有的二糖,哺乳动物的细胞
不能合成,B 错误;酵母菌属于真核生物。酵母菌的细胞含有细胞核,核内含有
DNA 和 RNA 两类核酸,C 正确;蓝藻属于原核生物。蓝藻细胞只有核糖体一种
细胞器,无线粒体,D 错误。因此,本题答案选 C。
2.C【解析】由题意可知,细胞周期依赖性蛋白激酶是细胞周期调控的核心物质,
不管是幼年个体还是老年个体内都会进行细胞的分裂,A 错误;酶的活性是受温
度影响的,所以温度的变化会影响一个细胞周期持续时间的长短,B 错误;CDK1
的存在能使细胞分裂顺利完成,故可能与细胞分裂过程中纺锤丝的形成有关,C
正确;各种 CDK 在细胞周期内特定的时间被激活,驱使细胞完成细胞周期,故
能促进癌细胞分裂间期的某些活动,促进癌细胞的增殖,D 错误。
3.D【解析】通过钠钾泵的跨膜运输是需要消耗 ATP 的运输,所以属于主动运输,
A 错误;氧气是有氧呼吸必需之物,ATP 主要是有氧呼吸产生,所以减少神经细
胞的氧气供应,会对该细胞膜上的钠钾泵的工作产生影响,B 错误;神经细胞受到
刺激后,钠离子是通过钠通道蛋白打开而内流,是被动运输,不是通过钠钾泵的
主动运输,C 错误;钠钾泵是逆浓度梯度工作,所以它的工作结果使神经细胞内钾
离子浓度明显高于膜外,而钠离子浓度比膜外低,D 正确。
4.A【解析】肺炎双球菌转化实验包括格里菲斯体内转化实验和艾弗里体外转化实
验,其中格里菲斯体内转化实验证明 S 型细菌中存在某种“转化因子”,能将 R 型
细菌转化为 S 型细菌;艾弗里体外转化实验证明 DNA 是遗传物质。T2 噬菌体侵染
细菌的实验步骤:分别用 35S 或 32P 标记噬菌体→噬菌体与大肠杆菌混合培养→噬
菌体侵染未被标记的细菌→在搅拌器中搅拌,然后离心,检测上清液和沉淀物中
的放射性物质。
格里菲斯的实验结论是 S 型菌体内有“转化因子”,理由是无毒性的 R 型活细菌在
与被杀死的 S 型细菌混合后,转化为有毒性的 S 型活细菌,但是并没有得出转化
因子是 DNA 的结论,A 错误;艾弗里的实验结论是 DNA 是遗传物质,蛋白质等
不是遗传物质,理由是只有 S 型细菌的 DNA 才能使 R 型细菌转化为 S 型细菌,B
正确;蔡斯和赫尔希实验结论是 DNA 是遗传物质,理由是 DNA 是亲子代之间保
持连续的物质,并且还指导了蛋白质的合成,C 正确;科学研究表明,DNA 是主
要的遗传物质,理由是绝大多数生物的遗传物质是 DNA,少数生物(病毒)的遗
传物质是 RNA,D 正确。
5.A【解析】正常情况下,白眼雌蝇 XaXa 与红眼雄蝇 XAY 杂交,后代中雌果蝇应
该为红眼 XAXa,雄果蝇应该为白眼 XaY。出现的白眼雌蝇应该为 XaXaY,不育的
红眼雄蝇应该为 XAO。
白眼雌蝇(XaXa)与红眼雄蝇(XAY)杂交,F1 出现的白眼雌蝇为 XaXaY,
是异常卵细胞(XaXa)和正常精子(Y)结合的结果。不育的红眼雄蝇为 XAO,是
异常卵细胞(O)和正常精子(XA)结合的结果;因此,A 错误,B、C、D 正确。
故选 A。
6.A【解析】植被碳库中的碳主要以有机物的形式存在,其主要去路之一是以食物
的形式流向下一营养级,A 错误;薇甘菊根系密集,增加了土壤孔隙度,使得土
壤氧含量增加,从而使土壤中需氧型微生物的分解作用增强,使得土壤碳储量减
少,B 正确;与薇甘菊未入侵区域相比,薇甘菊重度入侵区域的总有机碳储量约减
少了(215.73-166.70)/215.73=22.7%,正确;随着薇甘菊入侵程度的加剧,凋落
物碳储量显著增加,原因是薇甘菊的入侵导致附主死亡,D 正确。
29.(1)线粒体、叶绿体、细胞质基质 释放 右上 增多
(2)D、H H 是
(3)60
30. (1)基因组在一定时间和空间上程序性表达
(2)蒸馏水 等量一定浓度的乙烯合成抑制剂 C02 浓度 与对照组
(A 组)相比,实验组(B 组)“呼吸峰值”的出现延迟
31. (1)食物链 食物网 猫头鹰 (2)调节生物的种间关系,以维持生
态系统的稳定 物质循环 能量流动 (3)负 >(或大于) (4)
物种多样性
32. (1)代谢过程 基因中脱氧核苷酸(对)的排列顺序不同 (2)9 (3)
纯合的粉花植株和纯合的红花植株 全为粉花植株 (4)选择植株甲和植株
乙杂交产生 F1,再让 F1 随机交配产生 F2,统计 F2 的表现型及比例 F2 的表现型
及比例为红花:粉花:白花=9:3:4,且粉花植株全为雄株
37. (1)水、碳源、氮源 pH、氧气 (2)接种环 (3)高压蒸汽灭菌锅 酒
精 酒精灯火焰 (4)低温 (5)B
38. (1) 胚胎移植 冲卵 早期胚胎未与母体子宫建立组织上的联系,处于游离
状态 (2)正常的二倍体核型 (3)基因修饰或基因合成 现有蛋白质 基因
工程 (4)对大多数蛋白质的高级结构了解还不够
化学答案
7 8 9 10 11 12 13
A B D C C B B
7.A【解析】 A.司母戊鼎的主要成分是青铜,是铜锡合金,故 A 错误;
B.硅是半导体材料,可用于制光电池,故 B 正确;
C.环氧树脂属于高分子化合物,故 C 正确;
D.偏二甲肼-四氧化二氮作燃料,会产生二氧化氮等污染物,发射神舟十一号飞
船所用火箭的燃料是液氧和煤油,产物为二氧化碳和水,燃料毒性小、污染少,
有利于环保,故 D 正确;答案选 A。
8.B【解析】A.由结构可知青蒿素的分子式为 C15H22O5,故 A 错误;B.双氢青
蒿素含-OH,能发生氧化反应、酯化反应,故 B 正确;C.青蒿素不含碳碳双键或
三键,则不能与溴发生加成反应,故 C 错误;D.青蒿素转化为双氢青蒿素,H 原
子数增加,为还原反应,故 D 错误;故选 B。
9.D【解析】A. 氯气和水反应为可逆反应,所以转移的电子数目小于 0.1NA,故 A
错误;
B. 标准状况下,6.72LNO2 的物质的量为 0.3mol,根据反应 3NO2+H2O═2HNO3+NO
可知,0.3mol 二氧化氮完全反应生成 0.1molNO,转移了 0.2mol 电子,转移的电子
数目为 0.2NA,故 B 错误;
C. NaAlO2 水溶液中,除了 NaAlO2 本身,水也含氧原子,故溶液中含有的氧原子
的个数大于 2NA 个,故 C 错误;
D. 14g 由 N2 与 CO 组成的混合气体的物质的量为: 14
28 /
g
g mol =0.5mol,含有 1mol
原子,含有的原子数目为 NA,故 D 正确。故答案选 D。
10.C【解析】A、次氯酸钠水解生成的次氯酸具有强氧化性,能将有机色质漂白褪
色;
B、氯化铜在溶液中水解生成氢氧化铜和氯化氢,加热促进氯化铜水解,生成的氯
化氢易挥发使水解趋于完全生成氢氧化铜;
C、离子反应向着离子浓度减小的方向进行;
D、未反应的氯气对取代反应的产物 HCl 的检验产生干扰。
A 项、次氯酸钠水解生成的次氯酸具有强氧化性,能将有机色质漂白褪色,不能
用 pH 试纸测次氯酸钠溶液的 pH,不能达到实验目的,故 A 错误;
B 项、氯化铜在溶液中水解生成氢氧化铜和氯化氢,加热促进氯化铜水解,生成的
氯化氢易挥发使水解趋于完全生成氢氧化铜,制备无水氯化铜应在 HCl 气流中蒸
发,故 B 错误;
C 项、碘化银和氯化银是同类型的难溶电解质,向浓度相同的银氨溶液中分别加入
相同浓度氯化钠和碘化钠溶液,无白色沉淀生成,有黄色沉淀生成,说明碘化银
溶度积小于氯化银,故 C 正确;
D 项、氯气溶于水也能与硝酸银反应生成白色的氯化银沉淀,未反应的氯气对取
代反应的产物 HCl 的检验产生干扰,不能达到实验目的,故 D 错误。故选 C。
11.C【解析】依题意可知,M 是 NH4HSO3,N 是 NH4HSO4,故元素 R、X、Y、Z
依次为 H、N、O、S,据此分析。
依题意可知,M 是 NH4HSO3,N 是 NH4HSO4,故元素 R、X、Y、Z 依次为 H、N、
O、S。A、H2O 的热稳定性比 NH3 强,选项 A 正确;
B、S2-的半径比 O2-的大,选项 B 项正确;
C、HNO3、H2SO4 均是强酸,但是,HNO2、H2SO3 均是弱酸,选项 C 错误;
D、NH3 和 H2S 可反应生成(NH4)2S、NH4HS 两种盐,选项 D 正确。答案选 C。
12.B【解析】氢气在电极 M 表面失电子转化为氢离子,为电池的负极,碱液室中
的氢氧根离子透过阴离子交换膜,中和正电荷。酸液室中的氢离子透过质子交换
膜,在电极 N 表面得到电子生成氢气,电极 N 为电池的正极,同时,酸液室中的
氯离子透过阴离子交换膜进入碱液室,补充负电荷,据此答题。
A.电极 M 为电池的负极,电子由 M 极经外电路流向 N 极,故 A 错误;
B.酸液室中的氢离子透过质子交换膜,在电极 N 表面得到电子生成氢气,N 电极
区的电极反应式为 2H++2e-=H2↑,故 B 正确;
C.酸液室与碱液室之间为阴离子交换膜,钠离子不能进入碱液室,应在酸液室得到
NaHCO3、Na2CO3,故 C 错误;
D.放电一段时间后,酸液室氢离子被消耗,最终得到 NaHCO3、Na2CO3,溶液 pH
增大,故 D 错误。故选 B。
13.B【解析】微粒的浓度越大,lgc 越大。酸性溶液中 c(CH3COOH)≈0.01mol/L,
lgc(CH3COOH)≈-2,碱性溶液中 c(CH3COO-)≈0.01mol/L,lgc(CH3COO-)≈-2;酸性
越强 lgc(H+)越大、lgc(OH-)越小,碱性越强 lgc(H+)越小、lgc(OH-)越大,根据图象
知,曲线 c 为 CH3COOH,a 为 CH3COO-,b 线表示 H+,d 线表示 OH-。据此分析
解答。
A. 根据上述分析,直线 b、d 分别对应 H+、OH-,故 A 正确;
B. 根据图象,pH=6 时,c(Ac-)>c(HAc)>c(H+),故 B 错误;
C. HAc 电离常数 Ka= ,当 c(CH3COOH)=c(CH3COO-),
Ka=c(H+)=10-4.74,数量级为 10-5,故 C 正确;
D. 曲线 a 与 c 的交点,表示 c(CH3COOH)=c(CH3COO-),根据 C 的分析,
Ka=c(H+)=10-4.74,pKa=-lgKa=-lg c(H+)=pH=4.74,故 D 正确;答案选 B。
26. (1)2Cr2O3+3O2+4Na2CO3 4Na2CrO4+4CO2 (2)CuSO4(或 CuSO4 和
H2SO4) (3)低温条件下,K2Cr2O7 的溶解度在整个体系中最小,且 K2Cr2O7 的溶
解度随温度的降低而显著减小 (4)Cr2
2-
7O +6Fe2++14H+ 2Cr3++6Fe3++7H2O
49.0 (5)是
27. (1)NaCN+H2O2+H2O=NH3↑+NaHCO3 (2)三颈烧瓶 (3)将产
生的氨气及时排出并被吸收,防止产生倒吸,减少发生副反应 (4)AB (5)
滴入最后一滴标准硝酸银溶液,锥形瓶的溶液中恰好产生黄色沉淀,且半分钟内
沉淀不消失 (6)0.49 (7)2HSO4—-2e-=S2O82—+2H+
28. (1)(2a+2b+c)kJ•mol-1 (2)1050K 前反应未达到平衡状态,随着温度
升高,反应速率加快,NO 转化率增大 20% 4 (3)A (4)< 0.25
35. (1)3d54s2 Mn2+ Mn2+价层电子排布为 3d5,3d 能级半充满,更稳定
(2)sp2 直线型 (3)2,4 O>C>H (4)半径 Mg2+