- 849.50 KB
- 2021-07-05 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2019
届高三化学备考的思考
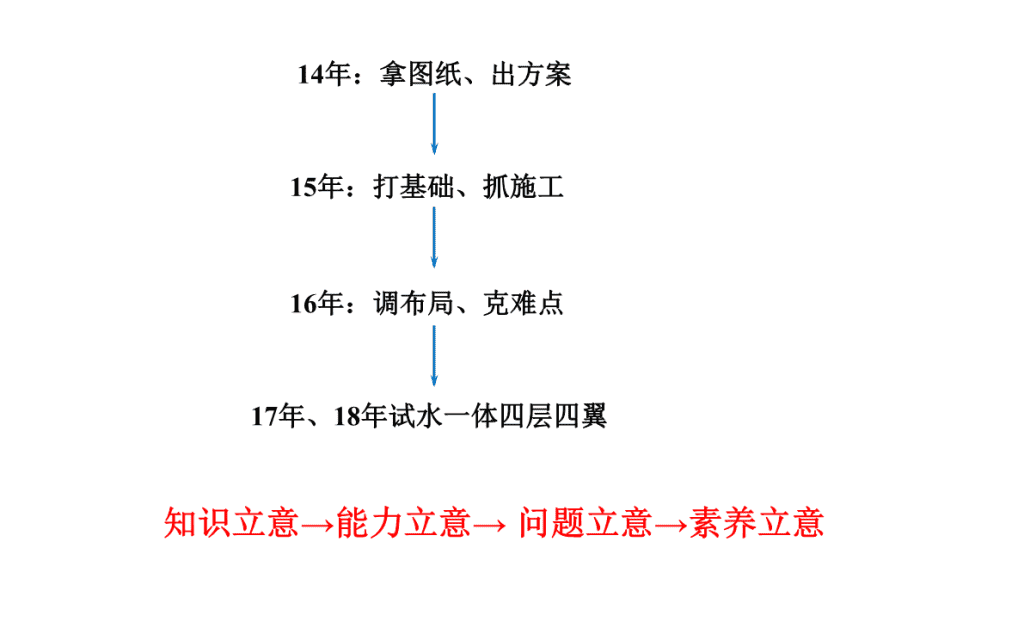
14
年:拿图纸、出方案
15
年:打基础、抓施工
16
年:调布局、克难点
17
年、
18
年
试水一体四层四翼
知识立意→能力立意→ 问题立意→素养立意
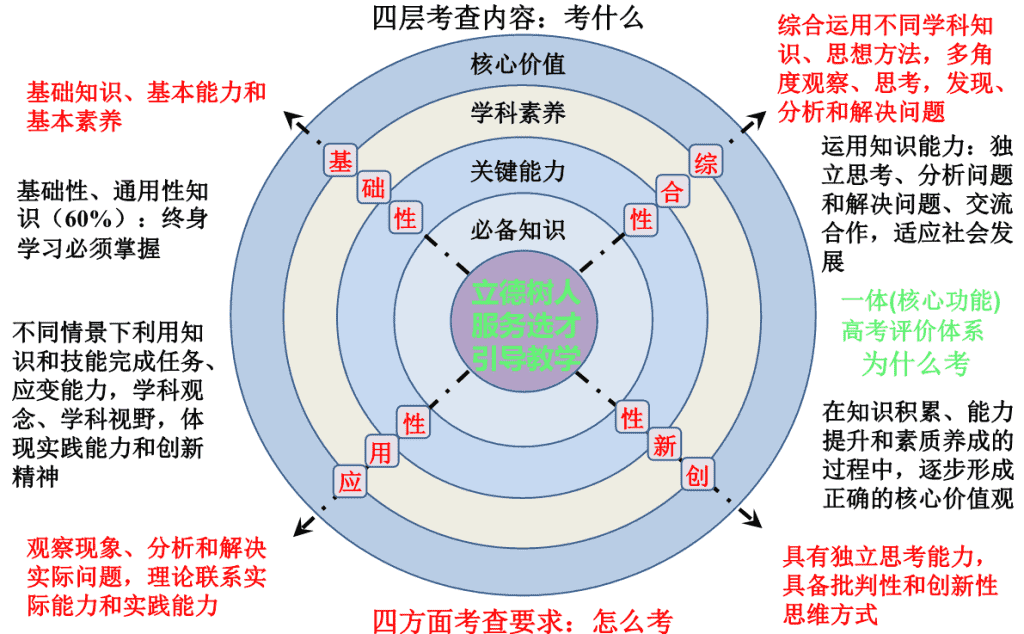
必备知识
关键能力
学科素养
核心价值
立德树人
服务选才
引导教学
基
础
性
性
用
应
性
新
创
综
合
性
一体
(
核心功能
)
高考评价体系
基础性、通用性知识(
60%
):终身学习必须掌握
运用知识能力:独立思考、分析问题和解决问题、交流合作,适应社会发展
不同情景下利用知识和技能完成任务、应变能力,学科观念、学科视野,体现实践能力和创新精神
在知识积累、能力提升和素质养成的过程中,逐步形成正确的核心价值观
基础知识、基本能力和基本素养
观察现象、分析和解决实际问题,理论联系实际能力和实践能力
具有独立思考能力,具备批判性和创新性思维方式
综合运用不同学科知识、思想方法,多角度观察、思考,发现、分析和解决问题
四层考查内容:考什么
为什么考
四方面考查要求:怎么考
17
、
18
年高考试题特点
平稳性:题型设置和考点切入保持平稳,重视核心和主干知识的考查
基础性:试题载体不回避来源于课本,重视元素化合物的载体作用,重视常见有机物考查
创新性:对同一知识体系的考查形式、切入角度进行调整,不回避用旧情景展示新观点
应用性:联系生产生活实际,重视信息整合和应用,重视化学实验
综合性:强调知识迁移,重视探究过程和方法、学科内和学科间的综合
热点性:不回避热点知识的重复和重现
高考题
—《
课标
》
、
《
课本
》
、
《
考纲
》
三位一体
备考
—
全面互动、注重基础、综合提升
原则
—
满足两个需要,科学实用高效
《
考纲
》
的具体要求
历年高考试题的研究及分析
高考需要
还要关注:
学生答题暴露出的问题
复习的整体规划
学生需要
两个需要:
}
预设和生成的统一
(
1
)化学基本
功的
加强(
基本公式掌握
、
基本化学用语使用、基本原理应用
等)(
2
)
审题能力的提升
(抓
住
关键词、句
,提取问题的实质
)
(
3
)计算能力
的提高
(
4
)
说理、解析型问题的解答
(
5
)实验设计思想
的
培养
(
6
)
信息处理及已有知识的准确迁移
这些多为
《
考纲
》
强调的知识和能力,也是学科素养的体现。
学生需要:
明确学生常见问题
(
2013
全国新课标卷
Ⅰ
)
27
.锂离子电池的应用很广,其正极材料可再生利用。某离子电池正极材料有钴酸锂(
LiCoO
2
),导电剂乙炔黑和铝箔等。
充电
时,该锂离子电池负极发生的反应为
6C
+
x
Li
+
+
x
e
-
=Li
x
C
6
。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件为给出)。
(
5
)
充
放
电过程中,发生
LiCoO
2
与
Li
1
-
x
CoO
2
之间的转化,写出放电时电池反应方程式
_____________________
。
原电池:
Li
x
C
6
-
x
e
-
=6C
+
x
Li
+
Li
1
-
x
CoO
2
+
x
e
-
+
x
Li
+
=LiCoO
2
总:
Li
x
C
6
+
Li
1
-
x
CoO
2
=6C
+
LiCoO
2
(-)
(
+
)
如关键字词
锂离子电池本质?
二甲醚直接燃料电池具有启动快、效率高等优点,其
能量密度
高于甲醇直接燃料电池
(5.93
kW
·
h
·
kg-1
)
。若电解质为酸性,二甲醚直接燃料电池的负极反应为
__________________________
,一个二甲醚分子经过电化学氧化,可以产生
___________
个电子的电量;该电池的理论输出电压为
1.20 V
,能量密度
E
=_____________________________
。
(
列式计算。
能量密度
=
电池输出电能
/
燃料质量,
1kW
·
h=3.6×10
6
J
)
。
充分利用单位导出公式
化学核心素养:
1
、宏观辨识和微观探析:结构决定性质、性质决定应用,并能从微观层面解释
2
、变化观念与平衡思想:从分类的角度研究物质变化的多重视角,揭示规律和特征,用动态的观点观察、分析和预测化学反应
3
、证据推理与模型认知:提出问题→做出假设→搜集论据、寻求方法→分析推理→得出结论→优化评价(穿插建模方法、构建思维框架)
4
、实验探究与创新意识:提出问题并能有效解决问题,合作、创新
5
、科学精神与社会责任:化学与生产、生活实际、科技前沿的紧密联系(情感态度价值观)
高考需要
——
内化素养,外显能力
知识立意→能力立意→ 问题立意→素养立意
三轮复习
功能:
整合教材
和
知识,
体现
逻辑性和综合
性
,形成知识体系和网络
,提升知识应用能力。
把握知识的
高度、
难度、广度
、厚度、关联度的
度。穿插两本选修内容,提升答题能力。
关注:
一轮复习和二轮复习的顺畅衔接。
备考无捷径,可以超越
不宜
跨越。
一轮复习
时间:
8
月
—
次年
1
月底
定位:
以章节为主线,形成知识网络和知识体系,知识能力一步到位,滚动复习,不留死角,加强基础训练和条块训练。
效果:
Fe
知识网络
提问:
Fe
元素形成的单质
、
化合物
哪
些有颜色?具体说明并完成各物质间的转化。
(
18
年
7
)
. 硫酸亚铁锂(
LiFePO
4
)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:
下列叙述错误的是
A.
合理处理废旧电池有利于保护环境和资源再利用
B.
从
“
正极片
”
中可回收的金属元素有
Al
、
Fe
、
Li
C.“
沉淀
”
反应的金属离子为
Fe
3+
D
.
上述流程中可用硫酸钠代替碳酸钠
近几年在考:
1
、化学与
STSE
:体现化学对生活、生产、科技等的重要贡献,彰显社会责任
(
18
年
12
)
.
主族元素
W
、
X
、
Y
、
Z
的原子序数依次增加,且均不大于
20
。
W
、
X
、
Z
最外层电子数之和为
10
;
W
与
Y
同族;
W
与
Z
形成的化合物可与浓硫酸反应,其生成物可腐蚀玻璃。下列说法正确的是
A.
常温常压下
X
的单质为气态
B
. Z
的氢化物为离子化合物
C. Y
和
Z
形成的化合物的水溶液呈碱性
D. W
与
Y
具有相同的最高化合价
2
、元素周期律和元素周期表:较好的渗透宏观辨识和微观探析
基本概念和基本理论
(
1
)基本化学用语
包括对元素符号及在周期表中的位置、电子式、微粒结构示意图、比例模型、分子式、结构式和结构简式、化学方程式和离子方程式等
化学用语
的考查,在选择题和非选择题中都可能出现。
基本化学用语要求的调整:
掌握
原子结构示意图、电子式、分子式、结构式和结构简式等表示方法。
3
、有机化学:有机物对人类进步和社会发展的重要作用
(
18
年
8
)
下列说法错误的是
A
.
蔗糖、果糖和麦芽糖均为双糖
B.
多数
酶是一类具有高选择催化性能的蛋白质
C.
植物油含不饱和脂肪酸酯,能使
Br₂/CCl
4
褪色
D.
淀粉和纤维素水解的最终产物均为葡萄糖
(
18
年
11
)
环之间共用一个碳原子的化合物称为螺环化合物,螺
[2
,
2]
戊烷(
)是最简单的一种。下列关于该化合物的说法错误的是
A.
与环戊烯互为同分异构体
B.
二氯代物超过两种
C
.
所有碳原子均处同一平面
D.
生成
1 mol C
5
H
12
至少需要
2 mol H
2
(三)常见有机物
未来可能倾向新材料的多元化考查
。
(
16
年
9
)
.下列关于有机化合物的说法正确的是
A
.
2-
甲基丁烷也称异丁烷
B
.由乙烯生成乙醇属于加成反应
C
.
C
4
H
9
Cl
有
3
种同分异构体
D
.油脂和蛋白质都属于高分子化合物
(
2
)了解有机化合物的同分异构现象,
增加:
能正确书写简单有机化合物的同分异构体。
(
3
)
掌握
常见
(原来为“上述”)
有机反应类型。
(
4
)了解甲烷、乙烯、苯等有机物的主要性质和
(增加“应用”)
(
5
)了解氯乙烯、苯的衍生物等在化工生产中的
重要作用。
基本营养物质和高分子化合物是否予以更多的关注?
4
、电化学:立足应用和创新,凸显关键能力
(
18
年
13
)
最近我国科学家设计了一种
CO
2
+H
2
S
协同转化装置,实现对天然气中
CO
2
和
H
2
S
的高效去除。示意图如图所示,其中电极分别为
ZnO@
石墨烯(石墨烯包裹的
ZnO
)和石墨烯,石墨烯电极区发生反应为:
①
EDTA-Fe
2+
-
e
-
=
EDTA-Fe
3+
②
2EDTA-Fe
3+
+H
2
S
=
2H
+
+S+2EDTA-Fe
2+
该装置工作时,下列叙述错误的是
A.
阴极的电极反应:
CO
2
+2H
+
+2e
-
=
CO+H
2
O
B.
协同转化总反应:
CO
2
+H
2
S
=
CO+H
2
O+S
C
.
石墨烯上的电势比
ZnO@
石墨烯上的低
D.
若采用
Fe
3+
/Fe
2+
取代
EDTA-Fe
3+
/EDTA-Fe
2+
,
溶液需为酸性
5
、基本实验:突出学科观念、学科视野、学科素养,培养科学精神和创新意识
(
18
年
9
)
在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是
D
说明:
关于
N
A
的
计算和判断
是常考题型之一,是对基本知识的综合考查。
6
、
N
A
:很好的补点题
(
18
年
10
)
N
A
是阿伏加德罗常数的值,下列说法正确的是
A. 16.25 g FeCl
3
水解形成的
Fe(OH)
3
胶体粒子数为
0.1
N
A
B
. 22.4 L
(标准状况)
氩
气含有的质子数为
18
N
A
C. 92.0 g
甘油(丙三醇)中含有羟基数为
1.0
N
A
D. 1.0 mol CH
4
与
Cl
2
在光照下反应生成的
CH
3
Cl
分子数为
1.0
N
A
说明:
重视课本知识及迁移、拓展;
重视元素化合物的载体作用;
重视联系实际;
17
年、
18
年全面试水“一体、四层、四翼”:
试题载体来源:
试题评价:
平稳性、传承性、热点性、创新性
改变:
②
在解决化学问题的过程中,运用化学原理和科学方法,能设计合理方案,初步实践科学探究。
增加:
1.
化学学科特点和基本研究方法
(
4
)了解定量研究方法是化学发展为一门科学的重要标志。
关注计算、数据处理、定量实验
(
3
)化学实验与探究能力
① 了解并初步实践化学实验研究的一般过程,
掌握
化学实验的
基本方法和技能。
(一轮复习)
② 在解决简单化学问题的过程中,运用
科学的方法
,初步了解
化学变化规律
,并对
化学现象
提出科学合理的
解释
。 (二轮复习)
变化:
1
、加大计算考查力度
了解物质的量(
n
)及其单位摩尔(
mol
)
、摩尔质量(
M
)、气体摩尔体积(
V
m
)、
物质的量浓度(
c
)、阿伏加德罗常数(
N
A
)
的含义。
了解溶液浓度的表示方法。
理解溶液中溶质的质量分数
和物质的量浓度的概念
,
并能进行有关计算。
2
、重视必备知识考查:
掌握
原子结构示意图、电子式、分子式、结构式和结构简式等表示方法。
增加:
掌握常见氧化还原反应的配平和相关计算
增加:
了解胶体是一种常见的分散系,
了解胶体和溶液的区别
了解常见金属及其重要化合物的
制备方法,掌握
其主要性质及其应用。
关注生产实际中的元素化合物,重视实验和实践关系。
增加:
了解共价键的形成、极性;了解氢键的含义。
三点变四点:
4
.
晶体结构与性质
(
1
)了解晶体的类型,了解不同类型晶体中结构微粒、微粒间作用力的区别。
(
2
)了解晶格能的概念,了解晶格能对离子晶体性质的影响。
(
3
)了解分子晶体结构与性质的关系。
(
4
)了解原子晶体的特征,能描述金刚石、二氧化硅等原子晶体的结构与性质的关系。
(
5
)理解金属键的含义,能用金属键理论解释金属的一些物理性质。了解金属晶体常见的堆积方式。
(
6
)了解晶胞的概念,能根据晶胞确定晶体的组成并进行相关的计算。
三道必做主观题
总体来看:
必做的大题重综合性,重能力,重过程方法,重应用,渗透科技前沿和情感态度价值观,且题型基本固定,一个综合探究实验题;一个无机综合题,主要形式是以生产实际为背景,以元素化合物为载体综合考查无机化学知识,并渗入溶液中离子平衡的知识,拼盘式设问形式居多;一个化学原理综合题,涉及考点主要为速率和平衡,反应机理,离子平衡,盖斯定律,电化学等,常有新信息呈现。
(
1
)侧重
创新
,重视
信息
与已有知识的
整合
题材新,背景新,信息新,试题呈现形式新(启普发生器),评价体系新,更
多的考查学生挖掘、整合、应用
信息解决新问题
的水平,体现现场学习的水平和创新精神;同时兼顾已有知识的呈现、迁移和应用,使题目更有内涵,更能体现学科本源。
综合实验题
(
2
)重视
考查能力
、重视
过程和方法
、重视
学科素养
重基础的同时重能力, 分析问题和解决问题的能力,预测实验现象和结论,设计和评价实验方案,重视基本操作及操作过程中的论述、解释和说理,重视实践能力,重视数据处理和误差分析,重视学科素养,重视科学精神和社会责任等核心价值。
无机综合题的形式和特点
随着新课标高考命题改革的深入,无机综合题内容更加丰富。以多元化主题研究和工艺流程为主,进行多角度考查,加大了逻辑性和综合性,拼盘形式设问居多。因此此类题的解法需重点突破。
(
1
)化学反应与热量:反应热的含义(三种反应热的表示方式及⊿
H
的符号判断、含义),大小比较及计算,燃烧热和中和热,盖斯定律的应用,热化学方程式的书写和计算、判断等。关注反应机理和历程。
(
2
)化学反应速率:反应速率的比较和计算,影响因素(内因、外因
—
浓度、压强、温度、催化剂、比表面积)。
化学反应原理综合题常见考点
(
3
)化学平衡:化学平衡常数表达式,与平衡常数有关的计算,判断影响平衡常数的因素,化学平衡状态的判断,用化学平衡的影响因素进行
分析和解释
,等效平衡(转化率、浓度的比较),反应热与等效平衡的融合,正逆反应速率与平衡的关系等。
(
4
)电化学基础:原电池和电解池的电极名称,电极反应式和总式的书写,溶液中离子的移动方向,以各电极电子转移总数相等为核心的计算,离子浓度和溶液
pH
的计算等。
关注学科间的综合和膜技术。
(
5
)水溶液中的离子平衡:
K
w
、电离平衡常数、溶度积常数、
pH
的应用和有关计算,盐溶液酸碱性和典型试纸的使用,溶液中各类离子方程式的书写并用来进行相关事实的解释,粒子浓度大小的比较,水和弱电解质的电离平衡、沉淀溶解平衡的判断、应用及有关计算等。
(
6
)化学反应速率、化学平衡
新课标高考对此内容的考查情有独钟,主要以判断、推理、计算等形式出现。从知识内容来看主要有以下几个方面:
①化学反应速率的影响因素、计算、测定方法及数据处理;
②化学平衡状态的判断;
③有关化学反应速率、化学平衡图像的分析和判断;
④有关化学平衡及常数的计算及影响因素;
⑤结合着等效平衡,进行有关物理量的比较;
⑥化学平衡与反应热的交叉;
⑦化学反应进行的方向判定;
⑧运用化学反应速率和化学平衡知识解释实际问题等。
⑨新视角下关于化学反应速率和化学平衡的考查,增大信息量。
定位:
以专题模块为主线,构架知识网络和知识体系,知识点全覆盖,加强综合训练。
二轮复习
时间:
大约两个半月
功能:
专题是有明确目的、明确任务、明确内容的专项综合训练,着重体现“专”字。旨在强化重点、突破难点、总结规律、归纳方法、体现思维过程,则要求训练中,将难度、高度、广度、深度提升到极致。
二轮复习承载的责任和功能更大。二轮复习的效果可能直接决定着一个考生高考的成败。
三轮复习:
以重点知识和主干知识为主线,强化知识网络和知识体系,回归课本,地毯式搜索,查缺补漏,加强模拟性综合训练。
强调解决综合题的方法:分解、拆分、迁移、整合综合题
回归课本不忽略边缘知识:
如:新型材料、金属材料、高分子化合物;油脂、糖类、蛋白质等基本营养物质;金属冶炼;海水资源的综合应用;煤和石油;熵变;环保;危险品标志;检验
Fe
2
+
。
有关有机物同分异构体的书写
前边简单提到过,再详细说一下,同分异构体书写主要有
几
个角度:
组合型:
主要指酯类,只要按要求分别写出组成酯的两部分(醇或酚、酸)的同分异构体,再进行组合即可,不要忽略了酯基有方向性以及
H
原子连接位置的特殊要求;如
13
年新课标卷Ⅰ的
12
题。
脂肪型:
也即链状,烷烃是母体,可先写等碳原子(官能团中不含
C
)或少一个碳原子(官能团中含有
C
)的烷烃的同分异构体,再结合对称原则找不等价
H
,依次用官能团分别取代。如链状有机物
C
4
H
6
Cl
2
的同分异构体的书写:先写
4
个碳原子的烷烃同分异构(有
2
种),再分别上 双键(共
3
种),再分别用一个氯原子取代各个烯烃中的
H
原子,最后再上一个氯原子,结束。
芳香
型
:
含有苯环的同分异构体主要考查苯环的对称性,可先苯环上连两个取代基,均为邻、间、对三种,再根据对称原则,一个一个上其他取代基。如用—
X
、—
Y
、—
Z
取代苯环上
H
,可先上任意两个,再上第三个;若多取代基,其中有相同的,可先上相同的,后边更容易找对称。
多苯环连接,可先找不等价碳,再依据对称原则书写。