- 285.00 KB
- 2021-07-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
化学试题
可能用到的相对原子质量:H-1 O-16 S-32 Ca-40 Cu-64
一.选择题(每小题只有一个正确答案,共24×2=48分)
1.下列变化中,一定不存在化学能与热能相互转化的是 ( )
A.铝热反应 B.金属钝化 C.燃放爆竹 D.干冰气化
2.冰融化为水的过程的焓变和熵变正确的是( )
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S>0 D.△H<0,△S<0
3.与盐类水解无关的化学应用是 ( )
A.明矾用于净水 B.氯化铁溶液腐蚀铜板
C.热的纯碱溶液洗涤除去油污 D.草木灰不能与铵态氮肥混合使用
4.将①H+、②Cl-、③Al3+、④K+、⑤S2-、⑥OH-、⑦NO3-、⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的离子是( )
A.①③⑤⑦⑧ B.②④⑥⑧ C.①⑥ D.②④⑦
5.下列不能用平衡移动原理解释的是( )
A.新制氯水中加入CaCO3固体可增大HClO分子的浓度
B.钢铁在潮湿的空气中比在干燥空气中更容易生锈
C.通入过量的空气与SO2反应可以提高SO2的利用率
D.由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
6.在空气中直接蒸发下列盐的溶液:①Al2(SO4)3 ②NaAlO2 ③KAl(SO4)2 ④NaClO ⑤NaHCO3,可以得到相应盐的晶体(可以含有结晶水)的是( )
A.①③⑤ B.①②③ C.②④ D.①③④⑤
7.某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)Z(g)+W(s)
ΔH>0。下列叙述正确的是( )
A.加入少量W,逆反应速率增大,正反应速率减小
B.升高温度,平衡逆向移动
C.当容器中气体压强不变时,反应达到平衡
D.反应平衡后加入X,上述反应的ΔH增大
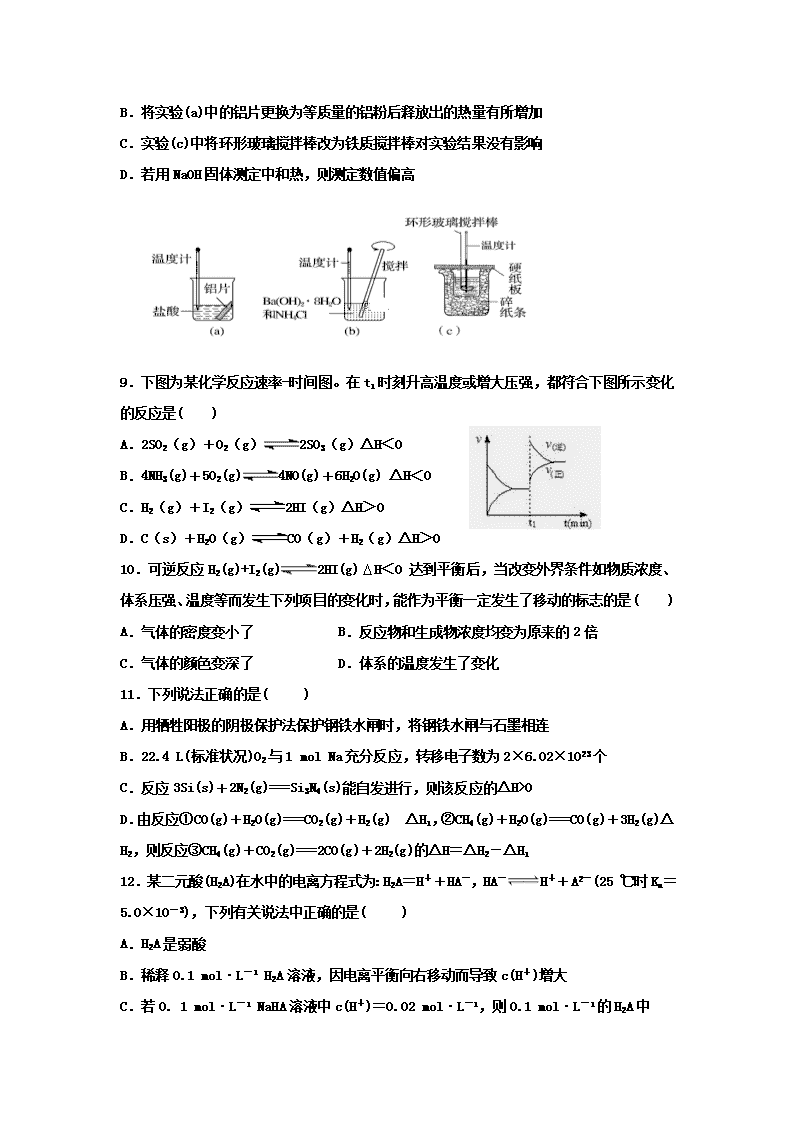
8.某同学设计如图所示实验,探究反应中的能量变化,下列判断正确的是( )
A.由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应
B.将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C.实验(c)中将环形玻璃搅拌棒改为铁质搅拌棒对实验结果没有影响
D.若用NaOH固体测定中和热,则测定数值偏高
9.下图为某化学反应速率-时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是( )
A.2SO2(g)+O2(g)2SO3(g)△H<0
B.4NH3(g)+5O2(g)4NO(g)+6H2O(g) △H<0
C.H2(g)+I2(g)2HI(g)△H>0
D.C(s)+H2O(g)CO(g)+H2(g)△H>0
10.可逆反应H2(g)+I2(g)2HI(g)H<0 达到平衡后,当改变外界条件如物质浓度、体系压强、温度等而发生下列项目的变化时,能作为平衡一定发生了移动的标志的是( )
A.气体的密度变小了 B.反应物和生成物浓度均变为原来的2倍
C.气体的颜色变深了 D.体系的温度发生了变化
11.下列说法正确的是( )
A.用牺牲阳极的阴极保护法保护钢铁水闸时,将钢铁水闸与石墨相连
B.22.4 L(标准状况)O2与1 mol Na充分反应,转移电子数为2×6.02×1023个
C.反应3Si(s)+2N2(g)===Si3N4(s)能自发进行,则该反应的ΔH>0
D.由反应①CO(g)+H2O(g)===CO2(g)+H2(g) ΔH1,②CH4(g)+H2O(g)===CO(g)+3H2(g)ΔH2,则反应③CH4(g)+CO2(g)===2CO(g)+2H2(g)的ΔH=ΔH2-ΔH1
12.某二元酸(H2A)在水中的电离方程式为:H2A=H++HA-,HA-H++A2-(25 ℃时Ka=5.0×10-3),下列有关说法中正确的是( )
A.H2A是弱酸
B.稀释0.1 mol·L-1 H2A溶液,因电离平衡向右移动而导致c(H+)增大
C.若0. 1 mol·L-1 NaHA溶液中c(H+)=0.02 mol·L-1,则0.1 mol·L-1的H2A中
c(H+)<0.12 mol·L-1
D.在0.1 mol·L-1的H2A溶液中,c(H+)=0.12 mol·L-1
13.等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
A.平衡常数K值越大,X的转化率越大
B.达到平衡时,反应速率v正(X)=2v逆(Z)
C.达到平衡后降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
D.达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
14.在一定体积的密闭容器中放入3L气体R和5L气体Q,在一定条件下发生反应:2R(g)+5Q(g)⇌4X(g)+nY(g)。反应完全后,容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中的n值是( )
A.2 B.3 C.4 D.5
15. 以铅蓄电池为电源,石墨为电极电解CuSO4溶液(足量),装置如下图。若一段时间后Y电极上有6.4 g红色物质析出,停止电解。下列说法正确的是( )
A.a为铅蓄电池的负极
B.电解过程中SO42-向右侧移动
C.电解结束时,左侧溶液质量增重8 g
D.铅蓄电池工作时正极电极反应式为:PbSO4+2e-===Pb+SO42-
16.下列叙述正确的是( )
A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42-
B.往等c(H+)和等体积的盐酸和醋酸中,分别加足量相同的锌片,相同状况下,与醋酸反应产生的气体体积更大
C.已知H2CO3 的 Ka1= 4.30×10-7,Ka2= 5.61×10-11,HClO的 Ka = 3.0×10-8,则反应CO2+H2O+2NaClO=Na2CO3+2HClO能够成立
D.等c (H+)的盐酸和醋酸,加水稀释100倍后,c(H+)前者大于后者
17.关于浓度均为0.1mol·L-1的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是( )
A.c(NH4+):③>①
B.水电离出的c(H+):③>②>①
C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O)
D.①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
18.下列叙述正确的是( )
A.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH增大
B.pH均为3的盐酸和醋酸,分别加水稀释至原溶液体积的1 000倍,所得溶液的pH均等于6
C.等浓度等体积的醋酸和NaOH溶液反应,溶液呈中性
D.室温时pH=3硫酸和pH=11的氨水等体积混合后,溶液呈中性
19.化学家正在研究尿素动力燃料电池,尿液也能发电。用这种电池直接去除城市废水中的尿素,既能产生净化的水,又能发电,尿素燃料电池结构如图所示,下列有关描述正确的是( )
A.电池工作时H+移向负极
B.该电池用的电解质溶液是KOH溶液
C.甲电极反应式:CO(NH2)2+H2O+6e-===CO2+N2+6H+
D.电池工作时,理论上每净化1 mol CO(NH2)2,消耗标况下氧气33.6 L O2
20.常温下,下列各组离子在指定环境中能大量共存的是( )
A.在=1013的溶液中:NH4+、Ca2+、Cl-、K+
B.由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、HCO3-、Cl-、K+
C.无色溶液中可能大量存在Al3+、NH4+、Cl-、S2-
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO42-
21.下列溶液中各微粒的浓度关系正确的是( )
A.0.1 mol·L-1NaHSO4溶液中:c(Na+)>c(SO42-)>c(H+) >c(OH-)
B.0.1 mol·L-1Na2S溶液中:2 c(Na+)=c(S2-)+c(HS-)+c(H2S)
C.0.1 mol·L-1NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
D.等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后:C(Na+)=c(CH3COO-)>c(H+)=c(OH-)
22.已知25℃时有关弱酸的电离平衡常数K1(H2Y)>K(HX)>K2(H2Y),则下列叙述不正确的是( )
A.物质的量浓度相同时,各溶液的pH关系为pH(Na2Y)>pH(NaX)>pH(NaHY)
B.a mol/L HX溶液与b mol/L NaOH溶液等体积混合,所得溶液中c(Na+)>c(X-),则不一定ac(OH—) >c(CH3COO—) >c(H+)
C.点①和点②所示溶液中都有: c(CH3COO—)-c(CN—) = c(HCN)- c(CH3COOH)
D.点②和点③所示溶液中都有:c(CH3COO—)+c(OH—)= c(CH3COOH) +c(H+)
二.非选择题(共52分)
25.(14分)
Ⅰ.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:①CO2(g)+3H2(g)CH3OH(g)+H2O (g) △H1;
②CO(g)+2H2(g)CH3OH(g) △H2
③CO2(g)+H2(g)CO(g)+H2O(g) △H3;
化学键
H-H
C-O
CO
H-O
C-H
E/(kJ·mol-1)
436
343
1076
465
X
回答下列问题:
(1)已知△H2=-99 kJ·mol-1,则根据上表相关的化学键键能(“CO”表示CO的化学键)计算X=_______ kJ·mol-1。
(2)反应①、②、③对应的平衡常数K1、K2、K3之间的关系式为___________。
(3)根据化学反应原理,分析增大压强对反应③的影响为_______________。(提示:从对反应速率、平衡状态、转化率角度回答)
Ⅱ.清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池。一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)CH3OH(g)△H=-99kJ•mol-1。向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:
①Ⅱ和Ⅰ相比,改变的反应条件是_________;
②反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)=_________;
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=_________;
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1_____T3(填“>”“<”“=”)
26.(9分)
电离平衡常数是衡量弱电解质电离程度的物理量。
已知:
化学式
电离常数(25 ℃)
HCN
K=4.9×10-10
CH3COOH
K=1.8×10-5
H2CO3
K1=4.3×10-7、K2=5.6×10-11
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为________(用化学式表示)。
(2)向NaCN溶液中通入少量的CO2,发生反应的化学方程式__________________。
(3)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=________ mol·L-1(填精确值),=_____。
27.(16分)
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H=—1214 kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H= —566kJ/mol
则表示甲烷燃烧热的热化学方程式____________________________________________。
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)CO(g)+3H2(g)
①一定条件下CH4的平衡转化率与温度、压强的关系如图,则Pl_________P2;A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为___________(填“<”、“>”“=”)
②100℃时,将1mol CH4和2mol H2O通入容积为10L的反应室,反应达平衡的标志是:_______
a.容器的压强恒定 b.单位时间内消耗0.1mol CH4同时生成0.3mol H2
c.容器内气体密度恒定 d.3v(CH4)=v(H2)
e. 容器内气体平均相对分子质量恒定
(3)已知2H2(g)+CO(g)CH3OH(g)△H=-akJ•mol-1(a>0),在一个容积固定的容器中加入2mol H2和1mol CO,在500℃时充分反应,达平衡后CH3OH的浓度为W mol•L-1。反应平衡后,若向原来容器中再加入2mol H2和1mol CO,500℃充分反应再次达平衡后,则CH3OH浓度___________2Wmol•L-1(填“>”、“<”或“=”)。
(4)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图所示的电池装置,
①负极的电极反应式为___________,
②用该原电池做电源,用惰性电极电解200mL饱和食盐水(足量),消耗标准状况下的CO 224mL,则溶液的pH=___________
28.(13分)
滴定法是解决化学分析问题的常用方法。滴定的方法有酸碱中和滴定、氧化还原滴定、沉淀滴定、络合滴定等。
I.如图为某浓度的NaOH溶液滴定10.00mL一定浓度的盐酸的示意图。根据图像分析:
(1)HCl溶液的浓度是__________;NaOH溶液的浓度是_______;
(2)若向20mL稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是________(填字母)。
П.氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。
(3)人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度,抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。滴定的实验数据如下所示:
实验编号
待测血液的体积/mL
滴入KMnO4溶液的体积/mL
1
20.00
11.95
2
20.00
13.00
3
20.00
12.05
①滴定时,盛放高锰酸钾溶液的仪器名称为_________确定反应达到终点的现象_____________。
②草酸跟酸性KMnO4溶液反应的离子方程式为:2MnO42-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,根据所给数据计算血液样品中Ca2+离子的浓度为__________mg/cm3
化学答案
1.D 2.A 3.B 4.D 5.B 6.B 7.C 8.D 9.B 10.D 11.D 12.C
13.A 14.A 15.C 16.B 17.B 18.A 19.D 20.A 21.C 22.C
23.B 24.C
25.(14分)
Ⅰ.(1)413
(1) K1=K2·K3(或者K3=K1/K2)
(2) 增大压强,反应速率加快,平衡不移动,反应物的转化率不变
Ⅱ①使用催化剂
② 0.125 mol/(L·min)
③ 12 ④ >
26.(9分)
I.(1)Na2CO3>NaCN>CH3COONa
(2)NaCN+H2O+CO2=HCN+NaHCO3
(3)9.9×10-7 18
27.(16分)
(1)CH4(g)+2O2(g)CO2(g)+2H2O(l) △H=-890kJ.mol-1
(2)①< KC>KB>KA ②ae
(3)>
(4)① CO-2e-+4OH-=CO32-+2H2O ②13
28.(13分)
I. (1)0.10mol/L 0.050mol/L (2)B
П.(3)①酸式滴定管
滴入最后一滴高锰酸钾溶液,溶液紫色不在褪去(溶液由无色变为浅紫色),且半分钟内无变化
②1.2mg/cm3