- 5.13 MB
- 2021-07-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
27题之无机物定性定量推断
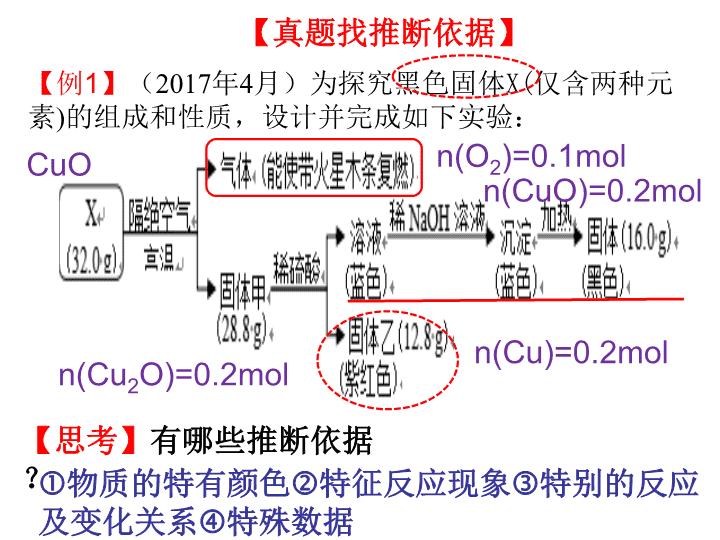
【真题找推断依据】
【例
1
】
(
2017
年
4
月)为探究黑色固体
X(
仅含两种元素
)
的组成和性质,设计并完成如下实验:
【思考】
有哪些推断依据?
n(Cu)=0.2mol
n(CuO)=0.2mol
n(Cu
2
O)=0.2mol
n(O
2
)=0.1mol
CuO
物质的特有颜色
特征反应现象
特别的反应
及变化关系
特殊数据
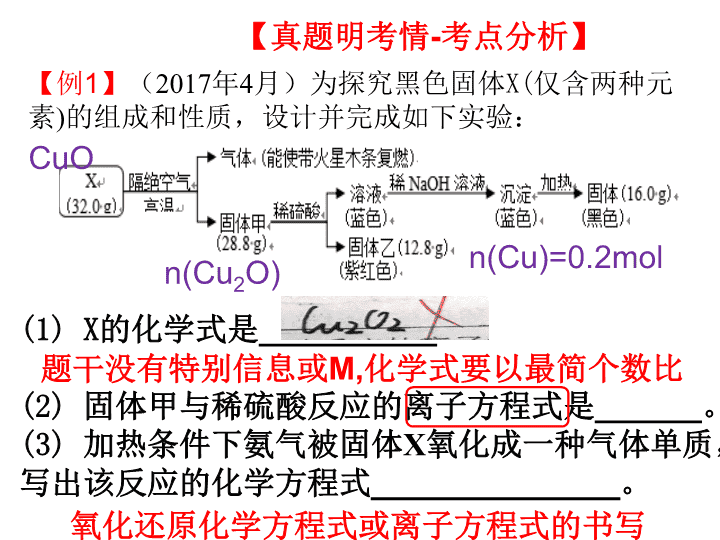
【真题明考情
-
考点分析】
【例
1
】
(
2017
年
4
月)为探究黑色固体
X(
仅含两种元素
)
的组成和性质,设计并完成如下实验:
n(Cu)=0.2mol
n(Cu
2
O)
CuO
(1) X
的化学式是
__________
(2)
固体甲与稀硫酸反应的离子方程式是
______
。
(3)
加热条件下氨气被固体
X
氧化成一种气体单质,写出该反应的化学方程式
______________
。
题干没有特别信息或
M,
化学式要以最简个数比
氧化还原化学方程式或离子方程式的书写
【例
2
】
(
2017
年
11
月)已知固体
Na
2
SO
3
受热易分解,实验流程和结果如下:
气体
Y
是一种纯净物,在标准状况下的密度为
1.518g
·
L
-
1
(
1
)气体
Y
分子的电子式
_______
,
(
2
)该流程中的
Na
2
SO
3
受热分解的化学方程式
____________________________________
。
(
3
)另取固体
X
试样和
Na
2
SO
3
混合,加水溶解后与稀盐酸反应,有淡黄色沉淀产生,写出产生淡黄色沉淀的离子方程式
___________________________________
。
写出
H
2
O
2
N
2
H
4
的电子式
2S
2-
+SO
3
2-
+6H
+
=3S↓
+3H
2
O
【归纳】熟悉常见物质的摩尔质量
【例
3
】
(2018
年
4
月
)
某同学用含
结晶水的正盐
X(
四种短
周期元素组成的纯净物
)
进行了如下实验:
实验中观测到:混合气甲呈无色并被蒸馏水全部吸收;固体
乙为纯净物
;在步骤
③
中,
取
1/
10
溶液丙
,恰好中和需消耗
0.00200 mol NaOH
;另取一定量的溶液丙,加入少量
K
2
FeO
4
固体,产生
黄绿色
气体。
n(HCl)=0.02mol
n(H
2
O)=0.05mol
(1) X
的化学式是
__
,步骤
①
的化学方程式是
__________
。
(2)
溶液丙与
K
2
FeO
4
固体反应的化学方程式是
_
。
n(MgO)=0.01mol
2K
2
FeO
4
+
16HCl=4KCl
+
2FeCl
3
+
3Cl
2
↑
+
8H
2
O
【考点归纳】
根据题给信息定性和定量结合推
断元素化合物的组成。
(1)电子式、结构(简)式等化学用语规范书写。
(2)化学方程式的书写技能:电离方程式、水解方程式、电极方程式、结合信息分析推理陌生反应的化学(离子)反应方程式;
(
3
)常见物质(离子)的检验方法,实验方案设
计及现象描述、结论分析。
熟记钠镁铁铜及其化合物的性质及主要用途,碳、氮、氧、硅、硫、氯等非金属及其化合物的相互转化关系。
黄色固体
蓝色沉淀
淡黄色固体
蓝色晶体
红色固体
浅绿色溶液
紫黑色固体
紫色溶液
红棕色粉末
棕黄色溶液
黑色粉末
血红色溶液
红褐色沉淀
红棕色气体
白色沉淀
黄绿色气体
Cl
2
AgI
, FeS
2
S
、
Na
2
O
2
、
AgBr
Cu
、
Cu
2
O
KMnO
4
、
I
2
Fe
2
O
3
MnO
2
、
Fe
3
O
4
、
CuO
、
C
Fe(OH)
3
BaSO
4
、
BaCO
3
、
CaCO
3
、
AgCl
、
Cu(OH)
2
CuSO
4
Fe
2+
MnO
4
-
Fe
3+
Fe(SCN)
3
NO
2
7
物质推断解题突破口之
物质特有的颜色
某化合物甲是制备负载型催化剂的主要原料。经组成分析化合物
甲中含有四种元素
。
气体混合物乙仅含两种元素,由丁和戊组成,其中丁占总体积的
2/3
,
密度为
1.25g
·
L
-
1
。戊能使澄清石灰水变浑浊。
n(CO)=0.06mol
n(CO
2
)=0.03mol
m(
气
)=3.00g
n(Fe
2
O
3
)=0.01mol
m(K
2
CO
3
)=4.14g
n(K
2
CO
3
)=0.03mol
(1)
化合物甲的化学式________
K
3
[Fe(C
2
O
4
)
3
]
或
K
3
FeC
6
O
12
(2)
加热化合物甲使其完全分解的化学方程式为
__________________________________________
。
2K
3
[Fe(C
2
O
4
)
3
]
=
3K
2
CO
3
+
Fe
2
O
3
+
6CO
+
3CO
2
;
5
题
为探究含结晶水的化合物
X(
含四种元素,摩尔质量为
180 g·mol
-
1
)
的组成和性质,某兴趣小组设计并完成如图所示实验:
n(FeO)=0.15mol
n(CO
2
)=0.15mol
n(CO)=0.15mol
FeC
2
O
4
2H
2
O
n(H
2
O)=0.3mol
1
.
(2018·
浙江金华一中月考
)
某研究小组为了探究一种浅绿色盐
X[
仅含四种元素,不含结晶水,
M
(X)
<
908 g·mol
-
1
]
的组成和性质,设计并完成了如下实验:
取一定量的浅绿色盐
X
进行上述实验,充分反应后得到
23.3 g
白色沉淀
E
、
28.8 g
红色固体
G
和
12.8 g
红色固体
H
。
①
浅绿色盐
X
在
570
℃
、隔绝空气条件下受热分解为非氧化还原反应;
②
常温下
B
呈液态且
1
个
B
分子含有
10
个电子
。
n(SO
3
)=0.1mol
n(Cu
2
O)=0.2mol
第
2
题和讲义第五题
2
、特征反应现象
【讲义
4
】
为探究无机盐
X
(仅含
三种短周期元素
)的组成和性质,设计并完成如下实验:请回答:
n(SiO
2
)=0.03mol
n(Mg(OH)
2
)
=0.06mol
(
3
)高温条件下白色粉末与焦炭发生置换反应,写出该反应的化学方程式
______
SiO
2
+2C==Si+2CO
高温
注意几个特殊的置换反应:
(
2
)金属
→
非金属
(
3
)非金属
→
非金属
(
4
)非金属
→
金属
(
1
)金属
→
金属
既能跟酸反应又能跟碱反应且生成气体的物质是
Al
、
NH
4
HCO
3
、
(NH
4
)
2
CO
3
【讲义
7
】
某研究小组为了探究仅一种白色粉末状固体
X(
仅含四种元素
)
的组成和性质,称取
6.3g
固体
X
,设计并完成了如下实验:
n(NH
3
)=0.1mol
n(CO
2
)=0.1mol
n(Cu
2
O)=0.1mol
HCOONa
物质推断中新型方程式书写
(
1
)某短周期元素组成的金属氢化物可与水反应产生氢气和能溶于
NaOH
的白色沉淀,写出该
金属氢化物与水
反应的化学方程式
。
(
2
)已知:
NH
2
Cl
与水可以微弱地反应产生具有漂白性的物质,因而
NH
2
Cl
具有消毒时间长等优点,写出该反应的化学方程式
。
(
3
)在空气中直接加热
CuCl
2
•2H
2
O
晶体得不到纯的无水
CuCl
2
,原因是
。(用化学方程式表示)
例
1
例
2
(
1
)以
KI
作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下
KI
与氧气反应的化学方程式
。
(
2
)在通气良好的土壤中,土壤中
NH
4
+
的氧化途径之一是在硝酸细菌作用下完成,写出反应的离子方程式
。
(
3
)工业上一般采用电解(惰性电极)
K
2
MnO
4
溶液制
KMnO
4
,写出电解总反应方程式
。