- 1.01 MB
- 2021-07-07 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
选考题型突破系列
(
六
)
元素周期表和元素周期律
(
选择题
)
【
题型特点
】
该题型是高考的热点题型
,
命题落点是借助元素周期表的片段
(
某一部分
)
推断元素
,
然后利用“位
—
构
—
性”关系综合考查元素及化合物性质和化学反应原理的相关内容。
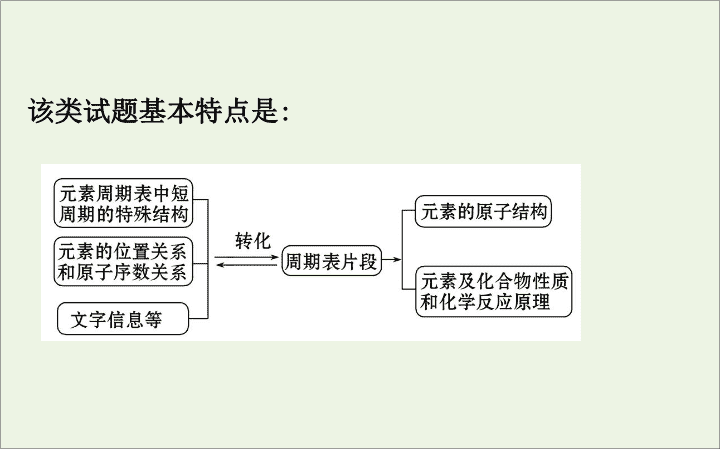
该类试题基本特点是
:
即在实际考查中只呈现元素周期表的某一片段
,
根据呈现的片段结构中提供的信息推断元素
,
推出元素在周期表中的位置
,
就可以快速确定元素的名称、原子结构及相关性质。
【
典题示例
】
【
典例
】
W
、
X
、
Y
、
Z
四种短周期元素
,
它们在周期表中的位置如图所示
,
下列说法不正确的是
(
)
A.Z
、
Y
、
X
的原子半径依次减小
,
非金属性依次降低
B.Z
、
Y
、
W
的最高价氧化物对应水化物的酸性依次降低
C.WH
4
与
Z
元素的单质在一定条件下可发生化学反应
D.W
的位置是第
2
周期、第
ⅣA
族
【
解题思路
】
(1)
依据周期表的片段及题干信息明确四种元素均为短周期元素及其种类。
(2)
由元素在周期表中的位置明确原子半径的相对大小。
(3)
元素的非金属性强弱确定其相应最高价氧化物对应的水化物的酸性强弱。
【
解析
】
选
A
。根据元素在元素周期表中的位置可知
,W
是
C
、
X
是
O
、
Y
是
S
、
Z
是
Cl
。元素周期表中左下角元素
的原子半径大
,
所以原子半径
Y>Z>X,
右上角元素的非金
属性强
,
则非金属性
X(O)>Z(Cl)>Y(S),A
选项错误
;
元素
的非金属性越强
,
其最高价氧化物对应水化物的酸性越
强
,
即
Z>Y>W,B
选项正确
;WH
4
为
CH
4
,Z
元素的单质是
Cl
2
,
CH
4
和
Cl
2
在光照条件下能够发生取代反应
,C
选项正确
;W
是碳元素
,
处于元素周期表中的第
2
周期第
ⅣA
族
,D
选项正确。
【
类题通法
】
步骤
1:
分析题目有效信息。
(1)
图表信息
——
题中直接给出的周期表片段
;
(2)
文字信息
——
把题中给出的文字信息提炼
;
(3)
结构信息
——
题中给出的原子结构信息如微粒的质子数或电子数等。
步骤
2:
画出元素周期表片段
,
明确各元素的相对位置
,
推出元素。
步骤
3:
对照问题
,
根据元素周期律回答相应问题。
(1)
元素性质
:
原子半径、主要化合价、金属性和非金属性及其递变规律
;
(2)
单质及化合物性质
:
颜色、状态、熔沸点
,
气态氢化物的稳定性
,
最高价氧化物对应的水化物的酸碱性
;
(3)
化学键类型、化合物类型、电子式等。
【
类题试解
】
1.
如图为元素周期表中短周期的一部分
,
四种元素中只有一种是金属
,
下列说法不正确的是
(
)
A.W
的氢化物比
R
的氢化物稳定
B.T
的最高价氧化物对应的水化物可能为强碱
C.Q
的原子半径比
T
的小
D.W
和
Q
的原子序数相差
10
【
解析
】
选
B
。由图可知
T
为铝元素
,
结合位置可知
,Q
为碳元素
,R
为磷元素
,W
为硫元素。非金属性
S>P,W
的氢化物比
R
的氢化物稳定
,A
正确
;T
的最高价氧化物对应的水化物为氢氧化铝
,
为两性氢氧化物
,
属于弱碱
,B
错误
;
电子层越多
,
原子半径越大
,
则
Q
的原子半径比
T
的小
,C
正确
;W
和
Q
的原子序数分别为
16
、
6,
原子序数之差为
10,D
正确。
2.W
、
X
、
Y
、
Z
、
M
、
N
六种主族元素
,
它们在周期表中位置如图所示
,
其中
Y
最外层电子数是次外层的一半
,
下列说法正确的是 世纪金榜导学号
(
)
W
X
Y
Z
M
N
A.
原子半径
:Y>X>W
B.
单质的氧化性
:Z>M
C.
气态氢化物的稳定性
:M>X
D.
根据元素周期律
,
可以推断
N
元素的单质可作半导体材料
【
解析
】
选
D
。同周期从左到右
,
元素的原子半径逐渐减小
;
同主族从上到下
,
元素的原子半径逐渐增大
;
同周期从左到右
,
非金属元素单质的氧化性逐渐增强
;
同主族从上到下
,
元素的非金属性逐渐减弱
,
气态氢化物的稳定性逐渐减弱
,A
、
B
、
C
项错误
;
元素
N
为第
ⅣA
族的锗元素
,
位于金属和非金属的分界线附近
,
其单质可作半导体材料
,D
项正确。
3.
短周期元素
X
、
Y
、
Z
、
W
在周期表中相对位置如表所示
,Y
元素在地壳中的含量最高。下列说法正确的是
(
)
X
Y
Z
W
A.
原子半径
:Z