- 156.00 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
化学试卷
可能用到的原子量:H 1 O 16 C 12 N14 Na 23 Mg 24 S 32 Fe 56
一、 选择题(每题只有1个正确答案,每题3分,共60分)
1、与其危险化学品图形标志不一致的一组是( )
A.烧碱——1 B.甲烷——2 C.酒精——3 D.白磷——4
2、下列生产、生活、实验中的行为,符合安全要求的是 ( )
A.点燃打火机,可以检验液化气钢瓶口是否漏气
B.进入煤矿井下作业,戴上安全帽,用帽上的矿灯照明
C.节日期间,可以在热闹繁华的商场里燃放烟花爆竹,欢庆节日
D.实验室里,可以将水倒入浓硫酸及时用玻璃棒搅拌,配制稀硫酸
3、下列操作正确的是( )
A.过滤时用玻璃棒搅拌漏斗内的液体,以加速过滤
B.蒸发到析出晶体时才需要用玻璃棒搅拌
C.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
D.分液时,分液漏斗中下层液体从上口倒出,上层液体应从下口流出
4、己知乙酸异戊酯是难溶于水且密度比水小的液体。在洗涤、分液操作中,应充分振荡,然后静置,待分层后的操作是 ( )
A.直接将乙酸异戊酯从分液漏斗的上口倒出
B.直接将乙酸异戊酯从分液漏斗的下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
5、已知甲和乙的某些性质如下表所示:
物质
熔点(℃)
沸点(℃)
密度(g·mL-1)
溶解性
甲
-98
37.5
0.93
可溶
乙
-48
95
0.90
可溶
现有甲和乙的混合物,进行分离时,可采用的方法是( )
A.蒸馏 B.蒸发 C.过滤 D.萃取
6、现有三组溶液:①汽油和海水 ②体积分数为35%的醋酸溶液 ③单质碘的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
7、下列实验仪器用于加热时,通常需要垫上石棉网的是( )
A.试管 B.坩埚 C.蒸发皿 D.烧杯
8、NA 为阿伏伽德罗常数,下列说法错误的是( )
A.6.02×1023 个铜原子的质量为64g
B. 25℃,1.01×105Pa,64gSO2中含有的原子数为3NA
C.常温常压下,48g O3 所含的原子数为NA
D. 18g水所含的质子数为10NA
9、下列叙述正确的是( )
A.标准状况下,1mol任何物质的体积都约为22.4L
B.1mol H2和O2 的混合气体所含原子总数为2NA
C.常温常压下,11.2L N2 含有的分子数为NA
D.标准状况下,18g水所占的体积约为22.4L
10、下列叙述正确的是:( )
A.1mol水的质量为18g•mol-1 B.阿伏伽德罗常数个钠原子的质量为23g
C.1g H2 和1g N2 所含分子数相等 D.氢氧化钠的摩尔质量是40g
11、下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5mol NH3 ②标准状况下22.4L He ③4℃ 9mL 水 ④0.2mol H3PO4
A.①④③② B.④③②① C.②③④① D.①③④②
12、5.4 g M和16.0 g N恰好完全反应,生成0.2 mol X和10.2 g Y,则X的摩尔质量为( )
A.28 g·mol-1 B.56 g·mol-1 C.84 g·mol-1 D.112 g·mol-1
13、实验是化学研究的基础,关于下列各实验装置的叙述中,错误的是( )
A.装置①可用于分离煤油和水 B.装置②可用于准确称取8.55 g氯化钠固体
C.装置③可用于从海水中得到淡水 D.装置④可用于排空气收集CO2
14、科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3 和H2相同的是( )
A.原子数 B.分子数 C.体积 D.物质的量
15、两份质量相同的CH4和NH3比较,下列结论错误的是( )
A.分子个数比为17∶16 B.同温同压下两种气体的体积之比是17∶16
C.氢原子个数比为17∶12 D.原子个数比为17∶16
16、在标准状况下,由0.5 g H2、11 g CO2和4 g O2组成的混合气体,其体积约为( )
A. 8.4 L B. 11.2 L C. 14.0 L D. 16.8 L
17、在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体。在同温同压下,两容器内的气体一定具有相同的( )
A.原子数 B.密度 C.质量 D.质子数
18、不用其他试剂,用最简单的方法鉴别下列物质:
①NaOH溶液,②Mg(NO3)2溶液,③CuSO4溶液,④KCl溶液,正确的鉴别顺序是( )
A.①②③④ B.③④②① C.④①②③ D.③①②④
19、 (18分)
(1)等物质的量的SO2和SO3中,氧原子的个数比为 ,当SO2和SO3中氧原子个数比为1:1时二者的物质的量之比为_____质量比为_______原子个数比为_______。
(2)含有3.01×1023个氢原子的硫酸的物质的量为 ,与其含有相同氧原子的水的质量为 g。
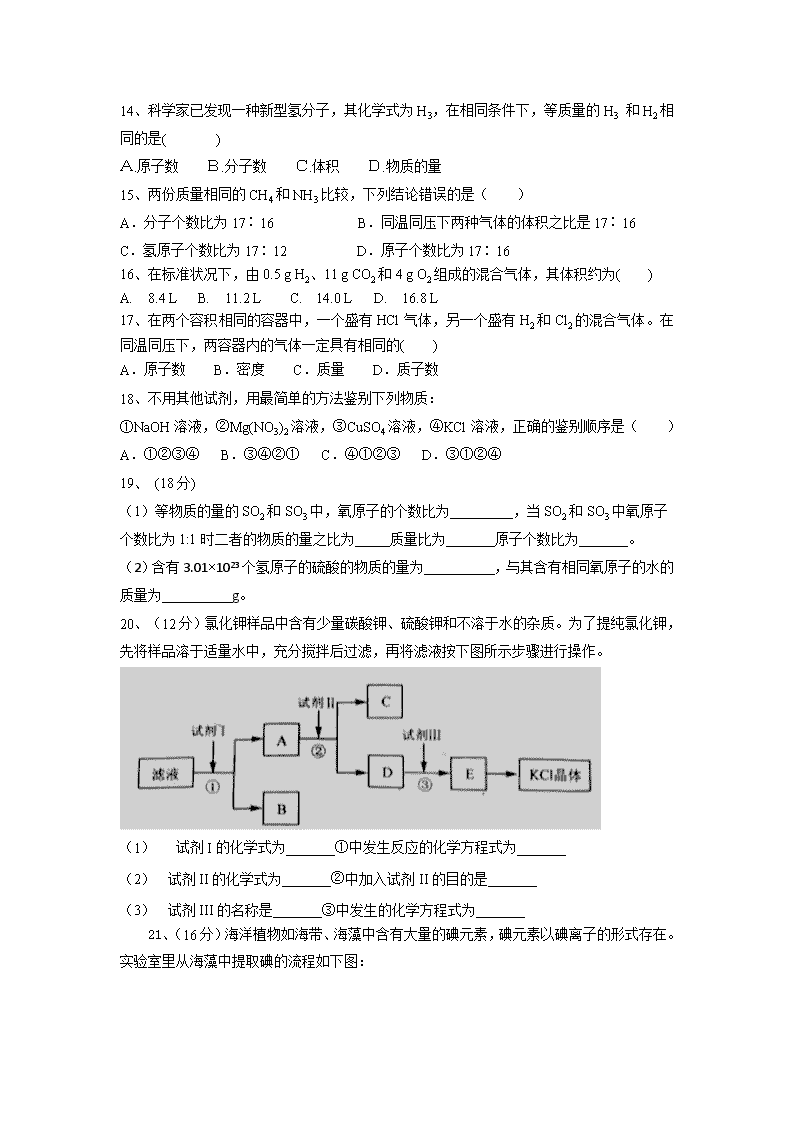
20、(12分)氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
(1) 试剂I的化学式为_______①中发生反应的化学方程式为_______
(2) 试剂II的化学式为_______②中加入试剂II的目的是_______
(3) 试剂III的名称是_______③中发生的化学方程式为_______
21、(16分)海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
(1)实验室焙烧海带,需要下列仪器中的_______________(填序号)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)提取碘的过程中有关的实验操作名称:①_______________,③_______________。
⑶提取碘的过程中,不能选择乙醇作有机萃取剂的原因是________________________。
(4)第③步时使用的主要玻璃仪器有_______________________。
(5)小组用CCl4萃取碘水中的碘,在右图的分液漏斗中,下层液体呈______色;他们打开分液漏斗活塞,却未见液体流下,原因可能是______________________________________________________________。
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
①______________________________________;
②_______________________________________。
(7)进行上述蒸馏操作时,使用水浴加热的原因是________________________________,最后晶态碘在蒸馏烧瓶里聚集。证明得到的固体是碘单质的化学方法是________________。
化学答案
1
2
3
4
5
6
7
8
9
10
A
B
C
D
A
C
D
C
B
B
11
12
13
14
15
16
17
18
A
B
B
A
D
C
A
D
19.(18分)
(1)2:3 3:2 6:5 9:8
(2)0.25mol 18
20.(12分)
(1)BaCl2、 BaCl2+K2SO4==BaSO4↓+2KCl、 BaCl2+K2CO3==BaCO3↓+2KCl
(2)K2CO3、除去过量的Ba2+
(3)盐酸、2HCl+K2CO3==2KCl+H2O+CO2↑
21.(16分)
(1)cdef(2分)(2)过滤(1分),萃取、分液(1分)
(3)乙醇与水以任意比例互溶,所得到的碘的酒精溶液无法与水分离(2分)
(4)分液漏斗,烧杯(2分)
(5)紫或紫红(1分),分液漏斗上口玻璃塞未打开(1分)(6)缺石棉网(1分),温度计插到了液体中(1分)
(7)使蒸馏烧瓶受热均匀,控制加热温度不至过高(2分);取得到的固体少许,将其加入到淀粉溶液中,淀粉溶液变蓝,即可证明所得固体为碘单质(其他合理方法也可)(2分)