- 10.05 MB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
北京市朝阳区 2020 年高三年级学业水平等级性考试练习二
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Fe 56
第一部分
每小题只有一个选项符合题意,每小题 3 分,共 14 道小题,共 42 分。
1.(2020 年北京朝阳 6 月)下列防护隔离、杀菌消毒等措施中,没有..应用蛋白质变性原理
的是( )
A.佩戴医用口罩 B.蒸煮餐具 C.紫外线杀菌 D.碘伏清洗伤口
2.(2020 年北京朝阳 6 月)正确应用物质性质并规范操作是保障安全的前提。下列做法不.
正确..的是( )
A.工业上金属钠残渣用乙醇进行处理
B.苯酚不慎沾到皮肤上,用氢氧化钠溶液擦拭
C.大量氯气泄漏时,戴好防毒面具,喷稀碱液进行吸收
D.向电石上滴加饱和食盐水,将产生的气体验纯后点燃,观察燃烧现象
3.(2020 年北京朝阳 6 月)下列变化中,与氧化还原反应无关..的是( )
A.向 Na2CO3 溶液中滴入 1~2 滴酚酞溶液,溶液呈红色
B.向 K2Cr2O7 酸性溶液中滴加乙醇,溶液由橙色变为绿色
C.向碘水中滴加维生素 C 溶液,溶液棕黄色褪去
D.向 FeSO4 溶液中滴加 NaOH 溶液,生成白色沉淀后迅速变为灰绿色,最后呈红褐色
4.(2020 年北京朝阳 6 月)用 NA 代表阿伏伽德罗常数的数值。下列说法正确的是( )
A.1mol 氨基含有的电子数为 10 NA
B.标准状况下,22.4 L O2 完全转化为 Na2O2 时转移的电子数为 4 NA
C.56 g C3H6 和 C4H8 的混合气体中含有的氢原子数为 8 NA
D.0.1 mol·L-1 CH3COONa 溶液中 CH3COO-、CH3COOH 数目之和为 0.1 NA
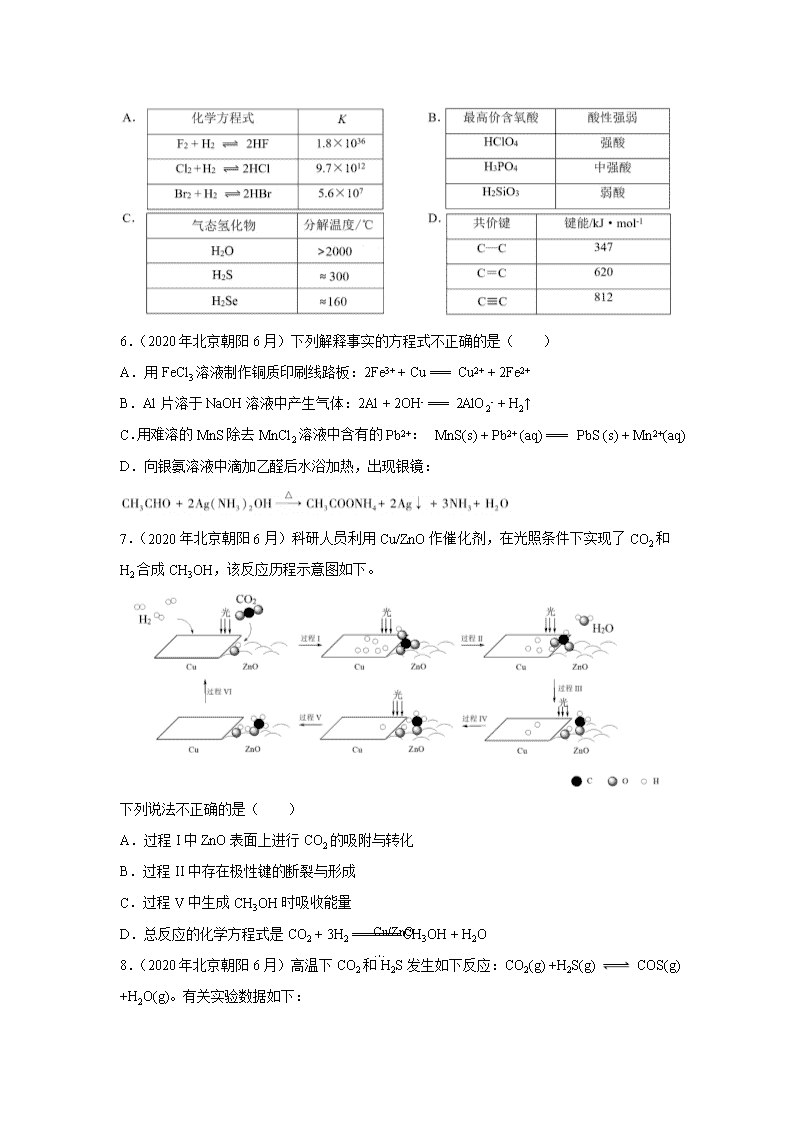
5.(2020 年北京朝阳 6 月)下列数据或事实所呈现的规律不能..用元素周期律解释的是( )
6.(2020 年北京朝阳 6 月)下列解释事实的方程式不正确...的是( )
A.用 FeCl3 溶液制作铜质印刷线路板:2Fe3+ + Cu === Cu2+ + 2Fe2+
B.Al 片溶于 NaOH 溶液中产生气体:2Al + 2OH- === 2AlO2- + H2↑
C.用难溶的 MnS 除去 MnCl2 溶液中含有的 Pb2+: MnS(s) + Pb2+ (aq) === PbS (s) + Mn2+(aq)
D.向银氨溶液中滴加乙醛后水浴加热,出现银镜:
7.(2020 年北京朝阳 6 月)科研人员利用 Cu/ZnO 作催化剂,在光照条件下实现了 CO2 和
H2 合成 CH3OH,该反应历程示意图如下。
下列说法不正确...的是( )
A.过程 I 中 ZnO 表面上进行 CO2 的吸附与转化
B.过程 II 中存在极性键的断裂与形成
C.过程 V 中生成 CH3OH 时吸收能量
D.总反应的化学方程式是 CO2 + 3H2 ====== CH3OH + H2O
8.(2020 年北京朝阳 6 月)高温下 CO2 和 H2S 发生如下反应:CO2(g) +H2S(g) COS(g)
+H2O(g)。有关实验数据如下:
Cu/ZnO
光
实验 温度
物质的起始物质的量/(mol) 平衡时 COS 物质的量/(mol)
n(CO2) n(H2S ) n(COS)
Ⅰ 337℃ 0.10 0.40 0.01
Ⅱ 347℃ 0.10 0.40 0.015
下列说法不正确...的是( )
A.该反应为吸热反应
B.实验Ⅰ达平衡后 COS 的物质的量分数为 5%
C.实验Ⅰ温度下,反应的平衡常数为
D . 平 衡 后 向 Ⅱ 中 再 充 入 0.10 mol CO2 和 0.40 mol H2S , 相 同 温 度 下 再 达 平 衡 时
n(COS)=0.03mol
9.(2020 年北京朝阳 6 月)用如图所示的装置进行实验(夹持及尾气处理仪器略去),能达到
实验目的的是( )
选项 a 中试剂 b 中试剂 c 中试剂 实验目的 装置
A 氨水 CaO 无 制取并收集氨气
B 浓盐酸 MnO2 饱和 NaCl 溶液 制备纯净的 Cl2
C 浓盐酸 Na2CO3 Na2SiO3 溶液
比较酸性强弱:
H2CO3>H2SiO3
D 浓硫酸 Na2SO3
KMnO4 酸性溶
液
验证 SO2 具有还
原性
10.(2020 年北京朝阳 6 月)漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为 Ca(ClO)2,
相应的生产流程如下。
下列说法不正确...的是 ( )
A.①中阳极的电极反应式为 2Cl- - 2e- ===Cl2↑
B.②中反应的化学方程式为 2Cl2 + 2Ca(OH)2 === Ca(ClO)2 + CaCl2 +2H2O
C.上述过程涉及氧化还原反应、化合反应、复分解反应
D.制备漂粉精过程中,Cl2 转化为 Ca(ClO)2 时,Cl 的原子利用率为 100%
11.(2020 年北京朝阳 6 月)尿素( )氮原子上的氢原子可以像苯酚分子中苯环上
的氢原子那样与甲醛发生反应,生成交联脲醛树脂,其结构片段如下图所示(图中 表
示链延长)。
下列说法不正确...的是 ( )
A.尿素可以与甲醛发生加成反应生成
B.脲醛树脂的合成反应为缩聚反应
C.交联脲醛树脂在一定条件下可以发生水解反应,重新生成尿素和甲醛
D.甲醛可以与 交联成网状结构的脲醛树脂
12.(2020 年北京朝阳 6 月)研究人员采用双极膜将酸-碱电解液隔离,实现 MnO2 / Mn2+和
Zn / Zn(OH)42-的两个溶解/沉积电极氧化还原反应,研制出新型高比能液流电池,其放电过
程原理示意图如下:
下列说法不正确...的是( )
A.放电过程中,总反应方程式为 Zn + MnO2 + 4OH- + 4H+ ===Zn(OH)42- + Mn2++2H2O
B.放电过程中,当 1 mol Zn 参与反应时,理论上有 4 mol K+ 发生迁移
C.充电过程中,阴极的电极反应为 Zn(OH)42- + 2e- ===Zn + 4OH-
D.充电过程中,右侧池中溶液 pH 逐渐减小
13.(2020 年北京朝阳 6 月)已知 Na2CO3 与稀盐酸反应分两步进行:CO2-
3 +H+==HCO-
3 ,
HCO-
3 +H+== CO2↑+H2O。向 10.00 mL 0.1000 mol·L-1 Na2CO3 溶液中滴加 0.1000 mol·L-1 盐
酸,溶液 pH 随盐酸体积的变化如图。
下列说法不正确...的是( )
A.V = 5.00mL 时,溶液中 c(HCO-
3 )>c(CO2-
3 )>c(OH-)>c(H+)
B.V =10.00mL 时,溶液中 c(Na+)=c(HCO-
3 )+c(CO2-
3 )+c(H2CO3)+c(Cl-)
C.a 点的溶液中:2n(CO2-
3 )+n(HCO-
3 ) = 0.001 mol
D.V = 20.00mL 时,溶液 pH<7,是因为 H2CO3 HCO3- + H+
14.(2020 年北京朝阳 6 月)研究金属钠的性质,实验如下:
实验装置
实验方案
液体 a 现象
蒸馏水 Ⅰ.钠浮在水面,剧烈反应,有少量白雾
0.1 mol·L-1 盐酸 Ⅱ.钠浮在液面,反应比Ⅰ剧烈,有白雾产生
浓盐酸
Ⅲ.钠浮在液面,反应比Ⅰ缓慢,产生大量白
雾,烧杯底部有白色固体
下列说法不正确...的是( )
A.Ⅱ中反应的离子方程式为 2Na + 2H+ === 2Na+ + H2↑
B.对比Ⅰ、Ⅱ、Ⅲ可知,随着 c(H+) 增大,反应的剧烈程度增大
C.实验Ⅰ、Ⅱ、Ⅲ均有白雾产生,说明 Na 与水或酸反应均放出大量热
D.推测Ⅲ中浓盐酸的 c(Cl-)以及生成的 NaCl 固体对反应剧烈程度有影响
第二部分
本部分共 5 题,共 58 分。
15.(8 分)(2020 年北京朝阳 6 月)近年来,FePO4 作为制备锂离子电池正极材料 LiFePO4
的重要原料而成为研究热点。一种以 FeCl3、H3PO4、氨水为主要原料制备 FePO4 的流程如
下图。
已知:H3PO4 是弱电解质
(1)将 FeCl3 溶液与 H3PO4 溶液按 3 3 4FeCl : H PO 1:1n n 混合,没有明显现象,逐渐
滴加氨水至 pH = 1.5 左右,生成 FePO4·2H2O 沉淀。
①操作 a 为_______________。
②生成 FePO4·2H2O 的离子方程式是_______________________________________。
③ 控制氨水用量,避免因 pH 偏高而产生_________杂质。
(2)测定产物样品中铁元素的质量分数,主要步骤如下:
ⅰ.取 a g 样品,加入过量盐酸充分溶解,再滴加 SnCl2(还原剂)至溶液呈浅黄色;
ⅱ.加入 TiCl3,恰好将 i 中残余的少量 Fe3+还原为 Fe2+;
ⅲ.用 c mol·L–1 K2Cr2O7 标准溶液滴定 Fe2+,消耗 v mLK2Cr2O7 标准溶液。
①将步骤ⅲ的离子方程式补充完整:
② 产物中铁元素的质量分数为________。
16.(10 分)(2020 年北京朝阳 6 月)尿素 2 2CO NH 是一种重要的化工产品,工业生产
尿素的主要流程如下:
NH3(g)和CO2(g) 合成尿素
粗尿素
除去杂质
尿素产品
(1)工业合成氨的化学方程式是__________________________________。
(2)尿素分子中 C、N 原子间的共用电子对偏向 N 原子,从原子结构的角度解释原
因:__________________________________________。
(3)由 NH3 和 CO2 合成尿素分为两步反应(均为可逆反应),其能量变化示意图如下:
1 合成尿素总反应的热化学方程式是________________________________________。
② 粗尿素中含有 NH2COONH4 杂质。通过控制温度和压强,可将 NH2COONH4 分解为 NH3
和 CO2。研究温度和压强对 NH2COONH4 分解率的影响,结果如下:
N
H
2
C
O
O
N
H
4
分
解
率
/
%
X 代表_____(填“温度”或“压强”),L1_____L2(填“>”或“<”)。
(4)工业上含尿素的废水需经处理后才能排放。一种利用电化学方法降解尿素的装置示意
图如下:
写出尿素被降解的电极反应式是_____________________________________________。
17.(14 分)(2020 年北京朝阳 6 月)中药黄芩的有效成分之一——汉黄芩素具有抗病毒、
抗肿瘤作用。合成汉黄芩素的中间体 M 的路线如下:
(1)A 属于芳香烃,A 的名称是_______________。
(2)由 A 生成 B 的化学方程式是___________________________________________。
(3)D 中含有的官能团是_________________。
(4)E 的结构简式是______________________。
(5)K 与 X 在一定条件下转化为 L, X 的分子式是 C4H8O2。
① 有机物 X 的结构简式是_______________。
② 符合下列条件的 K 的同分异构体有_____种。
a.含有苯环,能与 NaHCO3 反应生成 CO2
b.苯环上的一氯代物有两种
(6)F 与 L 合成 M 的步骤如下:
中间产物 1 和中间产物 2 的结构简式分别是________、________。
18.(12 分)(2020 年北京朝阳 6 月)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用
空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。
(1)柴油中含有多种烷烃,其燃烧性能用十六烷值表示。C16H34 完全燃烧的化学方程式是
__________________________________________。
(2)柴油发动机工作时在稀燃(O2 充足、柴油较少)和富燃(O2 不足、柴油较多)条
件下交替进行,催化转化装置中的物质变化如下图所示。
1 BaO 吸收 NO2 的化学方程式是____________________________________。
② 富燃条件下 Pt 表面反应的化学方程式是____________________________________。
(3)研究 CO2 对 BaO 吸收氮氧化物的影响,一定温度下,测得气体中 CO2 的体积分数与
氮氧化物吸收率的关系如下图所示。
①一定范围内,氮氧化物吸收率随 CO2 体积分数的增大而下降,原因是
____________________________________________。
②当 CO2 体积分数达到 10%~20%时,氮氧化物吸收率依然较高,原因可能有:
________________________________________________。
③若柴油中硫含量较高,在稀燃过程中,BaO 吸收氮氧化物的能力下降至很低水平,结合
化学方程式解释原因:______________________________________________________。
19.(14 分)(2020 年北京朝阳 6 月)化学小组探究铜与硝酸反应的快慢及产物。
(1)实验甲:将铜片放入盛有稀 HNO3 的试管中,开始无明显现象,渐有小气泡生成,该
气体是___________。液面上方出现浅红棕色气体,溶液呈蓝色。
(2)实验乙: 铜与浓 HNO3 反应,装置、现象如下:
实验装置 实验现象
A 中:最初反应较慢,随后加快,反应剧烈;
产生红棕色气体;溶液呈绿色。
B 中:溶液呈淡蓝色。
1 A 中铜与浓 HNO3 产生红棕色气体的化学方程式是______________________________。
② 实验现象“最初反应较慢,随后加快”的原因可能是______________________________。
(3)有文献记载:铜与浓 HNO3 反应一旦发生就变快,是因为开始生成的 NO2 溶于水形成
HNO2(弱酸,不稳定),它再和 Cu 反应,反应就加快。实验探究如下:
Ⅰ:向 1 mL 浓硝酸中加入几滴 30% H2O2 溶液、铜片,反应较慢,溶液呈蓝色。
Ⅱ:向 1 mL 浓硝酸中加入几滴 30% H2O2 溶液,无明显变化。
1 Ⅰ中反应变慢的原因是_____________________________________________。
2 NO2 与 H2O 反应生成 HNO2 和_________。
③ 对生成 HNO2 后反应变快的原因进行实验探究。
序号 实验操作 实验现象
Ⅲ
取 B 中溶液,加入一定量 固
体,再加入铜片
立即产生无色气体;液面上方呈
红棕色
Ⅳ
取 B 中溶液,放置一段时间,溶
液变为无色后,再加入铜片
产生无色气体,较Ⅲ慢;液面上
方呈浅红棕色
a.Ⅲ中加入的固体为_______________。
b.Ⅳ中“放置一段时间”的目的是__________________________________________。
实验Ⅲ、可以说明,HNO2 氧化 Cu 的反应速率比 HNO3 氧化 Cu 的反应快。
(4)化学小组同学结合实验甲、乙中 HNO3 被还原后的气体产物以及实验Ⅲ的产物,综合
上述实验,分析判断甲中反应慢的原因,除了硝酸起始浓度小、反应过程中温度较低外,另
一个重要原因是___________________________________________________。
【参考答案】
第一部分
每小题只有一个选项符合题意。14 个小题,每小题 3 分,共 42 分
题号 1 2 3 4 5 6 7 8 9 10
答案 A B A C D B C B D D
题号 11 12 13 14
答案 C B C B
第二部分
15.(8 分)
(1)① 过滤
②
③ Fe(OH)3
(2)① 1 ;6 ;14H+ ;2 ;6 ; 7H2O ②
16.(10 分)
(1) N2 + 3H2 2NH3
(2)N 和 C 电子层数相同,核电荷数 N>C,原子半径 N<C,原子核吸引电子能力 N>C
(3)① CO2(g) + 2NH3(g) CO(NH2)2(l) + H2O(l) ΔH = –101.5 kJ·mol-1
② 压强 ; <
(4)CO(NH2)2 + 8OH– – 6e– === CO32– + N2↑ + 6H2O
17.(14 分)
(1)甲苯 (2)
(3)—COOH、—NO2 (或羧基、硝基) (4)
(5)① CH3COOCH2CH3 ② 4
(6) ;
18.(12 分)
(1)2 C16H34 + 49 O2 32CO2 + 34 H2O
(2)① 2BaO + 4NO2 + O2 ===2Ba(NO3)2 ②
(3)① BaO 与 CO2 反应生成 BaCO3,覆盖在 BaO 表面
② BaCO3 在一定程度上也能吸收 NOx(其他答案合理给分)
③ 稀燃过程中,柴油中的硫氧化为 SO2,2BaO + 2SO2 + O2 ===2BaSO4 ,BaSO4 稳定,不
易分解,也难与 NOx 反应(其他答案合理给分)
19.(14 分)
(1)NO
(2)① Cu + 4HNO3 (浓)===Cu(NO3)2 + 2NO2↑+ 2H2O
② 反应放热,随着反应的进行,体系温度升高(其他答案合理给分)
(3)① H2O2 与 HNO2 发生反应使 HNO2 浓度降低 ② HNO3
③ a. NaNO2 b. 使 HNO2 完全分解(其他答案合理给分)
(4)稀硝酸不能将 NO 氧化为 NO2,体系中不能发生 NO2 与 H2O 生成 HNO2 的反应