- 653.00 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
富集在海水中的元素——溴和碘
一、选择题(本题包括4小题,每题6分,共24分)
1.(2020·深圳模拟)下列有关卤素的说法错误的是 ( )
A.将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2
B.HF、HCl、HBr、HI的还原性依次增强
C.淀粉碘化钾酸性溶液在空气中变蓝,4I-+O2+4H+2I2+2H2O
D.次氯酸盐具有氧化性,故漂白粉可以漂白织物
【解析】选A。HCl极易溶于水,饱和食盐水可抑制氯气的溶解,洗气得到的氯气中含水蒸气,干燥后得到纯净的Cl2,故A错误;非金属性越强,对应氢化物的还原性越弱,则HF、HCl、HBr、HI的还原性依次增强,故B正确;淀粉遇碘单质变蓝,则淀粉碘化钾酸性溶液在空气中变蓝,发生4I-+O2+4H+2I2+2H2O,故C正确;次氯酸根离子具有强氧化性,可知次氯酸盐具有氧化性,故漂白粉可以漂白织物,故D正确。
2.(双选)下列叙述中正确的是 ( )
A.能使湿润的淀粉KI试纸变成蓝色的物质一定是Cl2
B.用硝酸酸化的硝酸银溶液能一次鉴别NaCl、NaBr、KI三种失去标签的溶液
C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-
D.某浅黄色的溴水,加入CCl4振荡静置后,下层显橙红色
【解析】选B、D。还有很多氧化剂(如HNO3、O3等)能将I-氧化为I2,A错;碘单质的CCl4溶液显紫色,C项错;CCl4的密度比水大,下层显橙红色,D项正确。
3.(2019·东城区模拟) 如下所示为海水综合利用的部分流程,有关说法错误的是 ( )
A.实验室进行①的操作需用到坩埚、玻璃棒、酒精灯
B.②是一个将电能转化为化学能的过程
C.③④⑤涉及的反应均为氧化还原反应
D.④中反应的离子方程式为SO2+Br2+2H2O4H++S+2Br-
- 9 -
【解析】选A。操作①是蒸发,应使用蒸发皿、玻璃棒、酒精灯等,A项错误;②是电解熔融NaCl获得Cl2的过程,B项正确;③是NaBr与Cl2的反应,④是Br2将水溶液中的SO2氧化成H2SO4的过程,⑤是HBr被氧化成Br2的过程,③④⑤中均有元素化合价发生变化,C项正确;生成的H2SO4和HBr均为强电解质,D项正确。
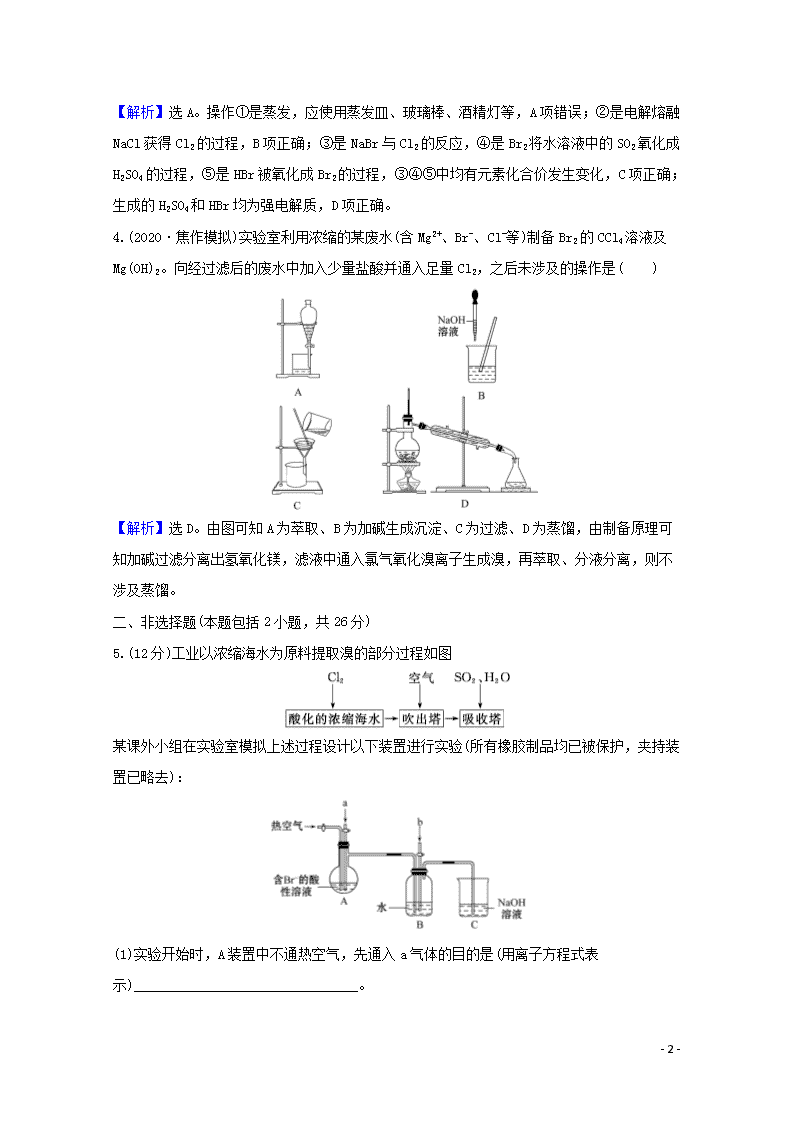
4.(2020·焦作模拟)实验室利用浓缩的某废水(含Mg2+、Br-、Cl-等)制备Br2的CCl4溶液及Mg(OH)2。向经过滤后的废水中加入少量盐酸并通入足量Cl2,之后未涉及的操作是 ( )
【解析】选D。由图可知A为萃取、B为加碱生成沉淀、C为过滤、D为蒸馏,由制备原理可知加碱过滤分离出氢氧化镁,滤液中通入氯气氧化溴离子生成溴,再萃取、分液分离,则不涉及蒸馏。
二、非选择题(本题包括2小题,共26分)
5.(12分)工业以浓缩海水为原料提取溴的部分过程如图
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
(1)实验开始时,A装置中不通热空气,先通入a气体的目的是(用离子方程式表示)________________________________。
- 9 -
(2)A装置中通入a气体一段时间后,停止通入,改通热空气,通入热空气的目的是________________________________。
(3)反应过程中,B装置中Br2与SO2反应的化学方程式:________________________________。
(4)C装置的作用是________________。
(5)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。
①一位同学根据溴的沸点是59 ℃,提出采用________方法从该混合液中分离出溴单质。
②另一位同学向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是________________。
(6)某同学提出证明反应后B装置的溶液中含有溴离子的实验方案是取出少量溶液,先加入过量新制氯水,再加入KI-淀粉溶液,观察溶液是否变蓝色。
该方案是否合理并简述理由:_______________________。
【解析】(1)欲使溴离子变成溴单质,则通入的a气体能和溴离子发生反应生成溴单质,氯气能和溴离子发生置换反应生成溴单质,离子方程式为Cl2+2Br-2Cl-+Br2。
(2)溴易挥发,升高温度促进其挥发,所以通入热空气的目的是吹出Br2。
(3)溴有强氧化性,能和二氧化硫在水中发生氧化还原反应,反应的化学方程式为SO2+Br2+2H2OH2SO4+2HBr。
(4)氯气不可能完全反应,氯气和溴离子反应生成溴单质,未反应的二氧化硫、氯气和溴都有毒,不能直接排空,且这几种物质都能和碱反应,所以C装置是尾气处理装置,即C的作用是吸收未反应的Cl2、Br2和SO2。
(5)①根据溴的沸点是59 ℃,采用蒸馏方法从该混合液中分离出溴单质,②向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是萃取分液。
(6)加入过量新制氯水,再加入淀粉KI溶液,观察溶液是否变蓝色的方法不合理,因过量的氯水也能氧化碘离子生成单质碘,单质碘遇到淀粉变蓝色。
答案:(1)Cl2+2Br-2Cl-+Br2
(2)将溴从蒸馏烧瓶A中吹出
(3)SO2+Br2+2H2OH2SO4+2HBr
(4)吸收未反应完的Cl2、Br2、SO2等有毒气体,防止污染空气
(5)①蒸馏 ②萃取分液
(6)不合理,氯水过量,氧化I-
- 9 -
6.(14分)碘化钾可用于有机合成、制药等,它一种白色立方结晶或粉末,易溶于水。实验室制备KI的实验装置如下:
实验步骤如下:
①在如图所示的C中加入127 g研细的单质I2和195 g 30%的KOH溶液,剧烈搅拌。
②I2完全反应后,打开弹簧夹向其中通入足量的H2S。
③将装置C中所得溶液用稀H2SO4酸化后,置于水浴上加热10 min。
④在装置C的溶液中加入BaCO3,充分搅拌后,过滤、洗涤。
⑤将滤液用氢碘酸酸化,蒸发浓缩至表面出现结晶膜,________、________、洗涤、干燥。
⑥得产品145 g。
回答下列问题:
(1)步骤①将碘研细的目的是______________。
(2)装置A中发生反应的离子方程式为______________; 装置B中的试剂是________,C装置的名称是________。
(3)装置C中I2与KOH反应产物之一是KIO3,该反应的化学方程式为 ________
______________________。
(4)步骤④的目的是______________________。
(5)补充完整步骤⑤:______________、 __________________。
【解析】(1)将碘研细的目的是增大反应物的接触面积,提高反应速率,使反应更充分。
(2)装置A中硫化亚铁与盐酸反应生成硫化氢气体和氯化亚铁,发生反应的离子方程式为FeS+2H+Fe2++H2S↑;因盐酸具有挥发性,制得的H2S气体中混有HCl气体,故装置B中应盛放饱和硫氢化钠溶液;C装置的名称是三颈烧瓶。
(3)由题意可知装置C中I2与KOH发生歧化反应,反应的化学方程式为3I2+6KOHKIO3+5KI+3H2O。
(4)BaCO3与溶液中的S反应生成硫酸钡沉淀,则目的是除去产品中的S。
(5)从溶液中获得KI晶体,要经过蒸发浓缩、冷却结晶、过滤、洗涤和干燥操作。
- 9 -
答案:(1)增大反应物的接触面积,提高反应速率,使反应更充分
(2)FeS+2H+Fe2++H2S↑ 饱和硫氢化钠溶液 三颈烧瓶
(3)3I2+6KOHKIO3+5KI+3H2O
(4)除去产品中的S
(5)冷却结晶 过滤
一、选择题(本题包括3小题,每题6分,共18分)
1.某同学设计完成了以下两个实验:
①向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色(生成了HIO3)。
②向盛有KBr溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成红棕色。继续向试管中滴加氯水,振荡,CCl4层的颜色没有变化。
下列说法不正确的是 ( )
A.实验①生成HIO3时发生的反应为I2+5Cl2+6H2O2HIO3+10HCl
B.实验②中当CCl4层变成红棕色时可通过分液的方法获得Br2的CCl4溶液
C.由上述实验得出Cl2、Br2、I2的氧化性由强到弱的顺序是Cl2>Br2>I2
D.由上述实验得出Cl2、HIO3、HBrO3氧化性由强到弱的顺序是HBrO3>Cl2>HIO3
【解析】选C。由实验①继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色(生成了HIO3)可知,氯气可氧化碘单质,发生的反应为I2+5Cl2+6H2O 2HIO3+10HCl,故A正确;由实验②向盛有KBr溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成红棕色可知,溴易溶于CCl4,则可通过分液的方法获得Br2的CCl4溶液,故B正确;根据氧化剂的氧化性强于氧化产物的氧化性,由实验①可知氧化性:Cl2>I2,由实验②可知氧化性:Cl2>Br2,不能比较Br2、I2的氧化性强弱,故C错误;由实验①、②可知,氧化性由强到弱的顺序是HBrO3>Cl2>HIO3,故D正确。
2.(双选)海洋是一座巨大的化学资源宝库,如图是从海水中提取若干种化学物质的流程图,则下列说法正确的是 ( )
- 9 -
【已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等,应在氯化氢气流中加热。】
A.除去粗盐中的S、Ca2+、Mg2+、Fe3+等杂质,①中加入试剂的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.②中包含制取MgCl2溶液、无水MgCl2及电解熔融状态的MgCl2几个阶段
C.③⑤中溴元素均被氧化
D.蒸馏法是技术最成熟也是最具发展前景的海水淡化方法
【解析】选B、C。A项题给试剂不能除去钡离子,加入药品的正确顺序可为:BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,故A错误;B项第②步,氢氧化镁先与HCl反应生成氯化镁溶液,浓缩结晶得到MgCl2·6H2O,再在HCl气流中加热得到无水氯化镁,电解熔融氯化镁制取Mg,故B正确;C项第③步中溴离子被氧化为溴单质,第⑤步中溴离子被氧化为溴单质,故C正确;D项从海水蒸馏可得蒸馏水,但消耗能源多,该技术不最具发展前景,故D错误。
3.(2020·龙岩模拟)某研究性学习小组的同学利用MnO2、浓盐酸反应来制取干燥的氯气并验证其有无漂白性,所用装置如图所示(可重复使用,不含制气装置)。下列说法正确的是 ( )
A.按气流流动的先后顺序,装置连接顺序依次为DACBE
B.按气流流动的先后顺序,装置连接顺序依次为DABAE
C.装置E的主要用途是制备NaClO
D.在实验中使用到装置C且有色布条褪色,则说明氯气有漂白性
【解析】选B。为验证干燥的氯气有无漂白性,就需要使进入B装置中的氯气不含HCl及水蒸气,故应先用饱和食盐水除去HCl,再用浓硫酸除去水蒸气,为防止E装置中水蒸气进入B装置中,在B、E装置之间还应加装一个A装置,尾气用NaOH溶液吸收,A、C错误,B正确;本实验的目的是验证干燥的Cl2是否具有漂白性,故不需要使用装置C,且Cl2使湿润的有色布条褪色是因为氯气与水反应生成的HClO具有漂白性,D错误。
二、非选择题(本题包括2小题,共32分)
- 9 -
4.(14分)实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为________________________________;该操作将I2还原为I-的目的是________________________。
(2)操作X的名称为________________。
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40 ℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是______________; 锥形瓶里盛放的溶液为________。
(4)已知:5S+2I+2H+I2+5S+H2O。
某含碘废水(pH约为8)中一定存在I2,可能存在I-、I中的一种或两种。请补充完整检验含碘废水中是否含有I-、I的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;________________________________________________。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液。
【解析】(1)该反应为Na2SO3、I2的氧化还原反应,离子方程式为S+I2+H2OS+2I-+2H+。含碘废液中碘以I-、I2的形式存在,将废液中的I2还原为I-的目的是使CCl4中碘进入水层。(2)CCl4不溶于水,因此可以通过分液的方法使其与水分离。(3)实验控制在较低温度下进行,是为了使氯气在溶液中有较大的溶解度(或防止I2升华或防止I2进一步被氧化)。锥形瓶中溶液的作用是吸收过量的Cl2,故锥形瓶中盛放的溶液为NaOH溶液。(4)检验I-,可以利用I-的还原性,先加入淀粉溶液,再加盐酸酸化,最后滴加FeCl3溶液,若溶液变蓝,
- 9 -
则说明废水中含有I-,若溶液不变蓝,则说明废水中不含有I-;检验I,可以利用I的氧化性,先加入淀粉溶液,再加盐酸酸化,最后滴加Na2SO3溶液,若溶液变蓝,则说明废水中含有I,若溶液不变蓝,则说明废水中不含有I。
答案:(1)S+I2+H2O2I-+S+2H+
使CCl4中的碘进入水层 (2)分液
(3)使氯气在溶液中有较大的溶解度(或防止I2升华或防止I2进一步被氧化) NaOH溶液
(4)从水层取少量溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加FeCl3溶液,若溶液变蓝,说明废水中含有I-;若溶液不变蓝,说明废水中不含有I-;另从水层取少量溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加Na2SO3溶液,若溶液变蓝,说明废水中含有I,若溶液不变蓝,说明废水中不含有I
5.(18分)(2020·黄冈模拟)IBr、ICl、BrF3等称为卤素互化物,(CN)2、(SCN)2、(OCN)2等称为拟卤素,它们的化学性质均与卤素单质相似,请回答下列问题。
(1)氯化碘(ICl)中碘元素的化合价为________;它与水反应的化学方程式为ICl+H2OHIO+HCl,该反应的反应类型为________________________(填中学常见的无机反应类型)。
(2)溴化碘(IBr)具有强氧化性,能与Na2SO3溶液反应,发生反应的离子方程式为____________________。
(3)①已知某些离子的还原性强弱顺序为I->SCN->CN->Br->Cl-。现将几滴KSCN溶液滴入含少量Fe3+的溶液中,溶液立即变红,向其中逐滴滴入酸性KMnO4溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象: _____________
________。
②下列物质中,也可以使该溶液红色褪去的是________(填字母)。
A.新制氯水 B.碘水 C.SO2 D.盐酸
(4)KCN为剧毒物质,处理含有KCN的废水常用的方法:在碱性条件下用NaClO溶液将CN-氧化为C和一种单质气体,该反应的离子方程式为__________ ______________。
【解析】(1)Cl得电子能力强于I,则ICl中Cl元素显-1价、I元素显+1价;此反应中没有化合价的变化,属于复分解反应(非氧化还原反应)。
- 9 -
(2)IBr具有强氧化性,I元素显+1价,被还原成I-,S被氧化成S,因此离子方程式为IBr+S+H2OI-+Br-+S+2H+。
(3)①溶液立即变红,发生反应Fe3++3SCN-Fe(SCN)3,加入酸性KMnO4溶液红色褪去,说明KMnO4把SCN-氧化,促使上述平衡向逆反应方向移动,最终Fe(SCN)3完全反应,溶液红色褪去;②能使红色褪去的物质,可以具有强氧化性,如新制氯水将SCN-氧化,也可以具有还原性,如SO2将Fe3+还原,故A、C正确。
(4)CN-中N元素显-3价,C元素显+2价,另一种单质气体为N2,因此反应的离子方程式为2CN-+5ClO-+2OH-2C+N2↑+5Cl-+H2O。
答案:(1)+1 复分解反应
(2)IBr+S+H2OI-+Br-+S+2H+
(3)①酸性高锰酸钾溶液将SCN-氧化,减小了SCN-的浓度,使反应Fe3++3SCN-Fe(SCN)3的平衡不断向左移动,最终Fe(SCN)3完全反应,红色消失 ②AC
(4)2CN-+5ClO-+2OH-2C+5Cl-+N2↑+H2O
- 9 -