- 107.00 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
吉林省松原市油田第十一中学2020-2021学年高一上学期月考试卷
一.选择题(每小题只有一个选项正确,每小题2分共50分)
1.下列诗句描述的过程中包含化学变化的是( )
A.零落成泥碾作尘 B.群山倒影山浮水
C.人面桃花相印红 D.爆竹声中一岁除
2.下列物质的分类正确的是( )
碱
酸
盐
碱性氧化物
酸性氧化物
A
NaOH
H2SO4
BaCO3
SO2
CO2
B
纯碱
HCl
CaCO3
SiO2
CO
C
NaOH
NaHSO4
CaCl2
Na2O
SO2
D
KOH
HNO3
CaCO3
CaO
SO3
3.某同学在奥运五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型是( )
A.复分解反应 B.分解反应
C.化合反应 D.置换反应
4.下列说法中正确的是( )
A.NaHSO4显强酸性,因此从组成上分类它应该属于酸
B.含Fe元素质量分数为70%的Fe2O3是纯净物
C.CuSO4·5H2O是混合物
D.显碱性的物质一定为碱
5.中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700 ℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些理解,其中错误的是( )
A.金刚石属于金属单质 B.制造过程中元素种类没有改变
C.CCl4是一种化合物 D.这个反应是置换反应
6.下列液体中,不会出现丁达尔效应的分散系是( )
①鸡蛋清溶液 ②水 ③淀粉溶液 ④蔗糖溶液 ⑤FeCl3溶液 ⑥肥皂水
A.④⑤ B.③④
C.②④⑤ D.①③④
7.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
A.分散质颗粒直径都在1~100 nm之间 B.能透过半透膜
C.颜色都呈红褐色 D.能透过滤纸
8.下列有关说法正确的是( )
A.溶液和胶体的本质区别是能否发生丁达尔效应
B.含FeCl3溶质的溶液形成胶体后,胶体粒子为FeCl3
C.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3 胶体>FeCl3溶液
D.可通过观察液体是否澄清透明,来区别溶液和胶体
9.甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。下列各组物质按照甲、乙、丙的顺序不符合要求的是( )
A.C、CO、CO2 B.H2O2、H2O、O2
C.KOH、K2CO3、KNO3 D.Fe2O3、FeCl3、Fe(OH)3
10.常温下 ,某反应M+N―→盐+水,其中M、N的类别不可能是( )
A.酸、碱 B.单质、氧化物
C.氧化物、酸 D.氧化物、碱
11.下列叙述中正确的是( )
A.强电解质溶液的导电性一定比弱电解质溶液的导电性强
B.稀盐酸溶液能导电,所以稀盐酸是电解质
C.二氧化硫溶于水能导电,故二氧化硫属于电解质
D.硫酸钡虽然难溶于水,但硫酸钡属于电解质
12.下列关于电解质的叙述中错误的是( )
A.在水溶液里或熔融状态下能够导电的化合物叫电解质
B.电解质是对化合物而言,单质不属于此范畴
C.电解质在水中一定能导电,在水中导电的化合物一定是电解质
D.纯水的导电性很差,但水也是电解质
13. 下列电离方程式中,书写不正确的是( )
A.Ca(OH)2===Ca2++2OH- B.NaOH===Na++O2-+H+
C.HCl===H++Cl- D.KHCO3===K++HCO
14.分别向下列各溶液中加入少量NaOH固体,溶液的导电能力变化最小的是( )
A.水 B.盐酸
C.醋酸溶液 D.NaCl溶液
15.离子方程式CO+2H+===H2O+CO2↑中的CO代表的物质可以是( )
A.CaCO3 B.NaHCO3
C.Na2CO3 D.BaCO3
16.下列反应能用H++OH-===H2O表示的是( )
A.醋酸和氢氧化钠溶液 B.氢氧化镁和盐酸
C.氢氧化钡和稀硫酸 D.澄清石灰水和硝酸
17.在无色透明酸性溶液中能大量共存的离子组是( )
A.Al3+、Ag+、NO、Cl- B.Mg2+、NH、NO、Cl-
C.K+、CO、Cl-、Na+ D.Na+、OH-、SO、Fe2+
18.以下各组离子能在溶液中大量共存的是( )
A.含有大量SO的溶液:加入Mg2+、Cu2+、Cl-、NO
B.滴加酚酞变红的溶液:加入SO、Cu2+、K+、Cl-
C.所含溶质为NaHSO4的溶液:加入K+、CO、NO、Na+
D.常温下,加入铁粉能生成H2的溶液:加入Na+、Ca2+、Cl-、CO
19.下列各组离子在碱性条件下能大量共存,在强酸性条件下不能大量共存的是( )
A.Mg2+、Na+、SO、Cl- B.K+、CO、Cl-、NO
C.Na+、K+、NO、SO D.NH、Na+、SO、NO
20.下列各组离子在溶液中可大量共存的是( )
A.NH、SO、K+、OH- B.H+、Ba2+、NO、SO
C.K+、Cl-、CO、Na+ D.Ca2+、NO、Na+、CO
21.下列反应的离子方程式书写正确的是( )
A.稀硫酸滴在铁片上:2Fe+6H+===2Fe3++3H2↑
B.氧化钙与稀盐酸反应:CaO+2H+===Ca2++H2O
C.稀硝酸与石灰乳反应:H++OH-===H2O
D.锌和硝酸银溶液反应:Zn+Ag+===Zn2++Ag
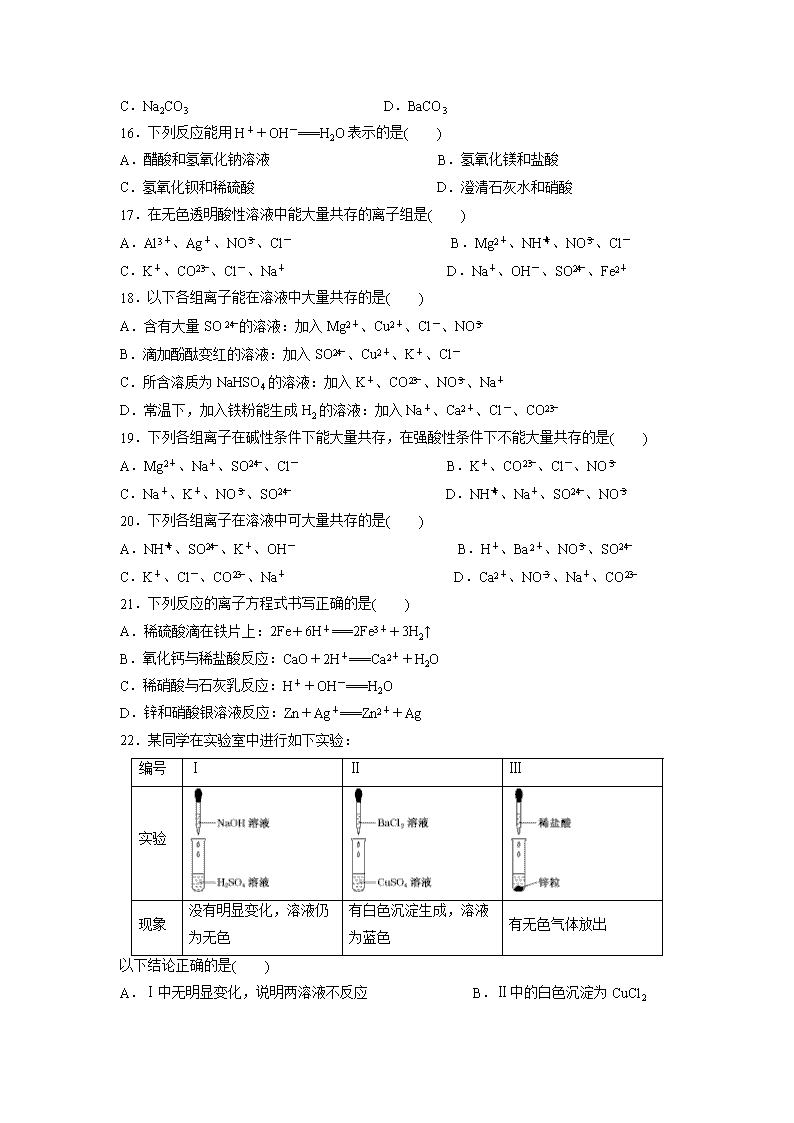
22.某同学在实验室中进行如下实验:
编号
Ⅰ
Ⅱ
Ⅲ
实验
现象
没有明显变化,溶液仍为无色
有白色沉淀生成,溶液为蓝色
有无色气体放出
以下结论正确的是( )
A.Ⅰ中无明显变化,说明两溶液不反应 B.Ⅱ中的白色沉淀为CuCl2
C.Ⅲ中的离子方程式为2H++Zn===Zn2++H2↑ D.Ⅲ中发生的反应不是离子反应
23.下列离子方程式不正确的是( )
A.氢氧化钠与盐酸反应:OH-+H+===H2O
B.氧化镁与稀硫酸反应:O2-+2H+===H2O
C.碳酸钙与盐酸反应:CaCO3+2H+===Ca2++H2O+CO2↑
D.Fe与硫酸铜溶液:Fe+Cu2+=== Cu+ Fe2+
24.下列离子方程式改写成化学方程式正确的是( )
A.Zn2++2OH-===Zn(OH)2↓ B.Ba2++SO===BaSO4↓
ZnCO3+2NaOH===Zn(OH)2↓+Na2CO3 Ba(OH)2+H2SO4===BaSO4↓+2H2O
C.Ca2++CO32-===CaCO3↓ D.Cu+2Ag+===Cu2++2Ag
CaCl2+Na2CO3===CaCO3↓+2NaCl Cu+2AgCl===CuCl2+2Ag
25.不能用离子方程式 CO32-+2H+═CO2↑+ H2O 表示的反应是( )
A.Na2CO3+2HCl═2NaCl+CO2↑+H2O B.NaHCO3+HCl═NaCl+CO2↑+H2O
C.K2CO3+2HNO3═2KNO3+CO2↑+H2O D.K2CO3+2HNO3═2KNO3+CO2↑+H2O
第Ⅱ卷 (60分)
二、填空(除34题外,每空2分,共50分)
26.(1)写出下列物质的电离方程式:
H2SO4 ___________________________; Ba(OH)2___________________________;
Fe2(SO4)3___________________________; NaHSO4(水溶液)________________ ______。
属于酸的物质是_______________ (写化学式,下同);属于碱的物质是_______________;
属于盐的物质是_______________。
(2)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是________________________________。
②写出纯碱的电离方程式:__________________________________。
27. 以下几种物质:①干燥的食盐晶体;②液态氯化氢;③水银;④蔗糖;⑤KNO3溶液;⑥CO2;⑦熔融的KCl;⑧盐酸;⑨H2SO4。
以上物质中,能导电的是______________ (填序号,下同);属于电解质的是______________;
属于非电解质的是______________。
28. 分类法是一种重要的学习方法。下列4组物质中均有一种物质的类别与其他三种不同,请分别填出其化学式。
甲:Ca、H2、O2、Cl2;
乙:CO、CaO、CO2、SO2;
丙:Ca(OH)2、K2CO3、KHCO3、K2SO4;
丁:NaOH、Ca(OH)2、KOH、CaCl2。
(1)甲________,乙________,丙________,丁________。
(2)根据图示,写出序号所示反应的化学方程式:
①________________________________________________________________________。
②________________________________________________________________________。
③________________________________________________________________________。
29.写出下列反应的离子方程式:(每个3分,共12分)
(1)NaOH溶液与稀硝酸的反应:_____________________________________________。
(2)BaCl2溶液与K2SO4溶液的反应:___________________________________________。
(3)K2CO3溶液与足量稀硫酸的反应:_________________________________________。
(4)AgNO3溶液与稀盐酸的反应:_____________________________________________。
三、附加题: (每空2分,共10分)
已知甲、乙、丙是三种可溶性物质。其中甲是碱,乙、丙是盐,它们溶于水后电离产生的所有离子如下表所示:
阳离子
Na+、H+、Ba2+
阴离子
OH-、CO、SO
(1)甲的化学式为__________。
(2)乙溶液与丙溶液反应可生成气体M,则M的化学式为___________,该反应的离子方程式为_______________________________________。
(3)乙、丙溶液与甲溶液反应可分别生成白色沉淀A和B,其中B可溶于稀硝酸。
①乙的化学式为__________;
②B溶于稀硝酸的离子方程式为___________________________________________________。
【参考答案】
一、选择题
DDBBA CDCCB DCBBC DBABC CBBCB
二、填空题
26.(1) H2SO4===H++SO42-
Ba(OH)2===Ba2++2OH-
Fe2(SO4)3 ===2Fe3++3SO42-
NaHSO4(水溶液) ===Na++H++SO42-
H2SO4 Ba(OH)2 Fe2(SO4)3 、 NaHSO4
(2) 纯碱 Na2CO3===2Na++CO32-
27. ③⑤⑦⑧ ①②⑦⑨ ④⑥
28. (1)Ca CaO Ca(OH)2 CaCl2
(2)①Ca+O2===CaO
②CaO+H2O=== Ca(OH)2
③Ca(OH)2+2HCl===CaCl2+2H2O
29.(1)OH-+H+===H2O (2)Ba2++SO===BaSO4↓
(3)CO+2H+===H2O+CO2↑ (4)Ag++Cl-===AgCl↓
附加题:(1)Ba(OH)2
(2)CO2 2H++CO===H2O+CO2↑
(3)①NaHSO4 ②BaCO3+2H+===Ba2++H2O+CO2↑