- 741.00 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第一节 物质的组成、分类和性质 传统化学文化
考纲定位
要点网络
1.了解分子、原子、离子和原子团等概念的含义。
2.理解物理变化与化学变化的区别与联系。
3.理解混合物和纯净物、单质和化合物、金属和非金属的概念。
4.理解酸、碱、盐、氧化物的概念及其相互联系。
5.了解胶体是一种常见的分散系。了解溶液和胶体的区别。
6.了解化学的主要特点是在原子、分子水平上认识物质。了解化学可以识别、改变和创造分子。
7.了解化学与传统文化的关系。
物质的组成和分类
1.物质的组成
(1)构成粒子
(2)元素、物质及粒子间的关系
①宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
②元素与物质的关系:
元素
(3)同素异形体
①同种元素形成的不同单质叫同素异形体。
②同素异形体之间的性质差异主要体现在物理性质上,同素异形体之间的转化属于化学变化。
(4)物质类别
①纯净物:由同种单质或化合物组成的物质。
②混合物:由几种不同单质或化合物组成的物质。
③氧化物:由两种元素组成,其中一种为氧元素的化合物。
a.酸性氧化物:能与碱反应只生成盐和水的氧化物。
如CO2、SO2。
b.碱性氧化物:能与酸反应只生成盐和水的氧化物。
如CaO、CuO。
c.两性氧化物:既能与酸反应又能与碱反应生成盐和水的氧化物。如Al2O3。
④酸:电离出的阳离子全部是H+的化合物。
⑤碱:电离出的阴离子全部是OH-的化合物。
⑥盐:金属阳离子或铵根离子与酸根阴离子构成的化合物。
[补短板]
(1)相同元素组成的物质不一定为纯净物,如O2与O3的混合物。
(2)分子式相同的物质组成的物质不一定为纯净物,如正丁烷与异丁烷的混合物。
(3)高分子化合物属于混合物(如淀粉、聚乙烯)。
(4)一个一元强酸分子一定能电离出一个H+,电离出一个H+的不一定是一元酸(如NaHSO4)。
(5)盐中的阳离子不一定是金属阳离子,也可能是NH。
(6)物质不一定都是由分子构成。如金刚石由原子构成,NaCl由离子构成。
(7)测定固体是否为纯净物的一般方法是测定是否有固定的熔点。
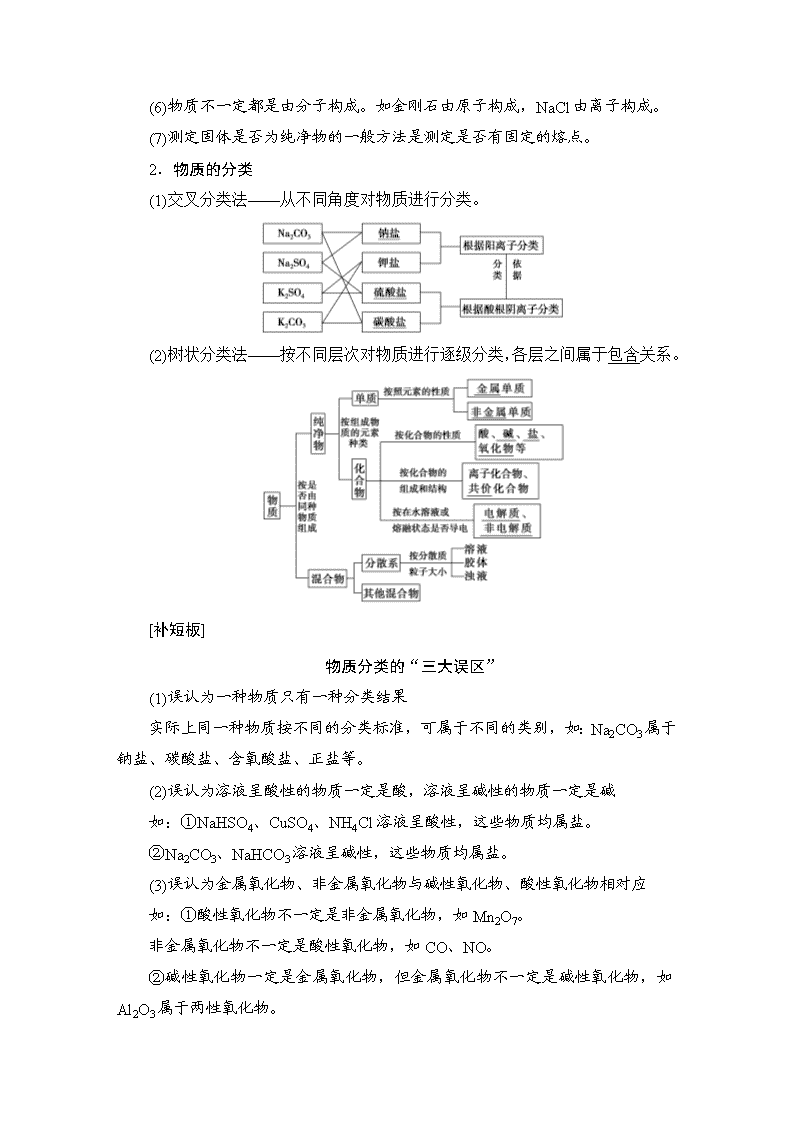
2.物质的分类
(1)交叉分类法——从不同角度对物质进行分类。
(2)树状分类法——按不同层次对物质进行逐级分类,各层之间属于包含关系。
[补短板]
物质分类的“三大误区”
(1)误认为一种物质只有一种分类结果
实际上同一种物质按不同的分类标准,可属于不同的类别,如:Na2CO3属于钠盐、碳酸盐、含氧酸盐、正盐等。
(2)误认为溶液呈酸性的物质一定是酸,溶液呈碱性的物质一定是碱
如:①NaHSO4、CuSO4、NH4Cl溶液呈酸性,这些物质均属盐。
②Na2CO3、NaHCO3溶液呈碱性,这些物质均属盐。
(3)误认为金属氧化物、非金属氧化物与碱性氧化物、酸性氧化物相对应
如:①酸性氧化物不一定是非金属氧化物,如Mn2O7。
非金属氧化物不一定是酸性氧化物,如CO、NO。
②碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物,如Al2O3属于两性氧化物。
(1)人们可以利用先进的化学技术,选择适宜的条件,利用化学反应制造新的原子。( )
(2)冰水混合而形成混合物,聚乙烯为纯净物。( )
(3)Fe2O3、Al2O3、Mn2O7、CrO3均与酸反应,均属于碱性氧化物。( )
(4)NaHSO4、NaHSO3的水溶液呈酸性,故二者既属于酸又属于盐。( )
(5)H3PO4、H3PO3、H3PO2均为三元弱酸。( )
[答案] (1)× (2)× (3)× (4)× (5)×
(1)①能电离出H+的化合物都是酸吗?___________________。
②CH3COOH属于几元酸?________;已知H3PO2的结构为属于一元酸,写出H3PO2与足量NaOH反应的化学方程式______________________,NaH2PO2的水溶液呈________性(填“酸”“碱”“中”)。
(2)①含氧的化合物都是氧化物吗?__________。
②只含一种元素的物质都是纯净物吗?________。
③C2H6O只是表示一种分子吗?________。
[答案] (1)①不一定,如NaHSO4 ②一元酸 H3PO2+NaOH===NaH2PO2+H2O 碱 (2)①不一定,如H2SO4 ②不一定,如金刚石与石墨的混合物 ③不是,可以表示乙醇或甲醚(CH3OCH3)
命题点 物质的组成和分类
1.(2019·试题调研)工业上利用矿物资源的流程图如下,下列说法正确的是
( )
A.转化产物中Al2O3、FeO均为碱性氧化物,碱性氧化物一定是金属氧化物
B.制备玻璃过程中,石灰石的主要成分属于盐类,纯碱属于碱类,二者均能与盐酸反应
C.在制备纯硅过程时,涉及的反应均为置换反应
D.黄铜矿(主要成分为CuFeS2)与O2反应产生的Cu2S、FeO均是还原产物
D [Al2O3属于两性氧化物,FeO属于碱性氧化物,碱性氧化物均为金属氧化物,A错误;石灰石的主要成分为碳酸钙,属于盐类,纯碱是碳酸钠,也属于盐类,二者均能与盐酸反应,B错误;硅与氯气反应生成四氯化硅的反应属于化合反应,C错误;根据CuFeS2与O2反应的原理,Cu与O化合价均降低,可以推断出产物Cu2S、FeO均是还原产物,D正确。]
2.下列物质的分类正确的是( )
选项
碱
酸
盐
碱性氧化物
酸性氧化物
A
Na2CO3
H2SO4
NaOH
SO2
CO2
B
NaOH
HCl
NaCl
Na2O
NO
C
KOH
HNO3
CaCO3
CaO
Mn2O7
D
NaOH
HCl
CaF2
Na2O2
SO2
C [A项,Na2CO3、NaOH、SO2依次为盐、碱、酸性氧化物,错误;B项,NO不是酸性氧化物,错误;D项,Na2O2不是碱性氧化物,错误。]
3.下列物质中,属于纯净物的是( )
①陶瓷 ②水泥 ③玻璃 ④漂白粉 ⑤胆矾 ⑥氯水
⑦液氯
A.①③⑤ B.②④⑥
C.⑤⑦ D.⑥⑦
[答案] C
4.有下列物质:①氧气 ②二氧化碳 ③臭氧(O3) ④盐酸 ⑤铁 ⑥碳酸钠 ⑦空气 ⑧氢氧化钠 ⑨冰水混合物 ⑩乙醇 ⑪甲醚
(1)其中由分子直接构成的纯净物有_______(填序号,下同)。
(2)由原子直接构成的纯净物有__________________________。
(3)由离子直接构成的纯净物有__________________________。
(4)互为同素异形体的是________________________________。
(5)属于单质的有______________________________________。
(6)属于化合物的有____________________________________。
(7)属于混合物的有____________________________________。
(8)互为同分异构体的是________________________________。
[答案] (1)①②③⑨⑩⑪ (2)⑤ (3)⑥⑧ (4)①③ (5)①③⑤ (6)②⑥⑧⑨⑩⑪ (7)④⑦ (8)⑩⑪
熟记常见混合物
(1)气体混合物:空气、水煤气(CO和H2)、爆鸣气(H2和O2)、天然气(主要成分是CH4)、焦炉气(主要成分是H2和CH4)、高炉煤气、石油气、裂解气。
(2)液体混合物:氨水、氯水、王水、天然水、硬水、软水、水玻璃、福尔马林、浓硫酸、盐酸、汽油、植物油、胶体。
(3)固体混合物:大理石、碱石灰、漂白粉、高分子化合物、玻璃、水泥、合金、铝热剂。
物质的性质及其类别转化
1.物质的性质和变化
(1)物质的性质
①物理性质主要表现在颜色、熔沸点、硬度、状态、气味、溶解性、导电性、导热性、密度、光泽和延展性等。
②化学性质主要表现在金属性、非金属性、可燃性、还原性、氧化性、酸碱性、稳定性等。
(2)物质的变化
物理变化
化学变化
特征(宏观上)
没有新物质生成
有新物质生成
实质(微观上)
只有化学键的断裂或生成,或两者均没有发生变化
有旧化学键的断裂,同时有新化学键的生成
提醒:熟记常见物理变化与化学变化
(1)常见的物理变化:①物质三态变化;②金属导电;③蒸馏和分馏;④挥发、升华;⑤吸附、盐析、渗析;⑥溶解、潮解;⑦焰色反应。
(2)常见的化学变化:①风化、硫化、老化、裂化、硝化、钝化、硬化、氢化、水化、皂化、炭化、催化、酯化、同素异形体的相互转化;②脱水;③干馏、爆炸;④电解、电镀、电化学腐蚀、电解质溶液导电;⑤煤的液化与气化。
2.物质的转化
(1)化学反应的分类
化学反应
(2)酸、碱、盐、氧化物和单质之间的转化
①强酸制弱酸:如实验室制CO2和SO2,其离子方程式分别为CaCO3+2H+===Ca2++CO2↑+H2O和SO+2H+===SO2↑+H2O。
②强碱制弱碱:如制NH3,NH4Cl+NaOHNaCl+NH3↑+H2O。
③易溶物转化为难溶物:如AgNO3+NaCl===AgCl↓+NaNO3。
④难溶物转化为更难溶物:如3Mg(OH)2+2FeCl3===3MgCl2+2Fe(OH)3。
⑤难挥发物转化为易挥发物:如
NaCl+H2SO4(浓)HCl↑+NaHSO4。
⑥置换反应:如
Zn+H2SO4===ZnSO4+H2↑,
Zn+FeSO4===Fe+ZnSO4。
⑦化合反应:如
2Cu+O22CuO,S+O2SO2。
(1)H2、CO的可燃性与还原性均体现化学性质。( )
(2)Fe、Al、Cu久置于潮湿空气中均变为氧化物。( )
(3)CO还原CuO的反应属于置换反应。( )
(4)酸性氧化物一定是非金属氧化物,且能与水反应生成相应的酸。( )
(5)冰的液化与煤的液化均为物理变化。( )
[答案] (1)√ (2)× (3)× (4)× (5)×
已知下列转化关系
请回答:
(1)①③④⑤的基本反应类型分别为________、______、________、________。
(2)写出上述转化所对应的化学方程式:
③_________________________________________________。
④_________________________________________________。
⑤_________________________________________________。
[答案] (1)化合反应 置换反应 复分解反应 复分解反应
(2)③Ca+2H2O===Ca(OH)2+H2↑
④Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
⑤CaCO3+2HCl===CaCl2+CO2↑+H2O
命题点1 物质的性质及变化
1.(2019·济南模拟)《天工开物》中的《燔石》篇载有:“百里内外,土中必生可燔石……掘取受燔……火力到后,烧酥石性,置于风中久自吹化成粉。急用者以水沃之,亦自解散……用以砌墙石,则筛去石块,水调粘合。”其中不涉及的物质是( )
A.石膏 B.石灰石
C.熟石灰 D.生石灰
A [“火力到后,烧酥石性”,发生反应:CaCO3CaO+CO2↑;“急用者以水沃之,亦自解散”,发生反应:CaO+H2O===Ca(OH)2;“
用以砌墙石,则筛去石块,水调粘合”,发生反应:Ca(OH)2+CO2===CaCO3↓+H2O,没有涉及的物质是石膏(CaSO4·2H2O),A项符合题意。]
2.(2019·郑州模拟)科学家将水置于足够强的电场中,在20 ℃时水分子瞬间凝固可形成“暖冰”。某兴趣小组做如图所示实验,发现烧杯中酸性KMnO4溶液褪色,且有气泡产生。将酸性KMnO4溶液换成FeCl3溶液,烧杯中溶液颜色无变化,但有气泡产生。则下列说法正确的是( )
A.20 ℃时,水凝固形成“暖冰”所发生的变化是化学变化
B.“暖冰”是水置于足够强的电场中形成的混合物
C.烧杯中液体为FeCl3溶液时,产生的气体为Cl2
D.该条件下H2燃烧的产物中可能含有一定量的H2O2
D [水凝固形成“暖冰”的过程中只有水的状态发生了变化,没有生成新物质,故所发生的变化是物理变化,A、B项错误;酸性KMnO4溶液褪色,说明H2燃烧生成了具有还原性的物质,该物质被氧化产生气体,故有气泡产生,结合元素守恒,推测该物质为H2O2,H2O2在Fe3+的作用下分解产生O2,故将酸性KMnO4溶液换成FeCl3溶液,溶液颜色不变化,但有气泡产生,C项错误,D项正确。]
3.下列变化中,前者是物理变化,后者是化学变化,且都有明显颜色变化的是( )
A.打开盛装NO的集气瓶;冷却NO2气体
B.用冰水混合物冷却SO3气体;加热氯化铵晶体
C.木炭吸附NO2气体;将氯气通入品红溶液中
D.向品红溶液中加入Na2O2;向FeCl3溶液中滴加KSCN溶液
C [A项,前者发生化学反应:2NO+O2===2NO2;B项,加热氯化铵晶体分解产生HCl和NH3,发生的是化学变化,没有明显颜色变化;D项,前者为Na2O2的氧化性漂白为化学变化。]
物理变化和化学变化的判断方法
命题点2 酸、碱、盐、氧化物、单质之间的转化
4.(2019·武汉名校联考)在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.FeFeCl2Fe(OH)2
B.CaCO3CaOCaSiO3
C.Al2O3Al(OH)3NaAlO2
D.SSO3H2SO4
B [Fe在氯气中燃烧生成FeCl3,A项错误;B项所示转化的化学方程式为CaCO3CaO+CO2↑、CaO+SiO2CaSiO3,B项正确;Al2O3难溶于水,不与水反应,C项错误;S在氧气中燃烧生成SO2,D项错误。]
5.下表各组物质中,可以实现XYZ(每步只发生一个反应)所示转化的是( )
选项
X
Y
Z
M
A
Fe
FeO
Fe2O3
O2
B
C
CO
CO2
O2
C
CO2
Na2CO3
NaHCO3
NaOH
D
AlO
Al(OH)3
Al3+
CO2
B [A项,FeFe3O4,错误;C项,Na2CO3与NaOH不反应,错误;D项,Al(OH)3与CO2不反应,错误。]
6.物质A、B、C、D满足下列连续氧化的转化关系:
ABCD(酸或碱)
(1)若D为碱,则A、B、C、D分别为________、________、________、________;并写出其转化关系___________________________________________________
__________________________________________________________________。
(2)若D为酸,则满足上述转化关系的物质分别有______________________;并分别写出其转化关系_______________________________________________。
[答案] (1)Na Na2O Na2O2 NaOH
NaNa2ONa2O2NaOH
(2)N2、NH3、S、H2S、C
N2:N2NONO2HNO3、
NH3:NH3NONO2HNO3、
S:SSO2SO3H2SO4、
H2S:H2SSO2SO3H2SO4、
C:CCOCO2H2CO3
分散系 胶体
1.分散系
(1)组成
(2)分类
①把分散系分为溶液、胶体和浊液的本质标准是:分散质粒子直径的大小。可用如下方式直观地表示:
②若按分散质或分散剂的状态分类,可分为9种分散系,如图:
烟属于固气分散系;雾属于液气分散系;
悬浊液属于固液分散系;合金属于固固分散系。
(3)三种分散系的比较
分散系
溶液
胶体
浊液
分散质粒子
单个小分子或离子
高分子或多分子集合体
巨大数目的分子集合体
性
质
外观
均一、透明
均一
不均一、不透明
稳定性
稳定
较稳定
不稳定
能否透
过滤纸
能
能
不能
能否透过
半透膜
能
不能
不能
鉴别
无丁达尔效应
有丁达尔效应
静置分层或沉淀
2.Fe(OH)3胶体的制备
(1)实验操作
(2)反应原理:FeCl3+3H2OFe(OH)3(胶体)+3HCl(写化学方程式)。
(3)书写制备Fe(OH)3胶体化学方程式的四个易错点
①用“===”而不用“”。
②Fe(OH)3分子式后注明胶体而不使用“↓”符号。
③反应条件是“△”。
④HCl后不能标“↑”符号。
3.胶体的本质特征、性质及应用
(1)本质特征:分散质粒子直径为1~100_nm。
(2)胶体的性质及应用
①丁达尔效应
可见光束通过胶体时,会出现光亮的通路现象。
应用:鉴别溶液和胶体。
②聚沉
胶体粒子聚集成为较大颗粒,从而形成沉淀从分散剂里析出的过程叫作聚沉。
使胶体聚沉的方法有a.加入电解质;b.加入与胶粒相反电荷的胶体;c.加热。
应用:三角洲的形成;明矾、铁盐溶液净水;盐卤制豆腐。
③电泳:在电场的作用下,胶体粒子在分散剂里作定向移动,利用此性质可以证明胶体粒子带有电荷。
应用:工业上静电除尘。
熟记:常见的胶体有①烟或雾、②鸡蛋白的溶液、③血液、④淀粉溶液、⑤豆浆、⑥牛奶、⑦墨水、⑧Fe(OH)3胶体、⑨硅酸胶体、⑩有色玻璃、⑪烟水晶。
(3)胶体净水
①胶体粒子的直径一般在1~100 nm之间,它决定了胶体粒子具有较大的表面积,吸附力很强,能在水中吸附悬浮固体或毒素形成沉淀,从而达到净化水的目的。
②常见的净水剂有KAl(SO4)2·12H2O、FeCl3·6H2O等,其净水原理是Al3+、Fe3+发生水解反应分别生成Al(OH)3胶体、Fe(OH)3胶体。
③胶体净水一般没有杀菌消毒作用。
[补短板]
(1)胶体一般分气溶胶(如雾)、液溶胶(如血液)和固溶胶(如烟水晶)。
(2)胶体不带电,胶体中的胶粒能够吸附体系中的带电离子而使胶粒带电荷,但整个分散系仍呈电中性。
(3)胶体中的分散质粒子能透过滤纸,但不能透过半透膜,因此可用过滤的方法分离胶体和浊液,用渗析的方法分离胶体和溶液中的分散质。
(4)丁达尔效应是物理变化,不是化学变化,是光的散射现象。
(5)在Fe(OH)3胶体中,Fe(OH)3胶体粒子是Fe(OH)3分子的集合体,因此1 mol Fe3+完全水解得到的Fe(OH)3胶体粒子数小于NA(NA表示阿伏加德罗常数的值)。
(1)依据丁达尔效应可将分散系分为溶液、胶体与浊液。( )
(2)鸡蛋白的溶液、血液、淀粉溶液均能发生丁达尔效应。( )
(3)胶体和溶液都是均一、稳定的分散系,静置不易产生沉淀。( )
(4)明矾净水时发生了化学及物理变化,能起到杀菌、消毒作用。( )
(5)型号不同的钢笔水混用易造成笔不出水和石膏加入豆浆中形成豆腐均与胶体的聚沉有关。( )
(6)河海交汇处易形成沙洲,体现胶体的聚沉。( )
[答案] (1)× (2)√ (3)√ (4)× (5)√ (6)√
(1)将FeCl3饱和溶液加入氨水或NaOH溶液中能形成Fe(OH)3胶体吗?为什么?
[答案] 不能。因为氨水或NaOH溶液中c(OH-)较大,生成Fe(OH)3沉淀。
(2)将制备的Fe(OH)3胶体做电泳实验,一段时间后,阴极附近颜色加深,可证明Fe(OH)3胶粒带什么电荷?
[答案] 正电荷。
(3)向Fe(OH)3胶体中加入饱和(NH4)2SO4溶液发生的现象是_____________,原因是_______________________________________________________________
____________________________________________________________________。
[答案] 产生红褐色沉淀 (NH4)2SO4为电解质,使胶体聚沉
(4)向Fe(OH)3胶体中滴入过量稀硫酸,现象是__________________________ __________,其原因是_________________________________________________ ___________________________________________________________________。
[答案] 先生成红褐色沉淀,后沉淀溶解 开始加稀硫酸,胶体聚沉生成Fe(OH)3沉淀,当酸过量时,Fe(OH)3沉淀又溶于酸
命题点 分散系与胶体的性质及应用
1.(2019·长春期中)FeCl3溶液、Fe(OH)3胶体、Fe(OH)3浊液是三种重要的分散系,下列叙述中不正确的是( )
A.Fe(OH)3胶体区别于其他分散系的本质特征是分散质粒子的直径在1~100 nm之间
B.分别用一束光透过三种分散系,只有Fe(OH)3胶体具有丁达尔效应
C.三种分散系的颜色都相同,且均能与盐酸反应,具有吸附性
D.三种分散系中分散质均属于电解质
C [FeCl3溶液为棕黄色,不能与盐酸反应,且不具有吸附性,Fe(OH)3胶体、Fe(OH)3浊液均为红褐色,Fe(OH)3浊液不具有吸附性,C项不正确。]
2.下列说法不正确的是 ( )
A.利用丁达尔效应可区分蛋白质溶液与葡萄糖溶液
B.将饱和FeCl3溶液滴入沸水中,继续煮沸至溶液呈红褐色即生成氢氧化铁胶体
C.用过滤法可以除去Fe(OH)3胶体中的FeCl3
D.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
C [胶体粒子可以通过滤纸,不能用过滤提纯胶体。]
3.生产生活中的许多现象或应用都与化学知识有关。下列现象或应用与胶体性质无关的是( )
A.将盐卤或石膏加入豆浆中,制成豆腐
B.一支钢笔使用两种不同型号的蓝黑墨水,易出现堵塞
C.泡沫灭火器中将Al2(SO4)3与NaHCO3两溶液混合后,喷出大量泡沫,起到灭火作用
D.清晨,人们经常能看到阳光穿过茂密的树木枝叶所产生的美丽景象
C [Al3+与HCO发生水解反应,生成沉淀和气体,与胶体性质无关。]
4.我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”也有科学道理。那么这种做法的化学原理是
( )
A.胶体的电泳
B.血液的氧化还原反应
C.血液中发生复分解反应
D.胶体的聚沉
D [血液属于胶体,往伤口上撒盐,能够中和血液胶体粒子所带电荷,使血液胶体粒子相互聚集而沉降,从而起到止血的作用。]
5.某同学在实验室进行了如图所示的实验,回答下列问题:
(1)利用________方法(填分离方法),可将Z中固体与液体分离。
(2)如何确定X、Z烧杯中的液体属于何种分散系:___________ ___________________________________________________________________
___________________________________________________________________。
(3)Y中反应的离子方程式为________________________________________
___________________________________________________________________。
[答案] (1)过滤
(2)通过丁达尔效应进行确定,能发生丁达尔效应的分散系是胶体,不能发生丁达尔效应的分散系是溶液
(3)3CaCO3+2Fe3++3H2O===2Fe(OH)3(胶体)+3CO2↑+
3Ca2+
化学与传统文化
——科学精神与社会责任
为了培养青少年对祖国的爱国情怀,各科高考命题都强化了传统文化与各学科之间的关系。对化学学科,分析近几年高考试题,命题的角度主要以传统文化中古诗词、传统化工工艺、古代著作叙述等为载体,考查化学物质的成分、性质及反应类型,实验操作等。体现了“科学精神与社会责任”的化学核心素养。
题型1 以传统文化为载体,考查物质成分
1.(2019·试题调研)方以智在《物理小识》中指出:“有硇水(硇水是一种酸),剪银块投之,则旋而为水。”下列叙述正确的是( )
A.其中涉及的反应为置换反应
B.其中的“硇水”是指MgCl2溶液
C.“硇水”与银反应可生成密度最小的气体
D.“旋而为水”中的“水”可用来检验Cl-
D [与Ag反应的酸应为HNO3,反应生成AgNO3溶液。]
2.我国湖笔的制作技艺属于国家非物质文化遗产,相传古人制作该毛笔的过程为“以枯木为管,鹿毛为柱,羊毛为被(外衣)”,下列说法不正确的是( )
A.枯木、鹿毛、羊毛的主要成分均为天然高分子化合物,且均能够水解
B.枯木等木材隔绝空气加强热可以得到焦炭、苯、甲苯等
C.鹿毛的成分中一定含有C、H、O、N元素
D.采用灼烧法可以区分毛笔的“外衣”是羊毛还是化学纤维
B [枯木的主要成分是植物纤维,鹿毛、羊毛的主要成分是蛋白质,二者均为天然高分子化合物,且均能够水解,A正确;枯木隔绝空气加强热可以得到木炭等,煤隔绝空气加强热可以得到焦炭以及煤焦油等,B错误;鹿毛的主要成分为蛋白质,一定含有C、H、O、N元素,C正确;区分蛋白质和化学纤维一般可以使用灼烧法,有烧焦羽毛气味的毛笔的“外衣”是羊毛,D正确。]
3.(2019·豫南豫北名校联考)下列对与化学有关的文献的理解错误的是
( )
A.《咏石灰》(明·于谦)中写道:“……烈水焚烧若等闲……要留清白在人间。”其中“清白”是指氢氧化钙
B.《咏煤炭》(明·于谦)中写道:“凿开混沌得乌金……不辞辛苦出山林。”其中“乌金”的主要成分是煤炭
C.《天工开物》中记载:“凡火药以硝石、硫黄为主,草木灰为辅……魂散惊而魄齑粉。”文中提到的是火药
D.《天工开物》中有如下描述:“世间丝、麻、裘、褐皆具素质……”,文中的“裘”主要成分是蛋白质
A [《咏石灰》的全诗是“
千锤万凿出深山,烈火焚烧若等闲。粉身碎骨浑不怕,要留清白在人间。”第二句描述的是碳酸钙分解,生成物是氧化钙,第三句是氧化钙溶于水,生成物为氢氧化钙,第四句描述的是氢氧化钙在空气中与二氧化碳反应,Ca(OH)2+CO2===CaCO3↓+H2O,故“清白”是指碳酸钙,A项错误;《咏煤炭》中描述的是煤炭的开采,“乌金”的主要成分是煤炭,B项正确;硫黄、硝石(硝酸钾)、草木灰按一定的比例混合可制成火药,C项正确;“裘”是动物的皮毛,主要成分为蛋白质,D项正确。]
题型2 以传统文化为载体考查物质的性质及反应类型
4.《本草经集注》中有如下描述:“其黄黑者名鸡屎矾,不入药,惟堪镀作以合熟铜。投苦酒中,涂铁皆作铜色。外虽铜色,内质不变。”其中“鸡屎矾”指的是碱式碳酸铜或碱式硫酸铜,“苦酒”指的是CH3COOH溶液。文中没有涉及的化学反应类型是 ( )
A.置换反应 B.离子反应
C.复分解反应 D.化合反应
D [鸡屎矾在CH3COOH溶液中溶解,其中碱式碳酸铜(或碱式硫酸铜)与乙酸的反应是复分解反应,也是离子反应,Fe与Cu2+的反应是置换反应,也是离子反应,故文中没有涉及的化学反应类型是化合反应,D项正确。]
5.中华民族历史悠久,在浩瀚的历史文明中有许多关于化学的记载。下列说法不合理的是( )
选项
古代文献
记载内容
涉及原理
A
《淮南万毕术》
“曾青得铁则化为铜”
活泼金属置换不活泼金属
B
《鹤林玉露·一钱斩吏》
“一日一钱,千日千钱,绳锯木断,水滴石穿”
不涉及化学变化
C
《天工开物》
“凡火药,硫为纯阳,硝为纯阴”
纯阴指化合价降低,利用硝酸钾的氧化性
D
《肘后备急方》
“青蒿一握,以水二升渍,绞取汁”
利用物理方法提取青蒿素
B [选项A,“曾青得铁则化为铜”描述的是铁和硫酸铜反应生成硫酸亚铁和铜,铁的活泼性强于铜,A项合理;选项B,“水滴石穿”
是石灰石和水、二氧化碳反应生成碳酸氢钙的过程,反应方程式为CaCO3+CO2+H2O===Ca(HCO3)2,属于化学变化,B项不合理;选项C,硝酸钾、硫在一定条件下发生氧化还原反应,C项合理。]
题型3 以传统化工为载体,考查化学实验中的分离提纯
6.(2019·武汉模拟)三国时期曹植在《七步诗》中这样写道:“煮豆持作羹,漉豉以为汁。萁在釜下燃,豆在釜中泣。”文中“漉”涉及的化学实验基本操作是( )
A.蒸馏 B.分液
C.过滤 D.升华
C [煮豆持作羹,漉豉以为汁的意思是豆子煮熟后,把豆子的残渣过滤出去,留下豆汁来作羹。“漉”涉及的化学实验基本操作是过滤。]
7.(2019·长沙模拟)下列对古文献记载内容理解错误的是( )
A.《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之”。“瓦”,传统无机非金属材料,主要成分为硅酸盐
B.《本草纲目》“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也”。这里所用的“法”是指蒸馏
C.《本草纲目》中记载:“此即地霜也。所在山泽,冬月地上有霜,扫取以水淋汁,后乃煎炼而成”。文中对硝酸钾的提取涉及升华操作
D.《本草经集注》有记载:“以火烧之紫青烟起,云是真消石也”,区分硝石(KNO3)和朴硝(Na2SO4)利用了焰色反应
C [制瓦的原料是“无沙粘土”,其主要成分是硅酸盐,A项正确;根据“蒸令气上”可知“法”是指蒸馏,B项正确;文中对硝酸钾的提取涉及的操作有溶解、蒸发、结晶,没有涉及升华,C项错误;钠的焰色为黄色,钾的焰色为紫色(需透过蓝色钴玻璃观察),D项正确。]
8.(2019·广州测试)《本草纲目》记载:“烧酒……用浓酒和糟入甑,蒸令气上,用器承取滴露”,“凡酸坏之酒,皆可蒸烧”。这里用到的实验方法可以用于分离( )
A.丁醇与乙醚 B.碘化钾与碘
C.硝酸钾与氯化钠 D.氯化铵与硫酸钠
A
[题述实验方法为蒸馏,适合分离沸点不同且互溶的液态混合物。丁醇与乙醚均为有机物且互为同分异构体,二者互溶,但丁醇分子间可形成氢键,其沸点比乙醚高,两者可以用蒸馏的方法分离,A项正确;可以将碘化钾与碘的混合物先加入四氯化碳(碘溶于四氯化碳,碘化钾不溶于四氯化碳),再过滤,从而使两者分离,B项错误;硝酸钾与氯化钠为固体混合物,且溶解度随温度的变化程度不同,可以用重结晶的方法分离,C项错误;氯化铵与硫酸钠为固体混合物,可以利用氯化铵加热不稳定来分离,D项错误。]
化学与传统文化的试题解题模板
第一步——读题:对于陌生度较高的信息要做到逐字逐句阅读,挖掘关键字,排除干扰信息,找出有效信息。
第二步——联题:在读题的基础上,结合题目中的问题或选项分析本题考查的知识板块,联系中学化学知识体系,寻找要提取的信息。
第三步——析题:找到需要的信息后,需进行分析。分析时要从大脑信息库中迅速提取所需要的知识,并使思维从新情境回归到课本、回归到平时的学习中来。
第四步——解题:解题时要注意根据题目的要求回答相应问题。
1.(2019·全国卷Ⅱ,T7)“春蚕到死丝方尽,蜡炬成灰泪始干”是唐代诗人李商隐的著名诗句,下列关于该诗句中所涉及物质的说法错误的是( )
A.蚕丝的主要成分是蛋白质
B.蚕丝属于天然高分子材料
C.“蜡炬成灰”过程中发生了氧化反应
D.古代的蜡是高级脂肪酸酯,属于高分子聚合物
D [A项,蚕丝的主要成分是蛋白质,正确;B项,蚕丝属于天然高分子材料,正确;C项,蜡烛燃烧属于氧化还原反应,正确;D项,高级脂肪酸酯不属于高分子聚合物,错误。]
2.(2018·全国卷Ⅱ,T7)化学与生活密切相关。下列说法错误的是( )
A.碳酸钠可用于去除餐具的油污
B.漂白粉可用于生活用水的消毒
C.氢氧化铝可用于中和过多胃酸
D.碳酸钡可用于胃肠X射线造影检查
D [Na2CO3溶液水解呈碱性,油污在碱性条件下能发生水解反应,A项正确;漂白粉的有效成分为Ca(ClO)2,Ca(ClO)2溶于水生成HClO,HClO具有杀菌消毒作用,故可用于生活用水的杀菌消毒,B项正确;胃酸的主要成分为盐酸,可用Al(OH)3进行中和,C项正确;BaCO3能与胃酸反应生成Ba2+,Ba2+为重金属离子,能引起蛋白质变性,D项错误。]
3.(2018·全国卷Ⅲ,T7)化学与生活密切相关。下列说法错误的是( )
A.泡沫灭火器可用于一般的起火,也适用于电器起火
B.疫苗一般应冷藏存放,以避免蛋白质变性
C.家庭装修时用水性漆替代传统的油性漆,有利于健康及环境
D.电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法
A [泡沫灭火器喷出的泡沫中含有大量水分,H2O能导电,且H2O也易损坏电器,因此泡沫灭火器不适用于电器起火,A项错误;疫苗的主要成分是蛋白质,高温下蛋白质易变性而失去活性,所以疫苗要冷藏存放,B项正确;水性漆与传统的油性漆相比,水性漆具有低甲醛和低芳香类化合物等优点,属于环保产品,C项正确;活泼金属镁易失去电子,形成原电池时为负极,电热水器内胆(Ag)被保护,此为牺牲阳极的阴极保护法,D项正确。]
4.(2017·全国卷Ⅰ,T8)《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是( )
A.蒸馏 B.升华
C.干馏 D.萃取
B [根据题中所述操作及现象可知,文中涉及的操作方法为升华。]
5.(2015·全国卷Ⅰ,T7)我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿滴,惟玻璃可盛。”这里的“强水”是指( )
A.氨水 B.硝酸
C.醋 D.卤水
B [A.氨水有一定的腐蚀作用,对铜的腐蚀比较强,对钢铁腐蚀比较差,对水泥腐蚀不大,氨水可以贮存于塑料、陶瓷等容器中,故A不正确。B.硝酸化学性质活泼,能与多种物质反应,它是一种强氧化剂,它可腐蚀各种金属(铂和金除外)和材料,故B正确。C.醋具有弱酸性,具有酸的通性,没有强氧化性,不能腐蚀“五金八石”,醋酸也可贮存于塑料瓶,故C不正确。D.卤水又称作卤碱,其主要成分为氯化镁、氯化钠和一些金属离子,是制作食盐过程中渗滤出来的液体,在日常生活中常用于制作豆腐,大量吞服卤水可引起消化道腐蚀,镁离子被人体吸收后对心血管及神经系统均有抑制作用,故D不正确。]
相关文档
- 2020届高考化学一轮复习化学平衡状2021-07-086页
- 2020届高考化学一轮复习化学实验基2021-07-0814页
- 2019届高考化学一轮复习化学反应与2021-07-0821页
- 2020届高三化学一轮复习化学实验综2021-07-0810页
- 2020届高考化学一轮复习化学能和热2021-07-0814页
- 2021届(鲁科版)高考化学一轮复习化学2021-07-0811页
- 2020届高考化学一轮复习化学反应速2021-07-0813页
- 2020版高考一轮复习化学通用版学案2021-07-0811页
- 2020届高考化学一轮复习化学反应速2021-07-0816页
- 2020届高考化学一轮复习化学平衡图2021-07-0825页