- 351.50 KB
- 2021-07-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
四川省仁寿第一中学北校区 2019-2020 学年高一下学期期末
模拟理综-试题
7.化学与生活密切相关,下列说法不正确的是( )
A.饮用牛奶和豆浆可以缓解重金属引起的中毒
B.向煤中加入适量石灰石,可减少其燃烧产物中的 SO2,降低对大气的污染
C.食品包装袋、食物保鲜膜等材料的主要成分是聚氯乙烯
D.单质硅是将太阳能转变为电能的常用材料
8.下列实验操作能达到实验目的的是( )
选项 实验操作 实验目的
A 将 Fe(NO3)2 样品溶于稀 H2SO4 后,滴
加 KSCN 溶液,观察溶液是否变红
检验 Fe(NO3)2 晶体是否已氧化变质
B 将 CO2 通入水玻璃溶液中 证明 C 元素的非金属性大于 Si
C 向乙酸和乙酸乙酯的混合溶液中加入
足量的 NaOH 溶液,充分反应后蒸馏
除去乙酸乙酯中混有的乙酸
D 淀粉与稀 H2SO4 共热,再加入银氨溶
液水浴加热
验证淀粉水解产物有无还原性
9.氨气是一种重要的化工产品,是生产尿素的原料。工业合成氨的反应如下:
N2(g) +3H2(g) 2NH3(g) 反应放热 92.4KJ 1mol N-H 键断裂吸收的能量为( )
A. 391KJ B .782KJ C. 195.5K J D.100KJ
10. X、Y、Z 是 3 种短周期元素,其中 X、Y 位于同一主族,Y、Z 处于同一周期.X 原子
的最外层电子数是其电子层数的 3 倍.Z 原子的核外电子数比 Y 原子少.下列说法正确的
是( )
A.元素非金属性由弱到强的顺序为 X<Y<Z
B.Y 元素最高价氧化物对应水化物的化学式可表示为 H3YO4
C.3 种元素的气态氢化物中,Z 的气态氢化物最稳定
D.原子半径由大到小的顺序为 Z>Y>X
11. 已知 C +CO2==2CO,其
△
H>0,反应速率为υ1,N2+3H2==2NH3,其
△
H<0,反应速率
为υ2。对于上述反应,当温度升高时,υ1 和υ2 的变化情况为( )
A.同时增大 B.同时减小 C. υ1 增大, υ2 减小 D. υ1 减小, υ2 增大
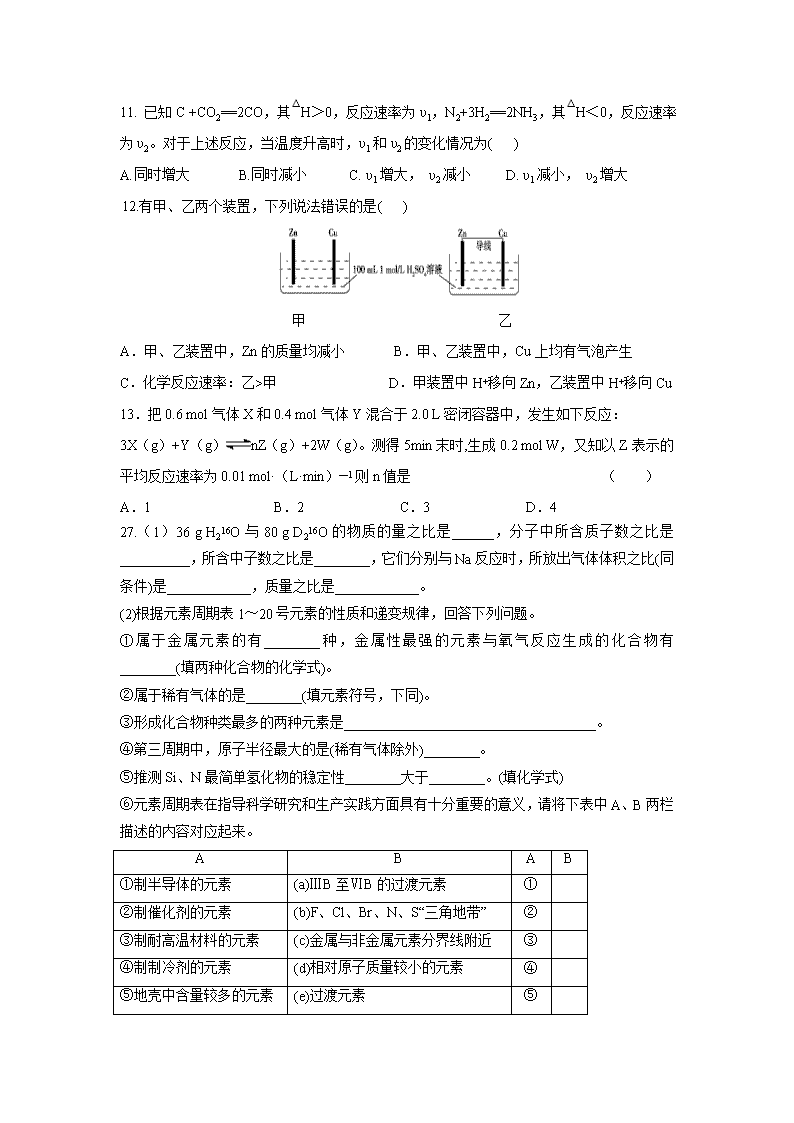
12.有甲、乙两个装置,下列说法错误的是( )
甲 乙
A.甲、乙装置中,Zn 的质量均减小 B.甲、乙装置中,Cu 上均有气泡产生
C.化学反应速率:乙>甲 D.甲装置中 H+移向 Zn,乙装置中 H+移向 Cu
13.把 0.6 mol 气体 X 和 0.4 mol 气体 Y 混合于 2.0 L 密闭容器中,发生如下反应:
3X(g)+Y(g) nZ(g)+2W(g)。测得 5min 末时,生成 0.2 mol W,又知以 Z 表示的
平均反应速率为 0.01 mol·(L·min)—1 则 n 值是 ( )
A.1 B.2 C.3 D.4
27.(1)36 g H216O 与 80 g D216O 的物质的量之比是______,分子中所含质子数之比是
__________,所含中子数之比是________,它们分别与 Na 反应时,所放出气体体积之比(同
条件)是____________,质量之比是____________。
(2)根据元素周期表 1~20 号元素的性质和递变规律,回答下列问题。
①属于 金属元 素的有 ________种, 金属性 最强的 元素与 氧气 反应生 成的化 合物有
________(填两种化合物的化学式)。
②属于稀有气体的是________(填元素符号,下同)。
③形成化合物种类最多的两种元素是____________________________________。
④第三周期中,原子半径最大的是(稀有气体除外)________。
⑤推测 Si、N 最简单氢化物的稳定性________大于________。(填化学式)
⑥元素周期表在指导科学研究和生产实践方面具有十分重要的意义,请将下表中 A、B 两栏
描述的内容对应起来。
A B A B
①制半导体的元素 (a)ⅢB 至ⅥB 的过渡元素 ①
②制催化剂的元素 (b)F、Cl、Br、N、S“三角地带” ②
③制耐高温材料的元素 (c)金属与非金属元素分界线附近 ③
④制制冷剂的元素 (d)相对原子质量较小的元素 ④
⑤地壳中含量较多的元素 (e)过渡元素 ⑤
28.氢能是理想的清洁能源。科学家通过化学方法使能量按人们所期望的形式转化,从而
提高能源的利用率。
(1)氢气在燃烧时,放出大量热量,说明该反应是________反应(填“放热”或“吸热”);这
是由于反应物的总能量___生成物的总能量(填“大于”或“小于”);从化学反应的本质角度来
看,是由于断裂反应物中的化学键吸收的总能量___________形成产物的化学键放出的总能
量(填“大于”或“小于”)。
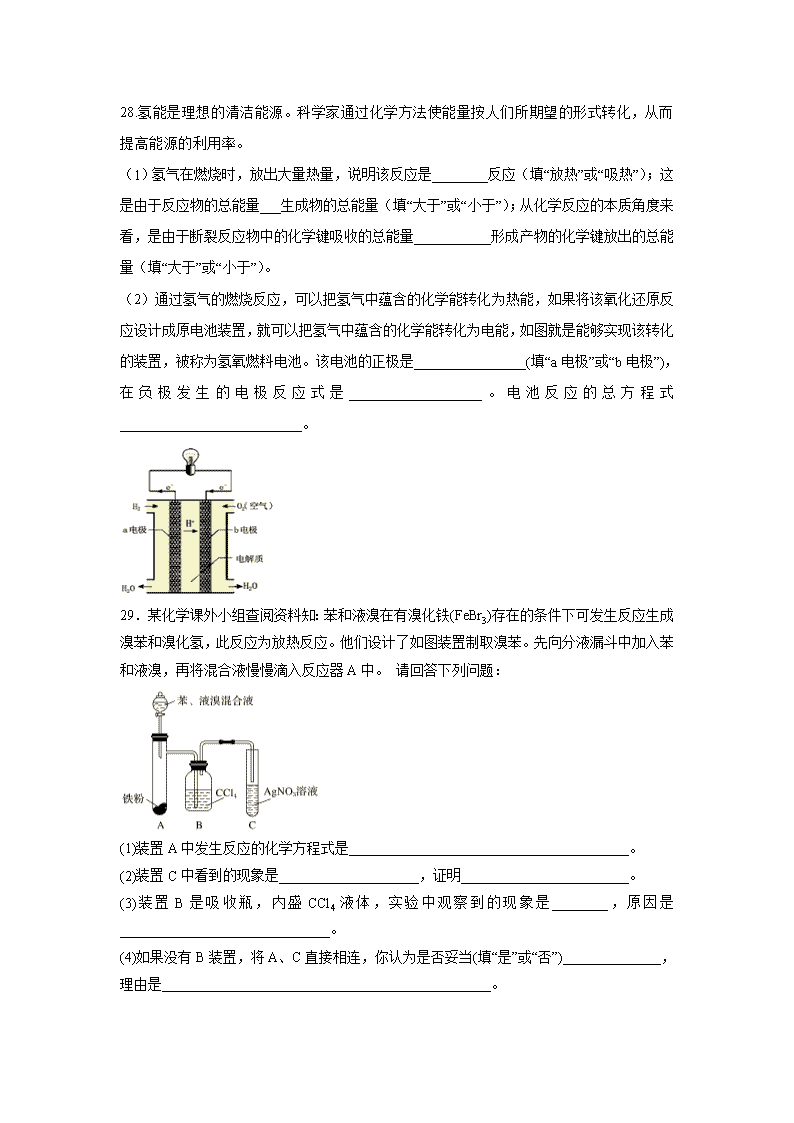
(2)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反
应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,如图就是能够实现该转化
的装置,被称为氢氧燃料电池。该电池的正极是________________(填“a 电极”或“b 电极”),
在 负 极 发 生 的 电 极 反 应 式 是 ___________________ 。 电 池 反 应 的 总 方 程 式
__________________________。
29.某化学课外小组查阅资料知:苯和液溴在有溴化铁(FeBr3)存在的条件下可发生反应生成
溴苯和溴化氢,此反应为放热反应。他们设计了如图装置制取溴苯。先向分液漏斗中加入苯
和液溴,再将混合液慢慢滴入反应器 A 中。 请回答下列问题:
(1)装置 A 中发生反应的化学方程式是________________________________________。
(2)装置 C 中看到的现象是____________________,证明________________________。
(3) 装 置 B 是 吸 收 瓶 , 内 盛 CCl4 液 体 , 实 验 中 观 察 到 的 现 象 是 ________ , 原 因 是
______________________________。
(4)如果没有 B 装置,将 A、C 直接相连,你认为是否妥当(填“是”或“否”)______________,
理由是_______________________________________________。
(5)实验完毕后将 A 试管中的液体倒在装有冷水的烧杯中,烧杯________层(填“上”或“下”)
为溴苯。
30.有机物 A 是基本的有机化工原料,A 与 CO、H2O 以物质的量 1:1:1 的比例生成 B。B、
C 两物质中的官能团分别具有乙酸、乙醇中官能团的性质。D 是有芳香味、不溶于水的油状
液体。有关物质的转化关系如下:请回答:
(1)A 的结构简式____________________________
(2)B + C → D 的化学方程式_______________________________________
(3)下列说法不正确的是__________________
A.有机物 A 能使酸性高锰酸钾溶液褪色
B.有机物 B 与乙酸互为同系物
C.有机物 B、C 都能与金属钠反应,且等物质的量的 B、C 与足量钠反应产生氢气质量相
等
D.可用 NaOH 溶液来除去有机物 D 中混有的杂质 B
(4)NO 是一种剧毒气体,但近年来发现许多生物体组织中存在少量 NO,它有扩张血管、
免疫、增强记忆的功能,因而成为当前生命科学的研究热点。
①写出自然界形成 NO 的化学方程式:____________________________________。
②NO 在大气层中可发生反应:NO+O3===NO2+O ①
NO2+O===NO+O2 ②
上述反应①中,NO 是________剂,上述反应②中,NO 是________产物。
【参考答案】
7-13 CBAD ABA