- 196.00 KB
- 2021-07-09 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
课时作业(九) 钠及其重要化合物
1.(2020·黑龙江哈尔滨月考)下面关于金属钠的描述正确的是( )
A.钠在自然界里以游离态或化合态形式存在
B.钠离子和钠原子都具有较强的还原性
C.等质量的钠分别与足量氧气反应生成Na2O和Na2O2时,转移电子的物质的量相等
D.钠和钾的合金于室温下呈固态,可作原子反应堆的导热剂
C [钠的化学性质很活泼,钠元素在自然界中以化合态存在,没有游离态,故A错误;钠原子容易失去电子,而钠离子只能得到电子,所以钠原子具有较强的还原性,而钠离子没有,故B错误;钠反应后均生成钠离子,因此等质量的钠与足量氧气反应,无论生成氧化钠还是过氧化钠,转移电子的物质的量相同,故C正确;钠和钾的合金熔点低,常温下为液态,具有良好的导热性,可作原子反应堆的导热剂,故D错误。]
2.(220·江西新余模拟)下列有关Na2O2的说法不正确的是( )
A.向包有Na2O2粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明Na2O2与H2O反应放热且有氧气生成
B.Na2O2与CO2反应时有单质O2生成,该反应属于置换反应
C.Na2O2在空气中久置变白,涉及的氧化还原反应中,Na2O2既是氧化剂,又是还原剂
D.Na2O2粉末加入Ca(HCO3)2溶液中,会产生气体和浑浊
B [A项,燃烧的条件是达到着火点和具有助燃物质;B项,反应物中没有单质参加反应,不符合置换反应的定义;C项,Na2O2与CO2、H2O的反应都是Na2O2自身的氧化还原反应;D项,Na2O2先和水反应生成O2和NaOH,NaOH再与Ca(HCO3)2反应产生沉淀CaCO3。]
3.(2020·吉林百校联盟联考)分别向CuSO4溶液和FeSO4溶液中加入等量的金属钠,下列说法一定正确的是( )
A.两溶液中均有金属单质析出
B.CuSO4溶液中最终有蓝色沉淀生成
C.FeSO4溶液中最终有白色沉淀生成
D.钠在CuSO4溶液中的反应更剧烈
B [钠是活泼的金属,投入盐溶液中首先与水反应生成氢氧化钠和氢气,因此两溶液中均没有金属单质析出,A错误;CuSO4溶液中最终有蓝色沉淀氢氧化铜生成,B正确;FeSO4溶液中首先产生氢氧化亚铁白色沉淀,最终转化为红褐色沉淀氢氧化铁,C错误;钠在溶液中反应的剧烈程度与溶液中的氢离子浓度有关,不能确定两溶液中的氢离子浓度,因此不能比较二者反应的剧烈程度,D错误。]
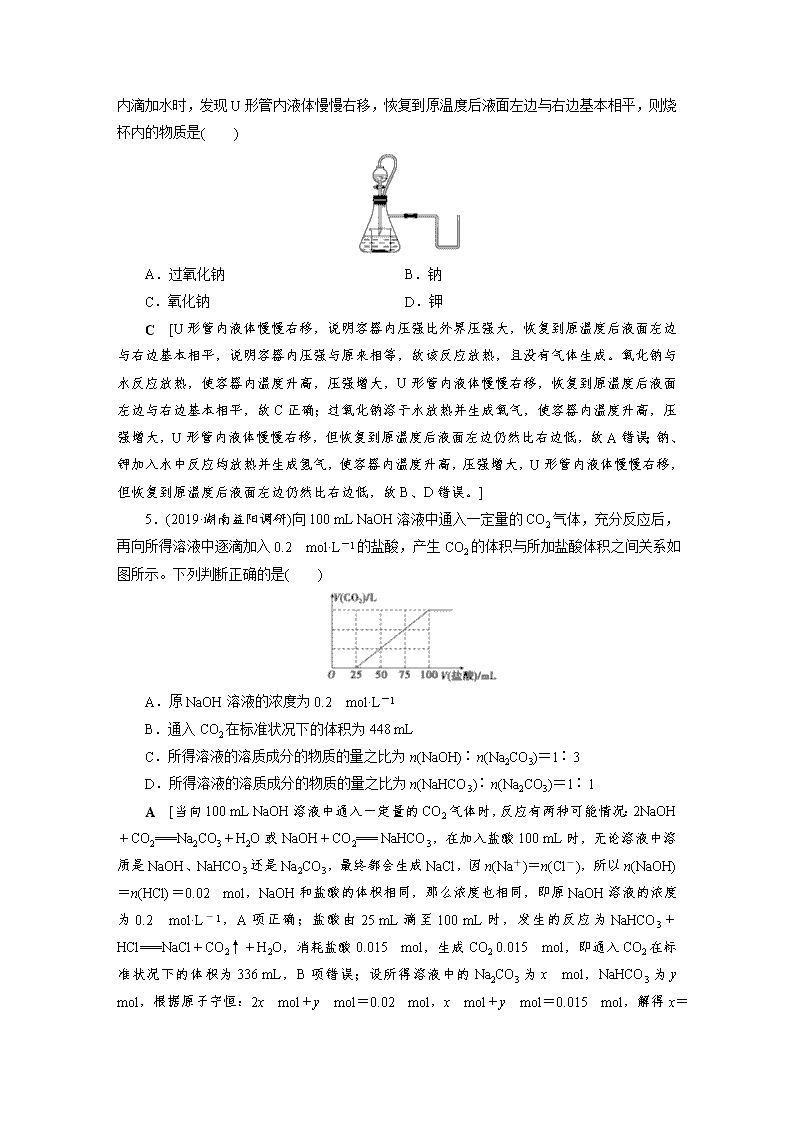
4.(2018·江西新余二模)如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,
向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则烧杯内的物质是( )
A.过氧化钠 B.钠
C.氧化钠 D.钾
C [U形管内液体慢慢右移,说明容器内压强比外界压强大,恢复到原温度后液面左边与右边基本相平,说明容器内压强与原来相等,故该反应放热,且没有气体生成。氧化钠与水反应放热,使容器内温度升高,压强增大,U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,故C正确;过氧化钠溶于水放热并生成氧气,使容器内温度升高,压强增大,U形管内液体慢慢右移,但恢复到原温度后液面左边仍然比右边低,故A错误;钠、钾加入水中反应均放热并生成氢气,使容器内温度升高,压强增大,U形管内液体慢慢右移,但恢复到原温度后液面左边仍然比右边低,故B、D错误。]
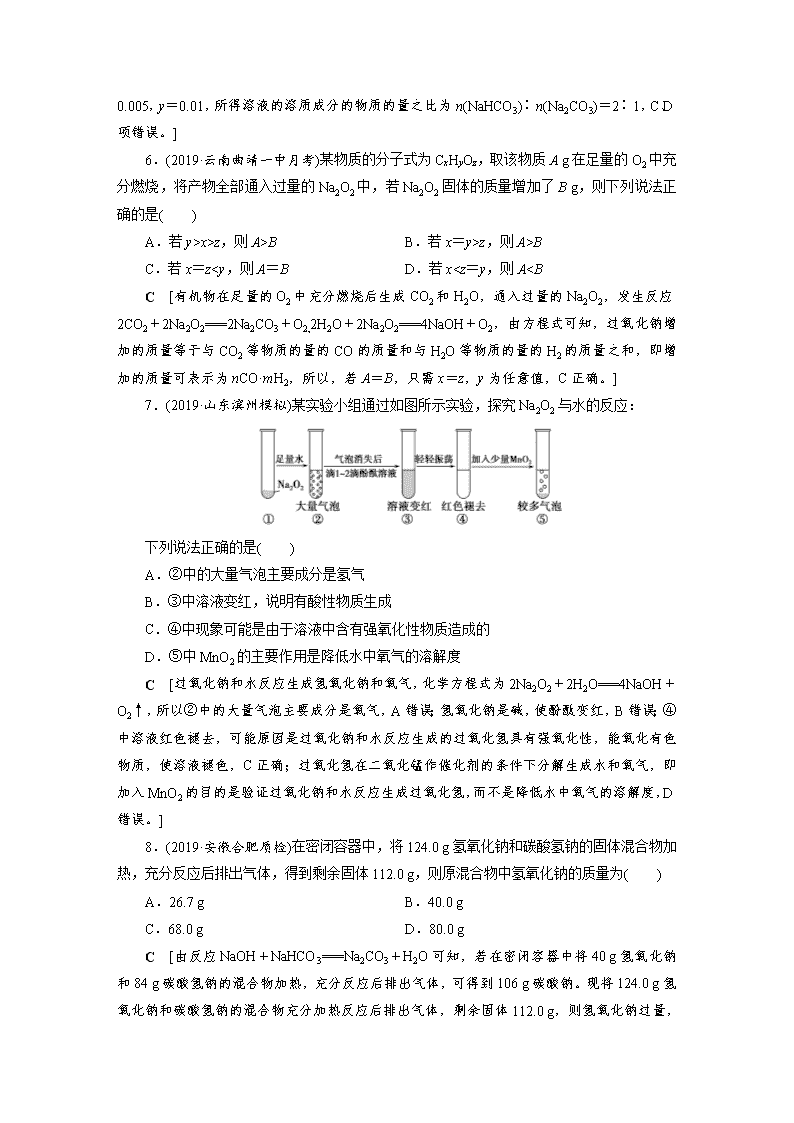
5.(2019·湖南益阳调研)向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol·L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。下列判断正确的是( )
A.原NaOH溶液的浓度为0.2 mol·L-1
B.通入CO2在标准状况下的体积为448 mL
C.所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3
D.所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3)=1∶1
A [当向100 mL NaOH溶液中通入一定量的CO2气体时,反应有两种可能情况:2NaOH+CO2===Na2CO3+H2O或NaOH+CO2=== NaHCO3,在加入盐酸100 mL时,无论溶液中溶质是NaOH、NaHCO3还是Na2CO3,最终都会生成NaCl,因n(Na+)=n(Cl-),所以n(NaOH)=n(HCl)=0.02 mol,NaOH和盐酸的体积相同,那么浓度也相同,即原NaOH溶液的浓度为0.2 mol·L-1,A项正确;盐酸由25 mL滴至100 mL时,发生的反应为NaHCO3+HCl===NaCl+CO2↑+H2O,消耗盐酸0.015 mol,生成CO2 0.015 mol,即通入CO2在标准状况下的体积为336 mL,B项错误;设所得溶液中的Na2CO3为x mol,NaHCO3为y mol,根据原子守恒:2x mol+y mol=0.02 mol,x mol+y mol=0.015 mol,解得x
=0.005,y=0.01,所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3)=2∶1,C、D项错误。]
6.(2019·云南曲靖一中月考)某物质的分子式为CxHyOz,取该物质A g在足量的O2中充分燃烧,将产物全部通入过量的Na2O2中,若Na2O2固体的质量增加了B g,则下列说法正确的是( )
A.若y>x>z,则A>B B.若x=y>z,则A>B
C.若x=z