- 479.00 KB
- 2021-08-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
绝密★启封前
宁夏六盘山高级中学2020届高三第二次模拟考试
理 科 综 合 试 卷-化学
命题教师:
注意事项:
1.答题前,考生务必将自己的姓名、班级、考场、准考证号填写清楚。
2.选择题答案使用2B铅笔填涂,非选择题答案使用0.5毫米的黑色中性(签字)笔或碳素笔书写,字体工整,笔迹清楚。
3.做答时,务必将答案写在答题卡上,写在本试题上、超出答题区域或非题号对应区域的答案一律无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 P-31 S-32 Cl-35.5 Ca-40 Fe-56
7.科技发展离不开化学。下列说法不正确的是( )
A.“一带一路”,丝绸制品严禁用添加蛋白酶的洗衣粉漂洗
B.“乘风破浪”,航母上的钛合金铆钉可抗海水腐蚀
C.“筑梦天宫”,火箭助推剂——液氧在工业上可通过分解氯酸钾制得
D.“直上云霄”,客机所用燃油是石油的分馏产物
8. 下列指定反应的离子方程式正确的是
A.已知酸性的强弱顺序:,则向溶液中通入少量的时:
B.在澄清石灰水中加入少量碳酸氢镁溶液:Ca2++OH-+HCO===CaCO3↓+H2O
C.侯氏制碱法:NaCl +NH3 +CO2 + H2O =NaHCO3 + NH4+
D.室温下用稀NaOH溶液吸收Cl2:Cl2+2OH−=ClO−+Cl−+H2O
9.短周期主族元素W、X、Y、Z的原子序数依次增大。W的某种核素不含中子;X、Y原子核外L层的电子数之比为3︰4;X与Z同主族,且X、Y、Z原子的最外层电子数之和为16。下列说法不正确的是( )
A.W、X、Z三种元素形成的化合物一定为强电解质
B.简单氢化物的稳定性:X>Z>Y
C.X分别可与W、Z各形成两种常见化合物
D.原子半径:Y>Z>X>W
10.关于化合物二苯基甲烷(),下列说法正确的是( )
A.分子式C13H14 B.是苯的同系物
C.其一氯代物有4种 D.所有碳原子一定共平面
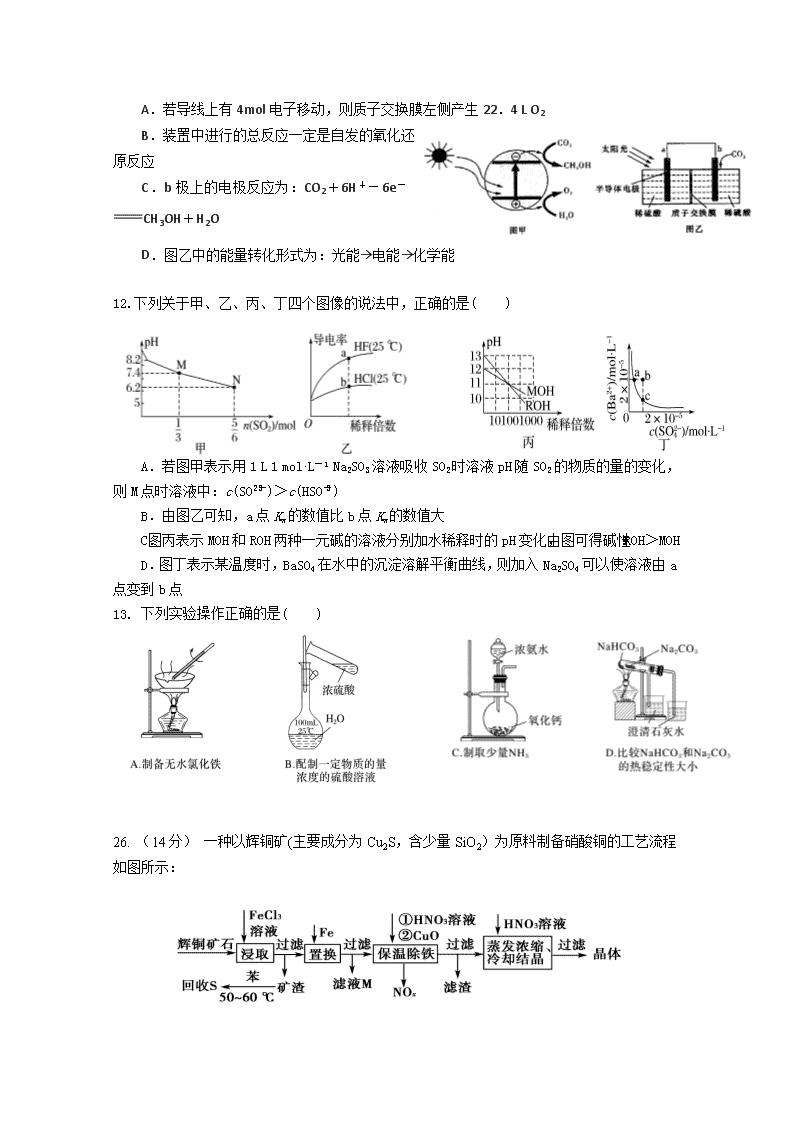
11、半导体光催化CO2机理如图甲所示,设计成电化学装置如图乙所示,则下列说法正确的是( )
A.若导线上有4mol电子移动,则质子交换膜左侧产生22.4 L O2
B.装置中进行的总反应一定是自发的氧化还原反应
C.b极上的电极反应为:CO2+6H+-6e-CH3OH+H2O
D.图乙中的能量转化形式为:光能→电能→化学能
12.下列关于甲、乙、丙、丁四个图像的说法中,正确的是( )
A.若图甲表示用1 L 1 mol·L-1 Na2SO3溶液吸收SO2时溶液pH随SO2的物质的量的变化,则M点时溶液中:c(SO)>c(HSO)
B.由图乙可知,a点Kw的数值比b点Kw的数值大
C.图丙表示MOH和ROH两种一元碱的溶液分别加水稀释时的pH变化,由图可得碱性:ROH>MOH
D.图丁表示某温度时,BaSO4在水中的沉淀溶解平衡曲线,则加入Na2SO4可以使溶液由a点变到b点
13. 下列实验操作正确的是( )
26. (14分) 一种以辉铜矿(主要成分为Cu2S,含少量SiO2)为原料制备硝酸铜的工艺流程如图所示:
(1)写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:_________________________。
(2)恒温“浸取”的过程中发现铜元素的浸取速率先增大后减少,有研究指出CuCl2是该反应的催化剂,该过程的反应原理可用化学方程式表示为:①Cu2S +2CuCl2=4CuCl+S;②________________________。
(3)“回收S”过程中温度控制在50~60℃之间,不宜过高的原因是________________________。
(4)向滤液M中加入(或通入)_________(填字母),可得到一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾 d.氯化氢
(5)“保温除铁”过程中,加入CuO的目的是________________;“蒸发浓缩、冷却结晶”过程中,要用HNO3溶液调节溶液的pH,其理由_____________________________。
(6)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见图,转化时转移0.2mol电子,生成Cu2S__________mol。
27.(14分)TiO2和TiCl4均为重要的化工原料,已知:
Ⅰ.TiCl4(g) + O2(g) TiO2(s) + 2Cl2(g) ΔH =-175.4 kJ/mol
Ⅱ.2C(s) + O2(g) 2CO(g) ΔH =-220.9 kJ/mol
请回答下列问题:
(1)TiCl4(g)+2CO(g)TiO2(s)+2C(s)+2Cl2(g) 的ΔH = kJ/mol
(2)toC时,向10L恒容密闭容器中充入1mol TiCl4和2molO2,发生反应I,4min达到平衡时测得TiO2的物质的量为0.2mol。
① 反应4min末的平均速率v(Cl2)= ,该温度下K =____(用分数表示),O2的平衡转化率=_______.
② 下列措施,既能加快正反应速率,又能增大O2的平衡转化率的是
A.缩小容器的体积 B.加入催化剂 C.分离出部分TiO2
D.增加O2的浓度 E.减低温度 F.以上方法均不可以
a
b
a%
M
L1
L2
a
③ toC时,向10L恒容密闭容器中充入3molTiCl4和一
定量的O2,发生反应I,两种气体的平衡转化率(a%)与起始的物质的量之比(TiCl4/O2)的关系如图所示:能表示O2的平衡转化率的曲线为_________ (填“L1”或“L2”)M点的坐标为______________(用整数或分数表示)
(3)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在NH4HCO3溶液中:c(NH)_____c(HCO)(填“>”、“<”或“=”);反应NH+HCO+H2ONH3·H2O+H2CO3的平衡常数K=_________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10−7mol·L−1,K2
=4×10−11mol·L−1)
28.(15分) 三氯氧磷(POCl3)是一种工业化工原料,可用于制取有机磷农药、长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O2和PCl3为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):
已知PCl3和三氯氧磷的性质如表:
熔点/℃
沸点/℃
其他物理或化学性质
PCl3
-112.0
76.0
PCl3和POCl3互溶,均为无色液体,遇水均剧烈水解,发生复分解反应生成磷的含氧酸和HCl
POCl3
1.25
106.0
(1)装置A中的分液漏斗能否用长颈漏斗代替?做出判断并分析原因:_______
(2)装置B的作用是______________(填标号)。
a.气体除杂 b.加注浓硫酸 c.观察气体流出速度 d.调节气压
(3)仪器丙的名称是___________,实验过程中仪器丁的进水口为__________(填“a”或“b”)口。
(4)写出装置C中发生反应的化学方程式 ,该装置中用温度计控制温度为60~65 ℃,原因是 。
(5)称取16.73 g POCl3样品,配制成100 mL溶液;取10.00 mL溶液于锥形瓶中,加入3.2 mol·L-1的AgNO3溶液10.00 mL,并往锥形瓶中滴入5滴Fe2(SO4)3溶液;用0.20 mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00 mL(已知:Ag++SCN-=AgSCN↓)。则加入Fe2(SO4)3溶液的作用是________,样品中POCl3的纯度为_____________。
【化学——选修3】
35.(15分)2016年诺贝尔化学奖授予在“分子机器设计和合成”领域有突出成就的三位科学家,其研究对象之一“分子开关”即与大环主体分子苯芳烃、硫或氮杂环杯芳烃等有关。回答下列问题:
(1)对叔丁基杯[4]芳烃(如图Ⅰ所示)可用于ⅢB族元素对应离子的萃取,如La3+、Sc2+。写出基态二价钪离子(Sc2+)的核外电子排布式:____,其中电子占据的轨道数为_____个。
(2)对叔丁基杯[4]芳烃由4个羟基构成杯底,其中羟基氧原子杂化方式为_____,羟基间的相互作用力为 。
(3)不同大小的苯芳烃能识别某些离子,如:N3-、SCN−等。一定条件下,SCN−与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式_______。
(4)NH3分子在独立存在时H-N-H键角为106.7°。如图[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因: 。
(5) 橙红色的八羰基二钴[Co2(CO)8]的熔点为52℃,可溶于乙醇、乙醚、苯等有机溶剂。该晶体属于 晶体,八羰基二钴在液氨中被金属钠还原成四羰基钴酸钠[NaCo(CO)4],四羧基钴酸钠中含有的化学键为 。
(6)已知C60分子结构和C60晶胞示意图(如图Ⅱ、图Ⅲ所示):
图ⅡC60分子结构
图 ⅢC60晶胞示意图
a cm
则一个C60分子中含有σ键的个数为 ,C60晶体密度的计算式为 g·cm−3。(NA为阿伏伽德罗常数的值)
【化学——选修5】
36.(15分)有机物A是聚合反应生产胶黏剂基料的单体,亦可作为合成调香剂I、聚酯材料J的原料,相关合成路线如下:
已知:在质谱图中烃A的最大质荷比为118,其苯环上的一氯代物共三种,核磁共振氢谱显示峰面积比为3:2:2:2:1。
根据以上信息回答下列问题:
(1)A的官能团名称为__________________,B→C的反应条件为_____________,E→F的反应类型为_____________。
(2)I的结构简式为____________________,若K分子中含有三个六元环状结构,则其分子式为________________。
(3)D与新制氢氧化铜悬浊液反应的离子方程式为_______________________________。
(4)H的同分异构体W能与浓溴水反应产生白色沉淀,1 mol W参与反应最多消耗3 mol Br2,请写出所有符合条件的W的结构简式___________________________________。
(5)J是一种高分子化合物,则由C生成J的化学方程式为_____________________________________
宁夏六盘山高级 中学
2019- -2020 学年第二学期高三第二次模拟测试卷答案
7
8
9
10
11
12
13
C
D
A
C
D
C
C
26(14分)
(1)Cu2S+4Fe3+=2Cu2++4Fe2++S (2分)
(2)CuCl+FeCl3=CuCl2+FeCl2(2分)
(3)温度高苯容易挥发 (2分)
(4)b(2分)
(5)调节溶液的pH,使铁完全转化为Fe(OH)3沉淀 (2分) 抑制Cu2+的水解(2分)
(6)0.2(2分)
27 .(14分)
(1)+45.5kJ/mol(1分)
(2)0.01 mol/(L∙min) (1分) (1分) 10%(1分) F (2分) L1 (2分)
(1, ) (2分)
(3)>(2分) 1.25×10−3 (2分
28(15分) (1) 否,长颈漏斗不能调节滴液速度 (2分) (2) acd (2分) (3). 三颈烧瓶 (2分) (4). a (2分) (5). 2PCl3+O2=2POCl3 (2分) (6). 温度过低反应速度过慢;温度过高,PCl3易挥发,利用率低 (2分) (7). 指示剂(1分) (8). 91.8%(2分)
35(15分) (1) 1s22s22p63s23p63d1或[Ar]3d1 (1分) 10 (1分) (2). sp3(1分) 氢键(1分) (3) N≡C—S—S—C≡N (1分) (4)氨分子与Zn2+形成配合物后,孤对电子与Zn2+成键,原孤对电子与键对电子间的排斥作用变为键对电子间的排斥,排斥减弱,故H-N-H键角变大 (2分) (5) 分子 (2分) 离子键、配位键、极性键(2分) (6)90 (2分) 4×12×60/(a3×NA) (2分)
36( 15分 ) (1). 碳碳双键 (1分) 氢氧化钠水溶液,加热 (2分) 消去反应(2分) (2). (2分) C18H16O4 (2分) (3). (2分) (4)、 (2分) (5). (2分)
(或产物写成:)