- 158.50 KB
- 2021-08-24 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
化学试题卷
考试时间:100分钟 试卷总分:100分
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5
一、单选题(每小题3分,共48分)
1. 溶液、胶体和浊液这三种分散系的根本区别是( )
A. 能否发生丁达尔效应 B. 分散质粒子直径的大小
C. 能否透过滤纸或半透膜 D. 是否均一、透明、稳定
2.将下列各组物质按单质、氧化物、酸、碱、盐分类顺序排列,其中正确的是( )
A.银、水、硫酸、烧碱、纯碱
B.碘酒、冰、盐酸、烧碱、食盐
C.氢气、二氧化硫、硝酸、纯碱、硝酸钾
D.铜、氧化铜、醋酸、石灰水、苛性钠
3.下列说法中不正确的是( )
①由同一种元素组成的物质是单质
②阴离子一定不含金属元素,阳离子一定含金属元素
③金属氧化物一定是碱性氧化物
④碱性氧化物一定是金属氧化物
⑤非金属氧化物一定是酸性氧化物
⑥酸性氧化物一定是非金属氧化物
⑦酸的元数不一定等于酸分子中的H原子数
A.①②④⑤⑦ B.①③④⑤ C.①②③⑤⑥ D.③④⑤⑦
4. 下列情况与胶体性质有关的有( )
明矾净水 血液透析 在大江、大河的入海口处易形成三角洲 静电除尘 在雾天,打开车灯能看到一道粗的光柱
A. 2项 B. 3项 C. 4项 D. 全部都是
5.下列溶液中Cl﹣的物质的量浓度最大的是( )
A.1000mL2.5mol•L﹣1 NaCl溶液 B.200mL2mol•L﹣1MgCl2溶液
C.250mL1mol•L﹣1AlCl3溶液 D.300mL5mol•L﹣1FeCl3溶液
6.为除去某物质中所含的杂质,所选用的除杂试剂或操作方法正确的是( )
序号
物质
杂质
除杂试剂或操作方法
①
NaCl
Na2CO3
溶解,加入过量盐酸,蒸发
②
FeSO4溶液
CuSO4
加入过量铁粉并过滤
③
H2
CO2
依次通过盛有NaOH溶液和浓硫酸的洗气瓶
④
NaNO3
CaCO3
加稀盐酸、过滤、蒸发结晶
A. ①②③ B. ②③④ C. ①②④ D. ①②③④
7.下列叙述错误的是( )
A. 标准状况下,5LCH4气体与5L NH3气体的原子个数之比为5:4
B. 常温常压下,11.2LO3中所含氧原子个数小于1.5NA
C. 同温、同压下,相同体积的N2和CO气体具有相同的分子数和相同的密度
D. 同温、同压下,等质量的一氧化碳和二氧化碳的密度比为11:7
8.将10 mL 1 mol/LH2SO4溶液稀释到100 mL,关于稀释后的溶液,下列说法正确的是( )
A.H+的物质的量浓度为0.1 mol/L
B.SO42-的物质的量浓度为0.1 mol/L
C.所含H2SO4的物质的量为0.1 mol
D.取10 mL该溶液,H2SO4的物质的量浓度为0.01 mol/ L
9.实验室用氢氧化钠固体配制 1.00mol/L 的NaOH 溶液 480mL,以下配制步骤正确的是( )
A.直接在托盘天平上称取 19.2g 的氢氧化钠固体放入烧杯中,加蒸馏水溶解
B.待溶液冷却后,用玻璃棒引流,将烧杯中的溶液转移到容量瓶中,并洗涤烧杯、玻璃棒2~3次
C.定容时,仰视凹液面最低处到刻度线
D.按照上述步骤配制的溶液(没有涉及的步骤操作都正确),所得溶质的物质的量浓度偏高
10.我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人。这种做法的化学原因是
A. 胶体的电泳 B. 胶体的丁达尔效应
C. 胶体的布朗运动 D. 胶体的聚沉
11.某溶液中含有Cl-、CO32-、SO42-三种阴离子,如果只取一次溶液,分别将三种离子检验出来,下列加入试剂及其顺序(从左至右)正确的是( )
A.氯化钡溶液、硝酸、硝酸银溶液 B.硝酸、硝酸银溶液、氯化钡溶液
C.硝酸、硝酸钡溶液、硝酸银溶液 D.稀硫酸、硝酸钡溶液、硝酸银溶液
12.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L
B.物质的量浓度为0.5 mol/L的MgCl2溶液中含有NA个Cl-
C.标准状况下,11.2 L H2O含有的分子数为0.5 NA
D.在常温常压下,1.06 g Na2CO3含有的Na+数为0.02 NA
13.在相同的温度和压强下,4个容器中分别装有4种气体。已知各容器中的气体和容器的容积分别是:a、CO2:100mL;b、O2:200mL;c、N2:400mL;d、CH4:600mL。则4个容器中气体的质量由大到小的顺序是( )
A.c>d>b>a B.b>a>d>c C.a>b>c>d D.d>c>a>b
14.V L Al2(SO4)3溶液中含Al3+a g,将此溶液稀释到4V L,则稀释后溶的物质的量浓度是( )
A.mol·L−1 B. mol·L−1 C.mol·L−1 D. mol·L−1
15.在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述正确的是( )
a. 体积②>③>①>④ b. 密度②>③>④>①
c. 质量②>③>①>④ d. 氢原子个数①>③>④>②
A.abc B.bcd C.abd D.abcd
16.标准状况下,n L 气体溶于m mL 中,得密度为 的R L的氨水,则此氨水的物质的量浓度为( )
A. B .
C. D.
第II卷 非选择题(52分〕
17.(8分)现有下列9种物质:
纯碱 硫酸 ⑨CO
其中属于正盐的是________;属于酸性氧化物的是________。(填序号)
有关胶体的实验中:
实验室制备胶体的化学方程式为_____________。
将橘红色的硫化锑胶体,装入U型管,插入电极后通直流电,发现阳极附近橘红色加深,证明胶粒带________填“正”或“负”电荷。
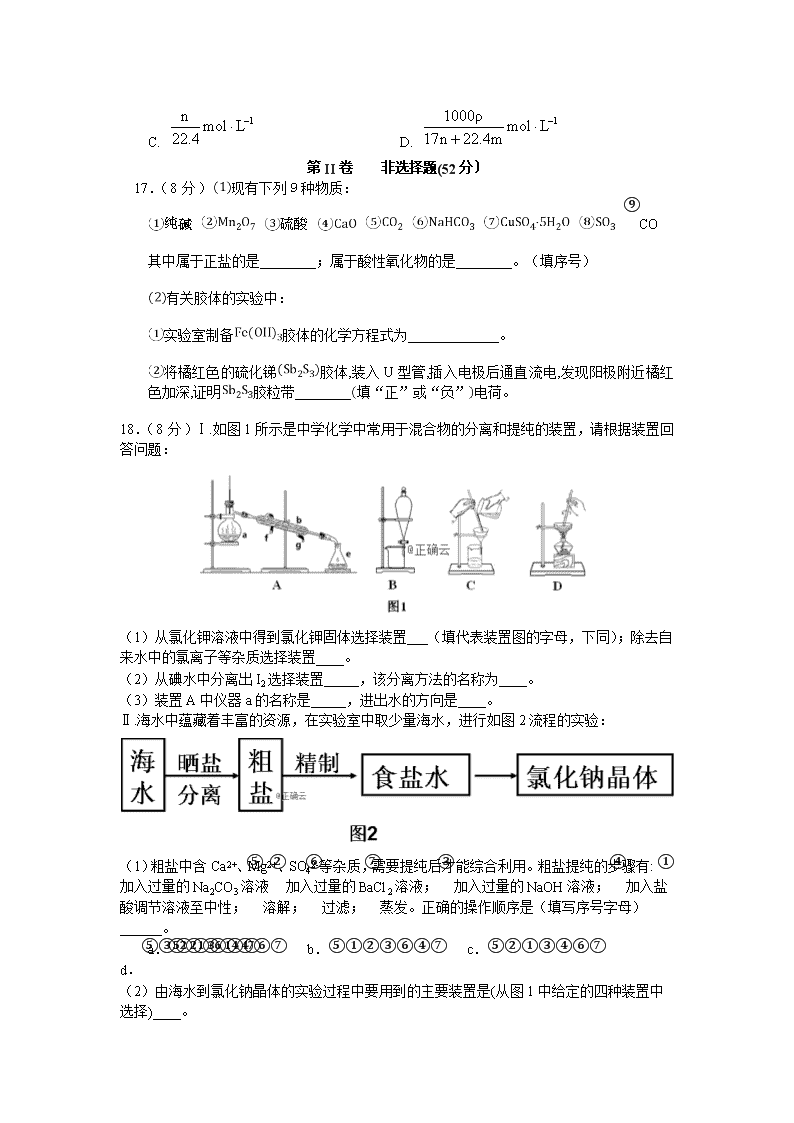
18.(8分)Ⅰ.如图1所示是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
(1)从氯化钾溶液中得到氯化钾固体选择装置___(填代表装置图的字母,下同);除去自来水中的氯离子等杂质选择装置____。
(2)从碘水中分离出I2选择装置_____,该分离方法的名称为____。
(3)装置A中仪器a的名称是_____,进出水的方向是____。
Ⅱ.海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如图2流程的实验:
(1)粗盐中含Ca2+、Mg2+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有: ①加入过量的Na2CO3溶液②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④加入盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是(填写序号字母)______。
a.⑤②③①④⑥⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(2)由海水到氯化钠晶体的实验过程中要用到的主要装置是(从图1中给定的四种装置中选择)____。
19.(12分)某同学需用480 mL 0.5 mol·L-1Na2CO3溶液,在实验室进行配制。
I.(1)该同学用托盘天平应称量________g Na2CO3粉末,使用容量瓶前必须进行的一步操作是______。
(2)下图是该同学配制的一些关键步骤和操作图。
配制过程的先后顺序为(用字母A~F填写)________________。
Ⅱ.若配制1mol/L的稀硫酸溶液500mL
(1)则需要质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为___________mL(计算结果保留一位小数)。如果实验室有10mL 、25mL、50mL量筒,应选用_____________mL规格的量筒最好。
(2)下面操作造成所配稀硫酸溶液浓度偏高的是( )
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
20.(14分)(1)与16gO2所含原子总数相同的NH3标准状况下体积是 L;
(2)已知2LAl2(SO4)3溶液中c(Al3+)=3mol/L,则c(SO42-)= ,与3L mol/LNa2SO4中SO42-的物质的量浓度相等。
(3)同温同压下,同体积的NH3和H2S气体的质量比为 ;同质量的NH3和H2S气体的体积比为 ;若二者氢原子数相等,它们的体积比为 。
(4)在标准状况下,8.96L的CH4和CO的混合气体,混合气体对氢气相对密度是9.5,混合气体平均摩尔质量为 ,混合气体中CH4的体积为 ,一氧化碳的质量分数为 ,二者原子个数比为 。
21.(10分)在0.24 L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。
(1)该混合液中,NaCl的物质的量为______mol,含溶质MgCl2的质量为________g。
(2)该混合液中CaCl2的物质的量为________mol,将该混合液加水稀释至体积为1200mL,稀释后溶液中Ca2+的物质的量浓度为______mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________mol。
参考答案
一、选择题(每题3分,共48分)
1.B
2.A
3.C
4.D
5.D
6.A
7.D
8.B
9.B
10.D
11.C
12.D
13.A
14.D
15. D
16.B
二、简答题(共52分)
17(8分). (2分);(2分)
胶体 (2分)
负 (2分)
18. (8分) D (1分) A (1分) B (1分) 萃取、分液 (1分)
蒸馏烧瓶(1分) 下进上出 (1分) d (1分) CD (1分)
19. (12分)I.(1)26.5 (2分) 检漏(2分) DBCAFE(2分) Ⅱ.(1)27.2(2分) 50 (2分) (2)A C D(2分)
18. (14分)(1)5.6(1分)
(2)4.5mol/L (1分) 4.5(1分)
(3)1:2 (1分) 2:1(1分) 2:3(1分)
(4)19g/mol (2分) 6.72L(2分) 36.8%(2分) 15:2(2分)
19. (10分)(1)0.24 (2分) 11.4(2分)
(2)0.12(2分) 0.1 (2分)
(3)0.72(2分)