- 151.73 KB
- 2021-08-24 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
课时规范练24 盐类的水解
(时间:45分钟 满分:100分)
一、选择题(本题共10小题,每小题5分,共50分,每小题只有一个选项符合题目要求)
1.25 ℃时,浓度均为1 mol·L-1的AX、BX、AY、BY四种正盐溶液,AX溶液的pH=7且溶液中c(X-)=1 mol·L-1,BX溶液的pH=4,BY溶液的pH=6。下列说法正确的是( )。
A.AY溶液的pH小于7
B.AY溶液的pH小于BY溶液的pH
C.电离平衡常数K(BOH)大于K(HY)
D.稀释相同倍数,BX溶液的pH变化大于BY溶液
答案:D
解析:25℃时,浓度为1mol·L-1的AX溶液的pH=7且溶液中c(X-)=1mol·L-1,则AX是强酸强碱盐,AOH是强碱,HX是强酸。BX溶液的pH=4,HX是强酸,则BX是强酸弱碱盐,BOH是弱碱。相同浓度时,若BY是强酸弱碱盐,则BX和BY溶液的pH应相等,实际上相同浓度时BX溶液的pH小于BY溶液的pH,则HY是弱酸,BY是弱酸弱碱盐,且B+的水解程度大于Y-。AY是强碱弱酸盐,Y-发生水解反应使其溶液显碱性,pH大于7,A项错误;AY溶液显碱性,BY溶液显酸性,显然前者的pH大于后者的pH,B项错误;BY是弱酸弱碱盐,且B+的水解程度大于Y-,离子的水解程度越大,对应电解质的电离程度则越小,故BOH的电离程度小于HY,则有电离平衡常数K(BOH)小于K(HY),C项错误;BX和BY是BOH形成的两种盐,而HX是强酸,HY是弱酸,稀释相同的倍数,BX溶液的pH变化大于BY溶液,D项正确。
2.(2019山东师大附中模拟)下列说法正确的是( )。
A.向CuCl2溶液中加入CaCO3,调节pH可除去溶液中混有的Fe3+
B.配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度
C.用加热的方法可以除去KCl溶液中少量的Fe3+
D.洗涤油污常用热的碳酸钠溶液
答案:D
解析:A项,由Fe3++3H2OFe(OH)3+3H+,加入CaCO3消耗H+,使平衡右移而除去Fe3+,但又引入新的杂质Ca2+,不合理;B项,所加酸应是稀硫酸,否则会引入新杂质;C项,加热法不能除去溶液中少量的Fe3+。
3.已知:常温下浓度为0.1 mol·L-1下列溶液的pH如表所示。下列有关说法不正确的是( )。
溶质
NaCl
Na2CO3
NaClO
NaHCO3
pH
7
11.6
9.7
8.3
A.在相同温度下,同浓度的三种酸溶液的导电能力:HCl>H2CO3>HClO
9
B.等体积等物质的量浓度的NaCl溶液与NaClO溶液中Cl-和ClO-离子个数:N(Cl-)>N(ClO-)
C.向Na2CO3溶液中逐滴滴入少量稀盐酸,反应为:Na2CO3+2HCl2NaCl+CO2↑+H2O
D.若将CO2通入0.1 mol·L-1 Na2CO3溶液至溶液呈中性,则溶液中:2c(CO32-)+c(HCO3-)=0.2 mol·L-1
答案:C
解析:由0.1mol·L-1NaCl、NaClO、NaHCO3溶液pH的大小可知酸性:HCl>H2CO3>HClO,故在相同温度下,同浓度的三种酸溶液的导电能力:HCl>H2CO3>HClO,A正确;ClO-在溶液中会发生水解,所以等体积等物质的量浓度的NaCl溶液与NaClO溶液中Cl-和ClO-离子个数:N(Cl-)>N(ClO-),B正确;向Na2CO3溶液中逐滴滴入少量稀盐酸生成碳酸氢钠和氯化钠,其反应的化学方程式为Na2CO3+HClNaHCO3+NaCl,C错误;若将CO2通入0.1mol·L-1Na2CO3溶液至溶液呈中性,根据电荷守恒c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(HCO3-),则溶液中:c(Na+)=2c(CO32-)+c(HCO3-)=0.2mol·L-1,D正确。
4.(2018北京)测定0.1 mol·L-1 Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻
①
②
③
④
温度/℃
25
30
40
25
pH
9.66
9.52
9.37
9.25
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。
下列说法不正确的是( )。
A.Na2SO3溶液中存在水解平衡:SO32-+H2OHSO3-+OH-
B.④的pH与①不同,是由于SO32-浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D.①与④的KW值相等
答案:C
解析:由①④时刻溶液加入盐酸酸化的氯化钡溶液,④产生白色沉淀较多,说明升温过程中亚硫酸钠被空气中的氧气氧化为硫酸钠,导致亚硫酸根浓度减小。A项,亚硫酸钠为强碱弱酸盐,在溶液中水解使溶液显碱性,A正确;B项,④与①的pH不同是因为亚硫酸钠被空气中的氧气氧化为硫酸钠,导致亚硫酸根浓度减小,溶液pH减小,正确;C项,升高温度,水解平衡右移,减小亚硫酸根浓度,平衡左移,错误;D项,①与④的温度相同,则水的离子积常数KW相同,正确。
5.常温下,下列溶液中的微粒浓度关系正确的是( )。
A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
C.pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+)
D.0.4 mol·L-1 CH3COOH溶液与0.2 mol·L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH)
9
答案:D
解析:新制氯水中加入固体NaOH,根据电荷守恒c(H+)+c(Na+)=c(Cl-)+c(ClO-)+c(OH-),A错误;碳酸氢钠溶液中碳酸氢根离子水解程度大于电离程度,c(H2CO3)>c(CO32-),B错误;C项,NH3·H2O是弱电解质,pH=11的氨水物质的量浓度比pH=3的盐酸的物质的量浓度大得多,氨水与盐酸反应后,氨水剩余,溶液呈碱性,离子浓度大小为c(NH4+)>c(Cl-)>c(OH-)>c(H+),C错误;0.4mol·L-1的CH3COOH溶液与0.2mol·L-1的NaOH溶液等体积混合后得到0.1mol·L-1的CH3COOH溶液和0.1mol·L-1的CH3COONa溶液,溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-);依据物料守恒:2c(Na+)=c(CH3COO-)+c(CH3COOH);两式合并得到:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH),D正确。
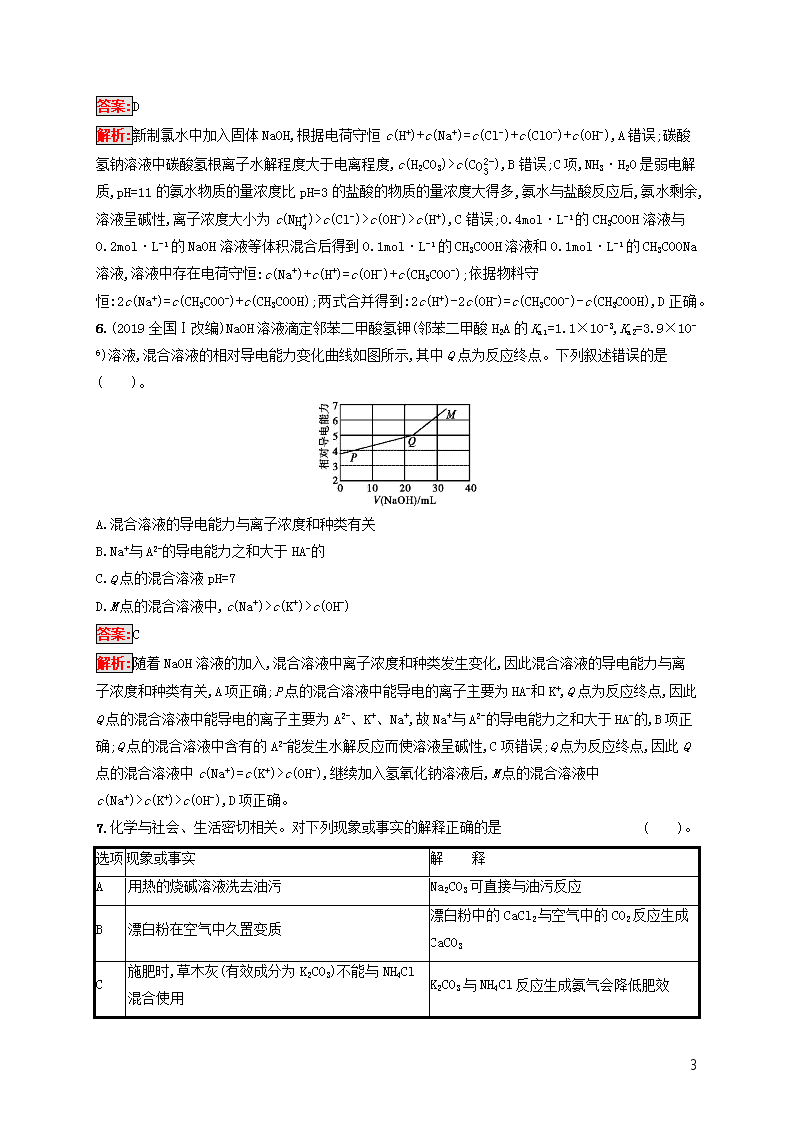
6.(2019全国Ⅰ改编)NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×10-3,Ka2=3.9×10-6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中Q点为反应终点。下列叙述错误的是( )。
A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2-的导电能力之和大于HA-的
C.Q点的混合溶液pH=7
D.M点的混合溶液中,c(Na+)>c(K+)>c(OH-)
答案:C
解析:随着NaOH溶液的加入,混合溶液中离子浓度和种类发生变化,因此混合溶液的导电能力与离子浓度和种类有关,A项正确;P点的混合溶液中能导电的离子主要为HA-和K+,Q点为反应终点,因此Q点的混合溶液中能导电的离子主要为A2-、K+、Na+,故Na+与A2-的导电能力之和大于HA-的,B项正确;Q点的混合溶液中含有的A2-能发生水解反应而使溶液呈碱性,C项错误;Q点为反应终点,因此Q点的混合溶液中c(Na+)=c(K+)>c(OH-),继续加入氢氧化钠溶液后,M点的混合溶液中c(Na+)>c(K+)>c(OH-),D项正确。
7.化学与社会、生活密切相关。对下列现象或事实的解释正确的是( )。
选项
现象或事实
解 释
A
用热的烧碱溶液洗去油污
Na2CO3可直接与油污反应
B
漂白粉在空气中久置变质
漂白粉中的CaCl2与空气中的CO2反应生成CaCO3
C
施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用
K2CO3与NH4Cl反应生成氨气会降低肥效
9
D
FeCl3溶液可用于铜质印刷线路板制作
FeCl3能从含Cu2+的溶液中置换出铜
答案:C
解析:A选项,烧碱是NaOH,错误;B选项,漂白粉变质是因为Ca(ClO)2与空气中的CO2反应,生成CaCO3、HClO,HClO见光分解,错误;D选项,原因是Fe3+与Cu反应生成Fe2+与Cu2+,错误。
8.(2019河南中原名校高三上学期第五次联考)25 ℃时,有下列几种浓度均为0.1 mol·L-1的溶液,下列说法正确的是( )。
A.0.1 mol·L-1NaHSO3溶液的pH=4,则水电离出的c(H+)=10-4 mol·L-1
B.物质的量浓度均为0.1 mol·L-1的Na2CO3和NaHCO3等体积混合,溶液中2c(OH-)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32-)
C.pH=a的NaClO溶液中加入Na2CO3溶液后,溶液pHc(NH4+)>c(SO32-)
C.物质的量浓度相等的①(NH4)2SO4溶液、②NH4HCO3溶液、③NH4Cl溶液、④(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小关系:④>①>②>③
D.0.10 mol·L-1 CH3COONa溶液中通入HCl至溶液pH=7:c(Na+)>c(CH3COOH)=c(Cl-)
答案:D
解析:没有给出Na2CO3和NaHCO3的量的关系,若二者的物质的量浓度相等,则离子浓度之间的关系正确,A项错误;根据电荷守恒有c(NH4+)+c(Na+)+c(H+)=c(OH-)+c(HSO3-)+2c(SO32-),溶液pH=7即c(H+)=c(OH-),所以c(NH4+)+c(Na+)=c(HSO3-)+2c(SO32-),根据物料守恒有c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3),进而有c(NH4+)+c(H2SO3)=c(SO32-),故有c(Na+)>c(SO32-)>c(NH4+),B项错误;Fe2+的水解抑制NH4+的水解,HCO3-的水解促进NH4+的水解,则c(NH4+)的大小关系为④>①>③>②,C项错误;根据电荷守恒有c(Na+)+c(H+)=c(OH-)+c(CH3COO-)+c(Cl-),溶液pH=7即c(H+)=c(OH-),即
9
c(Na+)=c(CH3COO-)+c(Cl-),根据物料守恒有c(Na+)=c(CH3COO-)+c(CH3COOH),因此c(CH3COOH)=c(Cl-),综合分析得c(Na+)>c(CH3COOH)=c(Cl-),D项正确。
10.25 ℃时,满足c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1的醋酸和醋酸钠混合溶液中,c(CH3COO-)与pH的关系如图所示。下列叙述错误的是( )。
A.该温度下醋酸的电离常数Ka为10-4.75 mol·L-1
B.M点所表示的溶液中:c(Na+)+c(H+)+c(CH3COOH)=0.1 mol·L-1
C.N点所表示的溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
D.Q点所表示的溶液中加入等体积的0.05 mol·L-1 NaOH溶液充分反应后pH>7
答案:B
解析:醋酸的电离常数等于c(CH3COO-)×c(H+)c(CH3COOH),Q点时醋酸根离子和醋酸的物质的量浓度相等,则Ka=c(H+)=10-4.75mol·L-1,A正确;M点溶液中电荷守恒,则c(Na+)+c(H+)=c(CH3COO-)+c(OH-),两边加上c(CH3COOH),可知c(Na+)+c(H+)+c(CH3COOH)=c(OH-)+0.1mol·L-1,B错误;从Q→Nc(CH3COO-)逐渐增大,溶液呈酸性,电离大于水解,所以离子浓度大小顺序为c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-),C正确;Q点所表示的溶液中加入等体积的0.05mol·L-1NaOH溶液充分反应后得到醋酸钠溶液,为强碱弱酸盐溶液,溶液呈碱性,pH>7,D正确。
二、非选择题(本题共3个小题,共50分)
11.(16分)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(NH4+)>c(OH-)>c(Cl-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只含有一种溶质,则该溶质是 ,上述四种离子浓度的大小顺序为 (填序号)。
(2)若四种离子的关系符合③,则溶质为 ;若四种离子的关系符合④,则溶质为 。
(3)将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数,则下面图像正确的是 (填字母)。
9
(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl) c(NH3·H2O)(填“大于”“小于”或“等于”,下同);混合前酸中c(H+)和碱中c(OH-)的关系为c(H+) c(OH-)。
答案:(1)NH4Cl ①
(2)NH4Cl和NH3·H2O NH4Cl和HCl
(3)B
(4)小于 大于
解析:(1)由已知的四种离子可知,当溶液中只存在一种溶质时,为NH4Cl;NH4Cl为强酸弱碱盐,NH4+水解使溶液呈酸性,离子浓度关系符合①。
(2)四种离子的关系符合③时,溶液呈碱性,说明碱过量,则溶液中存在的溶质为NH4Cl和NH3·H2O;当四种离子的关系符合④时,溶液呈强酸性,溶液中存在NH4Cl和HCl。
(3)加水稀释酸性溶液,使溶液中的c(H+)减小,则pH增大,NH4Cl为强酸弱碱盐,稀释促进其水解,产生H+,盐酸为强酸,在溶液中全部电离,稀释过程中不会产生H+,pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数时,盐酸的pH大于NH4Cl溶液的,B项符合。
(4)体积相等的稀盐酸和氨水混合,若c(HCl)=c(NH3·H2O),则得到NH4Cl溶液,溶液呈酸性,因得到的溶液为中性,则c(NH3·H2O)应略大于c(HCl)。
12.(18分)已知25 ℃时部分弱电解质的电离平衡常数数据如表所示:
化学式
CH3COOH
H2CO3
HClO
电离平衡常数
Ka=1.8×10-5
Ka1=4.3×10-7
Ka2=5.6×10-11
Ka=3.0×10-8
回答下列问题:
(1)物质的量浓度均为0.1 mol·L-1的四种溶液:
A.CH3COONa B.Na2CO3
C.NaClO D.NaHCO3
pH由小到大排列的顺序是 。
9
(2)常温下,0.1 mol·L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 。
A.c(H+) B.c(H+)c(CH3COOH)
C.c(H+)·c(OH-) D.c(OH-)c(H+)
E.c(H+)·c(CH3COO-)c(CH3COOH)
(3)体积均为100 mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数 (填“大于”“小于”或“等于”)CH3COOH的电离平衡常数,理由是 。
(4)25 ℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol·L-1(填精确值)。
(5)标准状况下,将1.12 L CO2通入100 mL 1 mol·L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:
①c(OH-)=2c(H2CO3)+ ;
②c(H+)+c(Na+)= 。
答案:(1)A碳酸的一级电离>次氯酸>碳酸的二级电离,所以物质的量浓度均为0.1mol·L-1的四种溶液的pH由小到大排列的顺序是AK2>K3 BD 调节溶液的pH
(2)C
(3)①HCOO-+H2OHCOOH+OH- 8.4
②c(Na+)>c(HCOO-)>c(Cl-)>c(H+)>c(OH-)
解析:(1)多元弱碱的阳离子水解分步进行,且逐渐减弱,故有K1>K2>K3。
依据平衡移动原理可知,加水稀释或加NaHCO3都可使平衡右移。
由于FeCl3可水解为Fe(OH)3,故将FeCl3溶液转化为高浓度聚合氯化铁时应调节溶液的pH。
9
(2)向Na2SO3溶液中加入H2SO4溶液,硫酸显酸性,不论是否存在平衡,均可使溶液酸性增强,溶液红色褪去;氯水具有强氧化性,能漂白一些有色的有机物;向Na2SO3溶液中加入BaCl2溶液,发生反应使溶液中的SO32-的浓度减小,平衡向逆反应方向移动,使c(OH-)减小,故C可以说明。
(3)①甲酸的电离平衡常数Ka=1.70×10-4,而Ka=c(HCOO-)·c(H+)c(HCOOH),说明HCOOH为弱酸;HCOONa为强碱弱酸盐,HCOO-发生水解反应使溶液显碱性。反应HCOO-+H2OHCOOH+OH-的平衡常数为Kh=c(HCOOH)·c(OH-)c(HCOO-)=KWKa=1×10-141.70×10-4=117×10-9,c(HCOOH)≈c(OH-),则有c(OH-)=Kh·c(HCOO-)=117×10-9×0.1mol·L-1,c(H+)=KWc(OH-)=17×10-9mol·L-1,故HCOONa溶液的pH=-lg(17×10-9)=-12lg17+9≈8.4。
②向20mL0.1mol·L-1HCOONa溶液中滴加10mL0.1mol·L-1的盐酸,二者反应后得到等浓度的HCOONa、HCOOH及NaCl混合液,混合液呈酸性,说明HCOOH的电离程度大于HCOO-的水解程度,则有c(H+)>c(OH-),由于Na+、Cl-不发生水解反应,故溶液中离子浓度的大小顺序为c(Na+)>c(HCOO-)>c(Cl-)>c(H+)>c(OH-)。
9