- 86.00 KB
- 2021-08-24 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第1课时研究物质性质的基本方法
1.某同学将一小块金属钠和一块铁分别放在表面皿中,研究它们在空气中的稳定性,该学生采用的研究方法是(D)
①假说法②实验法③分类法④比较法
A.①② B.①③ C.②③ D.②④
2.下列关于钠的叙述中,不正确的是(B)
A.钠燃烧时发出黄色的火焰
B.钠燃烧时生成氧化钠
C.钠有很强的还原性
D.钠原子的最外层只有一个电子
3.金属钠着火时,采用的灭火物质是(B)
A.煤油 B.沙子
C.水 D.泡沫灭火器
4.金属钠分别与下列溶液反应时,既有白色沉淀析出,又有气体逸出的是(D)
A.BaCl2溶液
B.K2SO4溶液
C.FeCl3溶液
D.饱和Ca(OH)2溶液
5.下列各组物质混合后,不能生成NaOH的是(D)
A.Na和H2O
B.Ca(OH)2溶液与Na2CO3溶液
C.Na2O和H2O
D.Ca(OH)2溶液与NaCl溶液
6.下列对Na2O2的叙述不正确的是(B)
A.Na2O2是淡黄色固体,久置于空气中变成白色
B.Na2O2的稳定性比Na2O差
C.用Na2O2和水反应可以制取氧气
D.Na2O2放入饱和NaOH溶液中有O2放出,恢复常温后有晶体析出
7.下列关于Na2O2的叙述中正确的是(B)
3
A.将过量Na2O2粉末加入紫色石蕊溶液中并振荡,溶液变为蓝色,且有气泡产生
B.将过量Na2O2粉末加入FeCl3溶液中并振荡,溶液中产生红褐色沉淀,且有气泡产生
C.凡是有Na2O2参与的反应,均能产生O2
D.Na2O2粉末在空气中长期放置不变质
8.把4.6 g金属钠投入95.4 g水中,所得溶液的质量分数是(C)
A.4.6% B.8% C.>8% D.<8%
9.观察法是研究物质性质的一种基本方法。一同学将一小块金属钠露置于空气中,观察到下列现象:
银白色①变灰暗②变白色③出现液滴④白色固体
下列说法正确的是(B)
A.银白色变灰暗是因为生成了过氧化钠
B.出现液滴是因为NaOH具有吸湿性
C.过程④只发生了物理变化
D.最后得到的白色固体是NaOH
10.Na2O2的强氧化性、漂白性:
(1)根据Na2O2与CO2的反应,分析Na2O2与SO2如何反应?写出化学方程式:Na2O2+SO2====Na2SO4。
(2)将Na2O2投入品红溶液中,现象是品红退色。
(3)将Na2O2投入无色酚酞溶液中,现象是溶液先变红后退色。
(4)将Na2O2投入紫色石蕊试液中,现象为溶液先变蓝后退色。
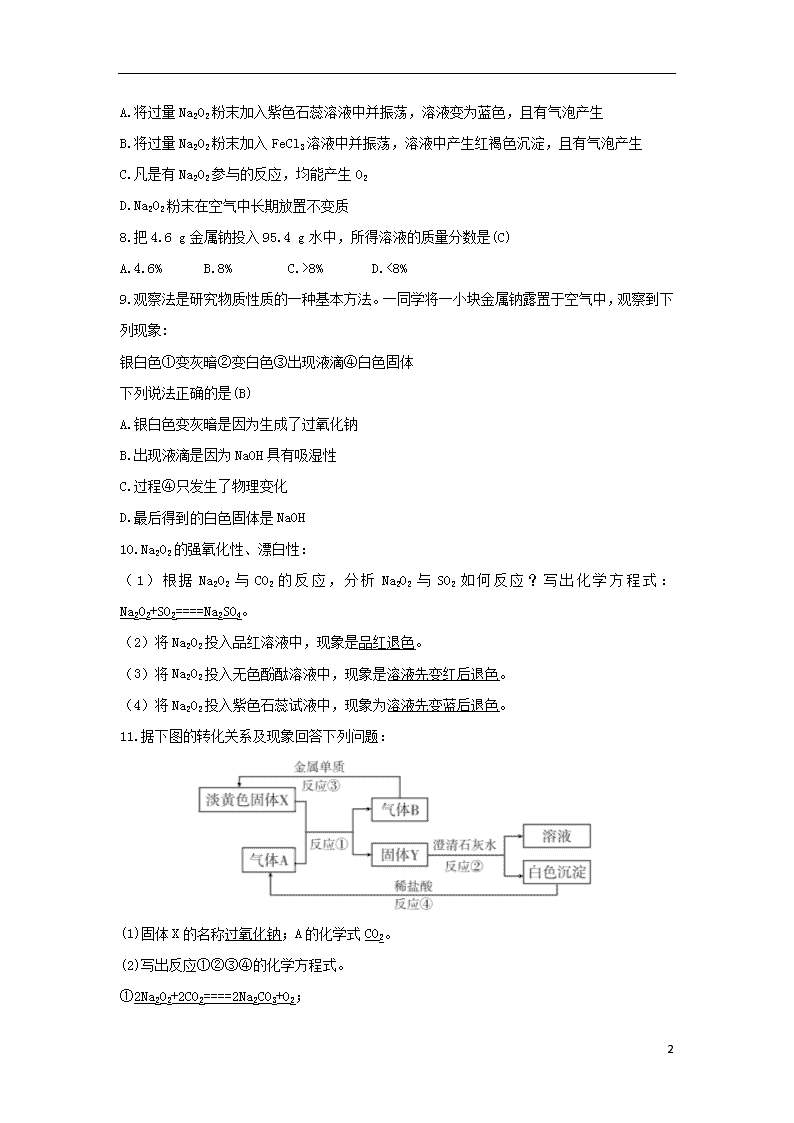
11.据下图的转化关系及现象回答下列问题:
(1)固体X的名称过氧化钠;A的化学式CO2。
(2)写出反应①②③④的化学方程式。
①2Na2O2+2CO2====2Na2CO3+O2;
3
②Na2CO3+Ca(OH)2====CaCO3↓+2NaOH;
③2Na+O2Na2O2;
④CaCO3+2HCl====CaCl2+CO2↑+H2O。
12.“二氧化碳是否在有水存在时才能与过氧化钠反应?”这个问题实验室里可以通过以下实验加以证明:
(1)按图所示的装置(固定试管Ⅰ、Ⅱ的铁架台略去),在干燥的试管Ⅲ中装入Na2O2后,在通入CO2之前,应事先用弹簧夹(K1、K2)夹持好,目的是防止试管Ⅲ和外界相通时过氧化钠发生吸潮现象。
(2)试管Ⅰ内的试剂X是浓H2SO4,打开弹簧夹(K1、K2),加热试管Ⅲ约5 min后,将带火星的木条插入试管Ⅱ的液面上,可以观察到带火星的木条不能复燃,且试管Ⅲ内淡黄色粉末没发生变化,则所得结论是过氧化钠和干燥的二氧化碳不反应。
(3)试管Ⅰ内试剂为NaHCO3饱和水溶液时,其他操作同(2),通过带火星的木条在试管Ⅱ的液面上复燃,同时Ⅲ内固体由淡黄色变为白色的现象可以证明Na2O2与潮湿的CO2能反应且放出O2。
(4)CO2与过氧化钠反应机理也可用示踪原子分析加以证明。请完成下列反应方程式:
Na2O2+C18O2+H218O====2Na2C18O3+O2↑+2H2O。
3
相关文档
- 2020版高中化学 第2章第1节与化学2021-08-2412页
- 2019高中化学 第一章 从实验学化学2021-08-246页
- 高中化学第四章电化学基础4金属的2021-08-243页
- 2019-2020学年高中化学人教版必修22021-08-2414页
- 高中化学选修五(人教版 练习):第三章 2021-08-246页
- 高中化学人教版选修二(学业分层测评2021-08-248页
- 2020版高中化学 第1章 原子结构 第2021-08-2411页
- 高中化学选修三(人教版 课件)-第三章2021-08-2423页
- 高中人教版化学选修1课件:第2章 第2021-08-2417页
- 高中化学必修2全册同步练习及答案(2021-08-2489页