- 845.56 KB
- 2021-11-06 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第
11
课时
金属的冶炼、防护和回收
第
5
章 金属的冶炼与利用
【
考试要求
】
1.
知道一些常见金属
(
铁、铝等
)
矿物。
(A)
2.
知道可用铁矿石炼铁。
(A)
3.
了解防止金属锈蚀的简单方法。
(B)
4.
认识废弃金属对环境的影响和回收金属的重要性。
(B)
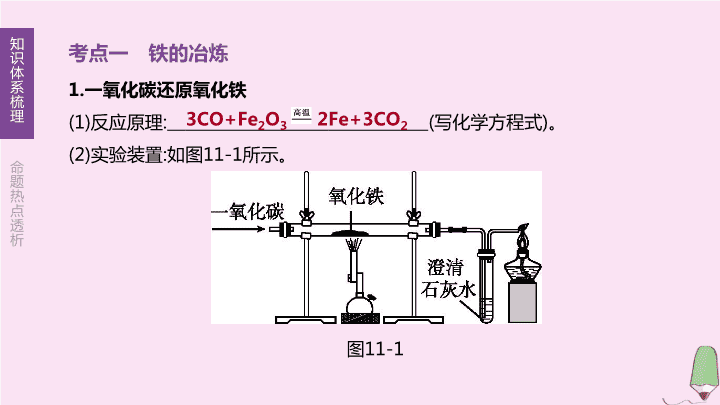
考点一 铁的冶炼
1.
一氧化碳还原氧化铁
(1)
反应原理
:
(
写化学方程式
)
。
(2)
实验装置
:
如图
11-1
所示。
图
11-1
3CO+Fe
2
O
3
2Fe+3CO
2
(3)
实验步骤
:
①
实验开始
:
通气、点灯
,
其目的是
_________________________________________
;
②
实验结束
:
灭灯、停气
,
其目的是防止液体倒吸
,
防止炽热的铁被氧化。
(4)
实验现象
:
红棕色固体变成
色
;
澄清石灰水
。
(5)
尾气处理
:
目的是
。可采用点燃或收集
(
用干瘪的气球收集、排水法收集
)
的方法处理尾气。
(6)
产物检验
:
为了检验生成的物质是否为铁
,
还要进行的操作是
_______________
,
看到
的现象
,
说明有铁生成了。
(7)
应用
:①
检验
CO;②
除去
CO
2
中的
CO
。
排尽玻璃管内空气
,
防止加热一氧化碳与
黑
变浑浊
防止有毒的
CO
排入大气中而污染环境
取样
,
滴加硫
有红色固体析出
,
溶液变为浅绿色
空气的混合物而爆炸
酸铜溶液
2.
高炉炼铁
工业炼铁时
,
把
跟
、
分别加入高炉
,
从下面通入
,
在炉内生成一氧化碳
,
把铁矿石还原成铁。以赤铁矿为例
,
写出高炉内发生反应的化学方程式
:
(1)
。
(2)
。
(3)
。
铁矿石
焦炭
石灰石
热空气
C+O
2
CO
2
CO
2
+C 2CO
3CO+Fe
2
O
3
2Fe+3CO
2
易错判断
(1)
用一氧化碳还原氧化铁
,
反应前后玻璃管中固体减少的质量是生成二氧化碳的质量
(
)
(2)
工业炼铁的产品是生铁
,
实验室模拟炼铁的产品是纯铁
(
)
×
√
考点二 铁的锈蚀与防护
1.
铁生锈条件的探究
实验装置
一周后现象
无现象
无现象
生锈
严重生锈
严重生锈
实验结论
铁与氧气、水同时接触时会生锈
,
酸或
NaCl
溶液能加快铁的锈蚀
注意
装置
②
中使用冷却后的沸水
,
目的是排出水中溶解的氧气
2.
铁生锈的条件
:
与
、
同时接触。
铁生锈的两个条件缺一不可。如果铁表面沾有酸液、氯化钠等物质时
,
往往会加快铁的锈蚀。若铁制品上有铁锈
,
因铁锈
(
主要成分为
Fe
2
O
3
)
疏松多孔
,
里层的铁会继续与氧气、水等反应
,
直至铁完全锈蚀。
3.
铁生锈应用
:
a.
验证氧气含量
;b.
暖宝宝原理
;c.
脱氧剂。
4.
防锈措施
(1)
保持铁制品表面
,
如用过的菜刀洗净擦干。
(2)
在钢铁表面覆盖
,
如刷漆、涂油等。
(3)
改变金属的内部结构
,
如制成不锈钢等合金。
空气
(
或氧气
)
水
洁净干燥
保护层
5.
常见的金属矿物、废旧金属的回收利用
(1)
金属矿物
:①
地球上除极少数很不活泼的金属如金、银等以
形式存在外
,
其余都以
形式存在
(
存在形式取决于金属的活动性
)
。
②
常见的铁矿石
:
赤铁矿
(
主要成分的化学式为
Fe
2
O
3
)
、磁铁矿
(
主要成分的化学式为
Fe
3
O
4
)
。
(2)
废旧金属的回收利用
:
废旧金属不但造成
,
还会产生镉、汞等有毒金属
,
对环境造成污染。保护金属资源的方法
:
回收利用废旧金属、防止金属锈蚀、合理开发金属资源、积极寻找金属代用品等。
单质
化合物
资源浪费
对点演练
1.
某化学兴趣小组用以下装置探究炼铁原理。关于该装置和反应过程的描述错误的是
(
)
A.
盛放药品前应先检查装置气密性
B.
加热前要先通
CO,
加热后
B
中出现浑浊
C.
已知方框中连接的是
C
和
D,
导管口的连接顺序为
a
→
b
→
c
→
d
D.
这种方法“炼”出的铁与工业上
炼出的生铁在组成上最大的区别是不含碳
题组
1
铁的冶炼
图
11-2
[
答案
]C
[
解析
]
由于有气体参加反应
,
则盛放药品前应先检查装置气密性
;
由于
CO
有可燃性
,
与空气混合点燃时易发生爆炸
,
故加热前要先通
CO,
排净管内空气
,CO
还原氧化铁有二氧化碳生成
,CO2
能使石灰水变浑浊
;
由于从
a
端出来的尾气主要是
CO,CO
有毒
,
且难溶于水
,
则需收集在
C
瓶中
,
所以导管口的连接顺序为
a→c→b→d
。
2.
某炼铁厂要冶炼
1 000 t
含杂质
3%
的生铁
,
需要含
Fe
2
O
3
80%
的赤铁矿石的质量是多少吨
?(
计算结果精确至
0.1)
解
:
设需含
Fe
2
O
3
80%
的赤铁矿石的质量为
x
。
3CO+Fe
2
O
3
2Fe+3CO
2
160 112
80%×
x
1 000 t×(1-3%)
x
≈
1 732.1 t
答
:
需要含
Fe
2
O
3
80%
的赤铁矿石的质量是
1732.1 t
。
3.
下列有关铁的锈蚀说法错误的是
(
)
A.
铁锈是一种疏松多孔的物质
,
主要成分是四氧化三铁
B.
铁的锈蚀过程能放热
,
属于缓慢氧化
C.
在干燥的空气中铁钉很难锈蚀
D.
用适量的稀盐酸除去铁钉表面的锈
题组
2
铁的锈蚀与防护
A
4.
为了减缓铁制品的锈蚀
,
下列做法不当的是
(
)
A.
在车船的表面喷涂油漆
B.
将使用后的菜刀用布擦干
C.
洗净铁制品表面的油膜
D.
在铁制品表面镀上一层锌
C
5.
下列有关金属材料的叙述错误的是
(
)
A.
回收利用废旧金属可减少对环境的污染
B.
铝块能制成铝箔是利用了铝的延展性
C.
铝比铁更容易跟氧气和其他物质反应
,
因而铝的抗腐蚀性能比铁差
D.
在铁制品表面刷漆或镀耐腐蚀性金属都可以防止铁制品锈蚀
C
6.
探究铁生锈的条件
,
有利于寻找防止铁制品锈蚀的方法。下列对比实验设计与所探究的条件
(
蒸馏水经煮沸并迅速冷却
),
对应关系正确的是
(
)
A.
甲和乙
:
水
B.
乙和丙
:
空气
C.
甲和丙
:
空气
D.
甲和丁
:
水
图
11-3
[
答案
]D
[
解析
]
铁与氧气和水同时接触会生锈
,
探究铁生锈的条件时应用控制变量法。丁实验中铁钉生锈
,
甲和丁可探究铁钉生锈需要与水接触
,
乙
(
或丙
)
和丁可探究铁钉生锈需要与氧气接触。
7.
将下面五个选择项分别填在横线上
,
每项只能用一次。
A.
缓慢氧化
B.
疏松多孔
C.
与空气、水共同作用
D.
使铁器与空气隔绝
E.
没有水分存在铁不易生锈
①
钢铁锈蚀的条件
;
②
钢铁锈蚀的过程
;
③
铁锈的状态
;
④
使铁器保持干燥
;
⑤
铁器表面喷漆
。
C
A
B
E
D
8.
小林同学用相同的铁钉探究铁生锈与哪些因素有关
,
设计的实验如图
11-4
。经过一周观察到
:
试管
A
和
C
中的铁钉无明显变化
,
试管
B
中的铁钉明显锈蚀。
(1)
铁生锈是铁与
和
同时接触并发生化学反应形成的
,
铁锈的主要成分化学式为
。
(2)A
中的蒸馏水事先要煮沸
,
其目的是
,C
中干燥剂的作用是
。
H
2
O
O
2
图
11-4
Fe
2
O
3
除去溶解在水中的氧气
除去空气中的水蒸气
8.
小林同学用相同的铁钉探究铁生锈与哪些因素有关
,
设计的实验如图
11-4
。经过一周观察到
:
试管
A
和
C
中的铁钉无明显变化
,
试管
B
中的铁钉明显锈蚀。
(3)
要防止铁器生锈通常有多种措施
,
不同的铁制品所采取的防锈措施有所不同。如自行车的链条常采用
的方法防锈
,
自行车的支架常采用
的方法防锈。
(4)
回收废旧金属的意义是
_______________
____________________________
(
答一条
)
。
涂油
喷漆
图
11-4
节约金属资源
(
或减少环境污染、节约能源、
降低生产成本
)
考向一 铁的冶炼
(
6
年
4
考)
1.
[2018
·
徐州树德一模
]
用“
W
”形玻璃管进行微型实验
,
如图
11-5
所示。下列说法不正确的是
(
)
A.a
处红棕色粉末变为黑色
B.a
处的反应为
CO+Fe
2
O
3
2Fe+CO
2
C.b
处澄清石灰水变浑浊证明有
CO
2
生成
D.
可利用点燃的方法进行尾气处理
B
图
11-5
2.
拓展
[2019
·
巴中
]
某化学实验小组利用以下装置测定某赤铁矿中氧化铁的纯度
:
向赤铁矿中通入纯净的一氧化碳气体
,
假设赤铁矿中杂质不参与反应。
请回答下列问题。
(1)
实验开始时
,
先进行的操作是
(
填序号
)
。
①
通入一氧化碳
②
加热
图
11-6
[
答案
]
(1)①
[
解析
]
(1)
一氧化碳具有可燃性
,
混有空气的一氧化碳在有限空间内燃烧可能发生爆炸
,
因此实验开始前
,
先通一氧化碳
,
排尽装置中的空气
,
以免加热时发生爆炸。
2.
拓展
[2019
·
巴中
]
某化学实验小组利用以下装置测定某赤铁矿中氧化铁的纯度
:
向赤铁矿中通入纯净的一氧化碳气体
,
假设赤铁矿中杂质不参与反应。
请回答下列问题。
(2)
实验过程中观察到装置
A
中玻璃管内发生的现象是
。
图
11-6
[
答案
]
(2)
红色粉末变为黑色
[
解析
]
(2)
一氧化碳和氧化铁在高温条件下反应生成铁和二氧化碳
,
氧化铁是红色粉末
,
铁粉是黑色粉末
,
所以
,
实验时观察到的现象是红色粉末变为黑色。
2.
拓展
[2019
·
巴中
]
某化学实验小组利用以下装置测定某赤铁矿中氧化铁的纯度
:
向赤铁矿中通入纯净的一氧化碳气体
,
假设赤铁矿中杂质不参与反应。
请回答下列问题。
(3)
写出
B
装置中发生反应的化学方程式
:
;
装置
C
的作用是
。
图
11-6
[
答案
]
(3)CO
2
+2NaOH Na
2
CO
3
+H
2
O
吸收空气中的二氧化碳
,
防止对实验产生干扰
[
解析
]
(3)
二氧化碳和氢氧化钠溶液反应生成碳酸钠和水
,B
中反应的化学方程式为
CO
2
+2NaOH Na
2
CO
3
+H
2
O;
空气中的二氧化碳如果进入
B
装置中
,
会使实验测得的二氧化碳质量偏大
,
导致计算出样品中氧化铁的质量分数偏大
,
因此
,
增加一个
C
装置
,
可以吸收空气中的二氧化碳
,
防止对实验产生干扰。
2.
拓展
[2019
·
巴中
]
某化学实验小组利用以下装置测定某赤铁矿中氧化铁的纯度
:
向赤铁矿中通入纯净的一氧化碳气体
,
假设赤铁矿中杂质不参与反应。
请回答下列问题。
(4)
从环境保护的角度看此实验存在的缺陷是
。
图
11-6
[
答案
]
(4)
没有尾气处理装置
(5)80%
[
解析
]
(4)
该实验过程中一氧化碳不能全部反应
,
最终的尾气中含有一氧化碳
,
一氧化碳有毒
,
直接排放到空气中会造成空气污染
,
需要对尾气进行处理
,
而该实验没有设置尾气处理装置。
2.
拓展
[2019
·
巴中
]
某化学实验小组利用以下装置测定某赤铁矿中氧化铁的纯度
:
向赤铁矿中通入纯净的一氧化碳气体
,
假设赤铁矿中杂质不参与反应。
请回答下列问题。
(5)
实验前称量赤铁矿的质量为
20 g
。通入足量的一氧化碳完全反应后
,B
装置总质量增加了
13.2 g,
则赤铁
矿中氧化铁的纯度为
。
图
11-6
[
答案
]
(5)80%
[
解析
]
(5)
实验结束后
B
装置增加的质量就是氢氧化钠吸收的二氧化碳质量
,
已知反应生成的二氧化碳质量为
13.2 g,
设样品中氧化铁质量为
x
。
Fe
2
O
3
+3CO 2Fe+3CO
2
160 132
x
13.2 g
x
=16 g
样品中氧化铁的质量分数为
×100%=80%
。
【
技法点拨
】
一氧化碳与氧化铁反应的实验步骤可简记为“气灯灯气”
,
即实验开始时先通气后加热
,
实验结束后先停止加热后停止通气体。
考向二 铁的锈蚀与防护
(
6
年
4
考)
3.
[2016
·
徐州节选
]
铁制品生锈是铁与
共同作用的结果。铁锈成分复杂
,
主要是
(
写化学式
),
工业上常用盐酸除去铁锈。
4.
[2015
·
徐州节选
]
铁器生锈是铁与
共同作用的结果
,
写出防止铁制品生锈的一种方法
:
。
氧气、水
Fe
2
O
3
氧气、水
刷涂油漆
(
合理即可
)
5.
拓展
(1)
为探究铁生锈的条件
,
小组同学设计了如图
11-7
所示的实验。
①
实验
A
中
,
(
填“
a
”“
b
”或“
c
”
)
处最先出现铁锈。
②
铁生锈的条件是
。
③
设计实验
C
的目的是
。
图
11-7
b
铁与水、空气
(
或氧气
)
同时接触
与实验
A
、
B
对照
,
说明铁生锈需要水和氧气
(
合理即可
)
5.
拓展
(2)
该小组又设计如图
11-8
所示装置
,
将一定量铁粉置于锥形瓶底部
,
塞紧瓶塞
,
滴加适量食盐水
,
开始测量容器内压强的变化。压强与时间变化关系如图
11-9
所示。
①
实验中食盐的作用是
。
②
锥形瓶内压强下降的原因是
。
③
生产、生活中铁制品的常见防锈方法有
(
举一例
)
。
图
11-8
加快铁粉的锈蚀速率
铁锈蚀有氧气参与
,
锥形瓶内氧气被消耗
在铁制品表面喷漆
(
合理即可
)
图
11-9
【
技法点拨
】
铁生锈的条件是与氧气、水同时接触
,
缺一不可
;
由于铁锈具有疏松多孔的结构
,
它会让氧气、水渗透进来
,
继续锈蚀铁
,
这也就是“铁生锈、锈吃铁”的原因
;
铁生锈能消耗氧气、发生缓慢氧化
,
同时放出热量
,
因此人们把铁粉用作脱氧剂、发热剂等。