- 208.96 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
2020年贵州省遵义市中考化学试卷
一、选择题(本大题包括10个小题,每小题2分,共20分。每小题只有一个正确答案,请在答题卡选择题栏内用2B铅笔将对应题目答案的标号涂黑。)
1. 乘坐公共交通工具,可携带的物品是( )
A.纸巾 B.鞭炮 C.汽油 D.酒精
2. 下列物质的用途是利用其物理性质的是( )
A.煤用于发电 B.铜丝作导线
C.氮气作保护气 D.小苏打用于发酵
3. 欲将硬水软化,生活中常用的方法是( )
A.加肥皂水 B.静置沉淀 C.加入明矾 D.加热煮沸
4. 分离氯化钾和二氧化锰的混合物,下列操作正确的是( )
A.取样 B.溶解
C.过滤 D.蒸发
5. 1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸腾,烟土溶解。该过程发生的反应有CaO+H2O=Ca(OH)2.下列说法不正确的是( )
A.该反应属于化合反应
B.该反应会放出热量
C.由此反应推测氧化钙可干燥氯化氢气体
D.此反应可制备氢氧化钙
6. 根据图示分析,下列说法正确的是( )
A.镁属于非金属元素 B.镁原子核外有3个电子层
C.镁的相对原子质量为24.31g D.镁原子易得到电子变为Mg2+
7. 醋酸(CH3COOH)是食醋的成分之一,其水溶液中存在H+和CH3COO-.下列说法正确的是( )
A.醋酸属于氧化物 B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气 D.醋酸中碳元素的质量分数最大
8. 下列实验设计及操作中,现象足以说明其结论的是( )
选项
操作
现象
结论
A
向一未知固体中加入稀盐酸
有气泡产生
该固体一定是碳酸盐
B
将一根燃着的木条伸入集气瓶中
木条熄灭
该气体一定是二氧化碳
C
点燃某种塑料
无刺激性气味
该塑料一定是聚氯乙烯
D
向一未知溶液中先加入足量稀盐酸,再滴加氯化钡溶液
刚开始无明显现象,后产生白色沉淀
该溶液中一定存在SO42-
A.A B.B C.C D.D
9. 用一氧化碳还原氧化铁的实验中,Fe2O3转化为铁的具体过程是:Fe2O3→400500Fe3O4→600680FeO→700800Fe
6 / 6
.已知铁的氧化物除Fe2O3外,其余均为黑色。下列说法正确的是( )
A.装置中漏斗的作用是防止倒吸
B.通过实验现象可以判断氧化铁是否完全转化为铁
C.该实验中所有的化学反应里,氧元素的化合价均未改变
D.当硬质玻璃管内固体中铁元素的质量分数为74%时,固体成分是Fe3O4和FeO
10. 某兴趣小组进行了化学探究活动。
实验一:相同条件下,将10.00g下列物质分别置于相同规格的烧杯中,敞口放置在空气中,烧杯中物质质量随时间变化如下表。
时间
水
饱和石灰水
稀盐酸
浓硫酸
氢氧化钠溶液
n小时
8.14g
8.32g
8.62g
11.16g
9.36g
2n小时
5.74g
5.93g
6.67g
12.53g
8.45g
实验二:
下列说法不正确的是( )
A.浓硫酸敞口久置后浓度会变小
B.实验二的溶液①中溶质只有Na2CO3
C.稀盐酸敞口久置后浓度可能会变大
D.饱和石灰水的质量变化小于水的质量变化,原因之一是饱和石灰水吸收了空气中的CO2
二、非选择题(本大题包括7个小题,每空1分,共40分。请在答题卡相应位置按要求作答。)
11. 如图为某品牌奶粉标签的一部分。
(1)写出配料中一种盐的化学式:________。
(2)营养素参考值%是指营养素含量占每日膳食推荐的营养素参考值的百分比。该奶粉中营养素参考值%最高的是________,缺乏该元素可能会导致的疾病是________。
(3)从均衡营养的角度分析,该奶粉中缺乏的营养素且属于有机物的是________。
(4)世界卫生组织建议,成人每天锌元素的最大摄入量为15mg。如果某人每天食用此奶粉50g,摄入的锌元素质量为________mg。
12. 氧气是人类无法离开的物质。
6 / 6
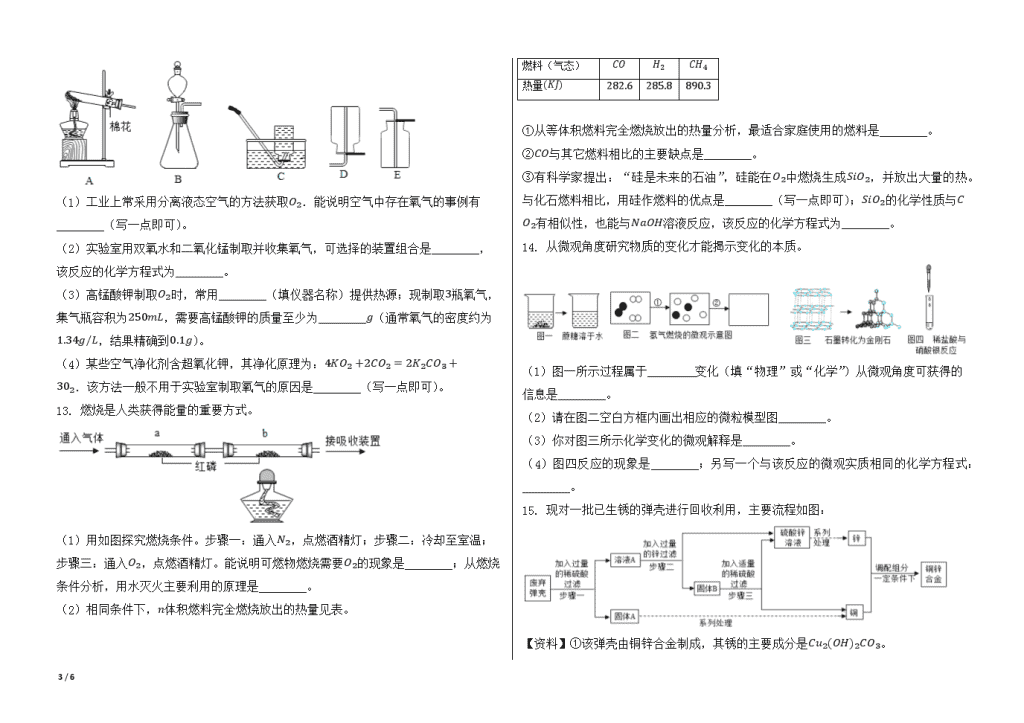
(1)工业上常采用分离液态空气的方法获取O2.能说明空气中存在氧气的事例有________(写一点即可)。
(2)实验室用双氧水和二氧化锰制取并收集氧气,可选择的装置组合是________,该反应的化学方程式为________。
(3)高锰酸钾制取O2时,常用________(填仪器名称)提供热源;现制取3瓶氧气,集气瓶容积为250mL,需要高锰酸钾的质量至少为________g(通常氧气的密度约为1.34g/L,结果精确到0.1g)。
(4)某些空气净化剂含超氧化钾,其净化原理为:4KO2+2CO2=2K2CO3+302.该方法一般不用于实验室制取氧气的原因是________(写一点即可)。
13. 燃烧是人类获得能量的重要方式。
(1)用如图探究燃烧条件。步骤一:通入N2,点燃酒精灯;步骤二:冷却至室温;步骤三:通入O2,点燃酒精灯。能说明可燃物燃烧需要O2的现象是________;从燃烧条件分析,用水灭火主要利用的原理是________。
(2)相同条件下,n体积燃料完全燃烧放出的热量见表。
燃料(气态)
CO
H2
CH4
热量(KJ)
282.6
285.8
890.3
①从等体积燃料完全燃烧放出的热量分析,最适合家庭使用的燃料是________。
②CO与其它燃料相比的主要缺点是________。
③有科学家提出:“硅是未来的石油”,硅能在O2中燃烧生成SiO2,并放出大量的热。与化石燃料相比,用硅作燃料的优点是________(写一点即可);SiO2的化学性质与CO2有相似性,也能与NaOH溶液反应,该反应的化学方程式为________。
14. 从微观角度研究物质的变化才能揭示变化的本质。
(1)图一所示过程属于________变化(填“物理”或“化学”)从微观角度可获得的信息是________。
(2)请在图二空白方框内画出相应的微粒模型图________。
(3)你对图三所示化学变化的微观解释是________。
(4)图四反应的现象是________;另写一个与该反应的微观实质相同的化学方程式:________。
15. 现对一批已生锈的弹壳进行回收利用,主要流程如图:
【资料】①该弹壳由铜锌合金制成,其锈的主要成分是Cu2(OH)2CO3。
6 / 6
②Cu2(OH)2CO3能与稀硫酸反应生成硫酸铜,其他杂质不溶于水,也不参与反应。
(1)为加快步骤一的反应速率,可采用的方法是________(填一种即可);
(2)溶液A中的溶质是________;
(3)步骤三中发生反应的化学方程式为________;
(4)回收锌的质量________废弃弹壳中锌元素的质量(选填“大于”、“小于”或“等于”);
(5)改变铜锌合金中锌的含量可以得到不同机械性能的黄铜。现欲制备120吨(t)含锌量小于35%的黄铜,该类黄铜具有良好的塑性,能承受冷热加工,但在200∘C∼700∘C之间热加工时易断裂。下列符合原料配比及热加工条件的是( )(填字母序号)。
A.锌44t 铜76t 750∘C B.锌38t 铜82t 500∘C
C.锌55t 铜65t 190∘C D.锌25t 铜95t 750∘C
16. 水是一种重要的物质。
(1)用水可以获得氢气。请写出一个由水生成氢气的化学方程式________。
(2)水还可以用于鉴别物质。水鉴别氯化钠和硝酸铵依据的是________。
(3)水是最常见的溶剂。
①下列溶液用水作溶剂的是( )(填字母序号);
A.生理盐水 B.碘酒 C.葡萄糖溶液 ②将100g溶质质量分数为98%的浓硫酸稀释为溶质质量分数为10%的稀硫酸,需加水的质量为 880 g; ③如图为某物质在水中的溶解度曲线,欲使a点所示溶液变为b点,可采取的措施是 升高温度加入溶质,升高温度恒温蒸发溶剂 。 ④20∘C时,用精密仪器称量5.85g NaCl和7.90g NH4HCO3,放入盛有50.00g 水的烧杯中,充分搅拌,静置,有晶体析出。请结合下表分析,理论上析出的晶体及晶体的质量分别为 碳酸氢钠、3.6g 。 20∘C时,五种物质在水中的溶解度:
物质
NaCl
NH4HCO3
NH4Cl
NaHCO3
Na2CO3
溶解度/g
36.0
21.0
37.2
9.6
21.5
17. 某兴趣小组发现某块土地玉米长势不好,为探究其原因,开启了项目学习之旅。
【查阅资料】玉米适宜在pH为6.0∼7.0的土壤中生长;植物生长需要多种营养元素,包括碳、氢、氧、氮、磷、钾、钙、镁等大量元素和其他微量元素。
【任务一】检测土壤的酸碱度并制定改良方案
(1)检测该地土壤的酸碱度
可选用的实验用品:精密pH试纸(可精确到0.1)、标准比色卡、pH计、其他自选
实验步骤
测量结果
实验结论
步骤一:将3份不同位置的土样,干燥后分别与自来水按2:5的质量比在不同的烧杯中混合,充分搅拌后静置;
试样一:pH=4.2
试样二:pH=4.4
试样三:pH=4.5
该土壤pH<6.0,不适合玉米生长
步骤二:________。
反思与评价:该实验方法有一处不够严密,请指出并说明原因________。
(2)探究熟石灰对土样酸碱性的改变情况
实验方法:取300g土样和________g蒸馏水混合,向其中加入一定量熟石灰,充分搅拌后静置,用pH计测定清液的pH;
测量结果:清液的pH为12.1;
反思:若要使改良的土壤适合玉米生长,需控制加入熟石灰的量。
6 / 6
(3)熟石灰用量的测定
实验目的:研究使300g土样呈中性所需的熟石灰的质量
实验方法:________。
(4)查阅资料,常用的酸性土壤改良剂有:生石灰、熟石灰、草木灰(主要成分K2CO3)、含钙的贝壳灰(主要成分CaCO3);要使改良后土壤的pH约为7,也可加入稍过量的________(从上述改良剂中选择)。
【任务二】分析土壤肥力
通过观察,该土地上玉米叶色略有发黄,且有倒伏现象;该小组同学建议施加适量含氮元素和钾元素的复合肥,如________。
6 / 6
参考答案与试题解析
2020年贵州省遵义市中考化学试卷
一、选择题(本大题包括10个小题,每小题2分,共20分。每小题只有一个正确答案,请在答题卡选择题栏内用2B铅笔将对应题目答案的标号涂黑。)
1.A
2.B
3.D
4.A
5.C
6.B
7.C
8.D
9.D
10.B
二、非选择题(本大题包括7个小题,每空1分,共40分。请在答题卡相应位置按要求作答。)
11.CaCO3[或FeSO4或Zn(C6H11O7)2]
钙(或Ca),骨质疏松(或佝偻病)
维生素
1.75
12.动物可在空气中呼吸(或食物在空气中腐败)
BC(或BE),2H2O2MnO22H2O+O2↑
酒精灯,9.9
收集到的气体不纯
13.步骤一中,b中的红磷不燃烧;步骤三中,b中的红磷燃烧,降低温度至可燃物的着火点以下
甲烷,CO有毒,硅在地壳中含量较高,SiO2+2NaOH=Na2SiO3+H2O
14.物理,粒子很小、粒子之间存在间隔、粒子在不断运动
原子的排列方式发生了改变
产生白色沉淀,NaCl+AgNO3=AgCl↓+NaNO3
15.加热
硫酸、硫酸锌、硫酸铜
Zn+H2SO4=ZnSO4+H2↑
大于
D
16.2H2O2H2↑+O2↑
氯化钠溶于水温度无明显变化,硝酸铵溶于水吸热,导致温度降低
AC②将100g溶质质量分数为98%的浓硫酸稀释为溶质质量分数为10%的稀硫酸,需加水的质量为:100g×98%÷10%﹣100g=880g,
17.把pH计分别伸入三份试样中,读出pH,不严密之处:土样与自来水混合;原因:自来水中含有多种物质,可能影响试样的pH
750
取300g土样和750g蒸馏水混合,称量一定质量的氢氧化钙,分多次加入试样中,搅拌,不断利用pH计测定试样pH,当pH约为7时,称量剩余固体质量,可以计算使用的氢氧化钙质量
含钙的贝壳灰,硝酸钾
6 / 6
相关文档
- 2011年全国各地市中考化学模拟试题2021-11-107页
- 初中化学九年级上册第二单元我们周2021-11-1020页
- 2012中考化学复习精品 分子和原子2021-11-105页
- 初中化学九年级上册第一单元走进化2021-11-1022页
- 中考化学一轮专题复习:如何正确书写2021-11-103页
- 中考化学全程复习第五单元化学方程2021-11-1030页
- 初中化学九年级上册第四单元自然界2021-11-104页
- 中考化学复习实验专题突破——化学2021-11-1014页
- 2020年山东省德州市中考化学试卷【2021-11-106页
- 2019年广西梧州市中考化学试题(Word2021-11-1019页