- 298.69 KB
- 2021-11-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
人教版九年级化学上册第三单元测试题
(时间:70分钟 满分:100分 姓名:______)
一、单项选择题(本大题包括10小题,每小题2分,共20分。每小题有四个选项,其中只有一个选项符合题意)
1.保持水的化学性质的最小粒子是 ( A )
A.水分子 B.氢原子
C.氧原子 D.氢原子和氧原子
2.下列有关元素、原子、分子和离子的说法正确的是
( A )
A.决定元素化学性质的是原子的最外层电子数
B.原子可以构成分子,不能直接构成物质
C.分子是化学变化中的最小微粒
D.离子只有得到电子才能变成原子
3.咏梅诗句“二十里中香不断,青羊宫到浣花溪”。诗人闻到香味的原因是 ( B )
A.分子很轻 B.分子不断运动
C.分子体积小 D.分子间有间隙
4.下列各组物质中,都由分子构成的一组是
14
( B )
A.铁、汞 B.氨、干冰
C.水、金刚石 D.硫酸铜、氯化钠
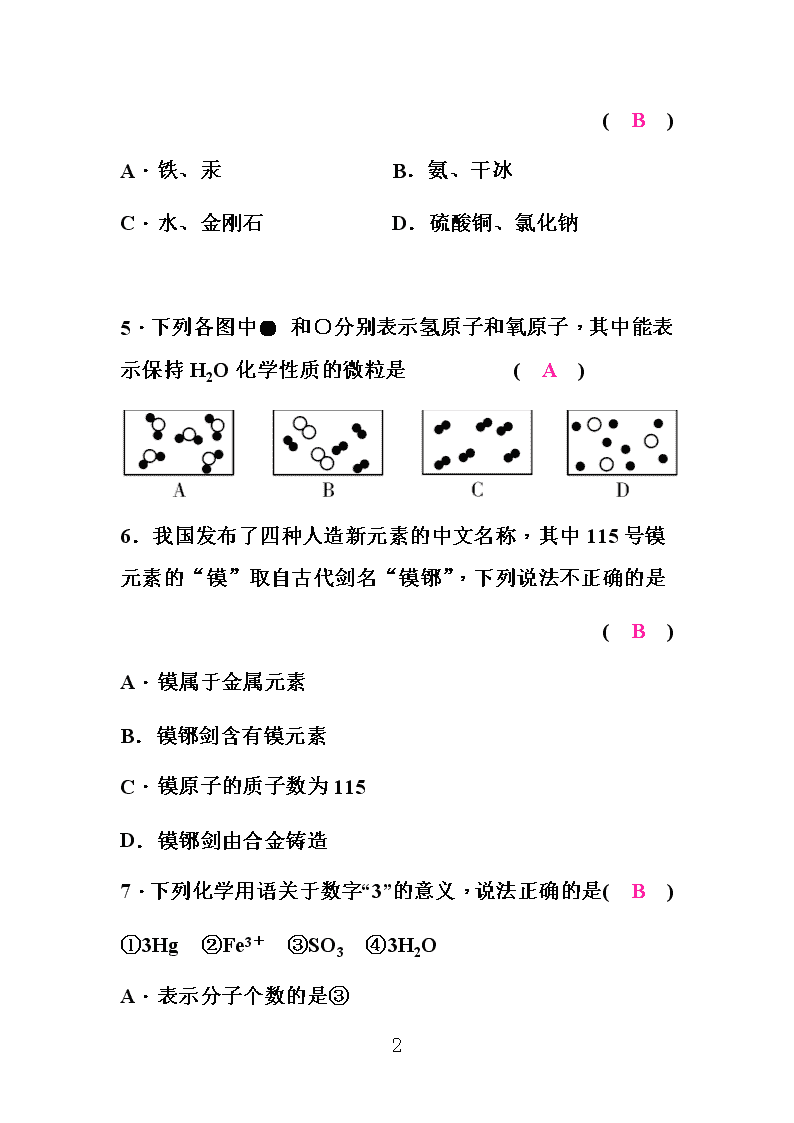
5.下列各图中和○分别表示氢原子和氧原子,其中能表示保持H2O化学性质的微粒是 ( A )
6.我国发布了四种人造新元素的中文名称,其中115号镆元素的“镆”取自古代剑名“镆铘”,下列说法不正确的是
( B )
A.镆属于金属元素
B.镆铘剑含有镆元素
C.镆原子的质子数为115
D.镆铘剑由合金铸造
7.下列化学用语关于数字“3”的意义,说法正确的是( B )
①3Hg ②Fe3+ ③SO3 ④3H2O
A.表示分子个数的是③
14
B.表示离子所带电荷数的是②
C.表示原子个数的是④
D.表示一个分子中含有某种原子个数的是①
8.以下事实用微观粒子的知识解释错误的是( B )
选项
事实
解释
A
一畦春韭绿,十里稻花香
分子不断运动
B
水结冰后体积变大
水分子体积变大
C
1滴水中大约有1.67×1021个水分子
分子很小
D
6 000 L氧气加压后可装入容积为40 L的钢瓶中
分子间有间隔
9.北京大学生命科学学院蒋争凡教授研究组发现,
14
锰离子是细胞内天然免疫激活剂和警报素。在元素周期表中锰元素的某些信息如图所示,下列有关锰的说法不正确的是( D )
A.原子序数为25
B.元素符号为Mn
C.原子核内质子数为25
D.中子数为54.95
10.(2019·广州)某微粒M的结构示意图如下,关于该微粒的说法正确的是 ( D )
A.M的原子易失电子
B.x只能为7
C.M为金属元素
D.x为8时,M为阴离子
二、选择填充题(本大题包括5小题,每小题3分,共15分。先在A、B、C中选择一个正确选项,然后在D处补充一个符合题意的答案,每小题的选择2分,填充1分)
11.逻辑推理是学习化学常用的思维方法,下列推理正确的是 ( A )
A.物质的分子结构不同则性质不同,所以氧气和臭氧(O3)的性质不同
14
B.由同种分子构成的物质一定是纯净物,所以纯净物一定是由同种分子构成
C.氧、硫、氯原子最外层电子数均多于四个,故非金属元素原子最外层电子数都多于四个
D.元素是具有相同质子数的同类原子,所以氢元素和氧元素的本质区别是__质子数不同__
12.从微观角度解释生活中的变化现象,下列说法正确的是
( A )
A.食物腐败:分子发生了变化
B.光合作用:分子分成原子,有新的原子生成
C.木炭燃烧:分子在不断运动
D.液氧转化为氧气:__分子间间隔变大__
13.如图所示,根据原子结构示意图可以确定的是( A )
A.质子数 B.相对原子质量
C.中子数 D.__原子序数__
14.如图是锑元素在元素周期表中的部分信息,下列有关说法正确的是 ( B )
14
A.锑元素属于非金属元素
B.锑元素的相对原子质量是121.8
C.锑元素的中子数为51
D.__锑原子核内有51个质子(合理均可)__
15.某阴离子的结构示意图为,则x的值可能是( A )
A.9 B.10 C.12 D.__8(或7等)__
三、填空与说明题(本大题包括8小题,共53分)
16.(5分)
(1)用适当的数字和化学符号填空:
①两个氧原子__2O__;
②三个氩原子__3Ar__;
③两个镁离子__2Mg2+__。
(2)写出符号中“2”的含义:
①2S__两个硫原子__;
②Ca2+__一个钙离子带两个单位正电荷__。
17.(3分)(2019·杭州)据报道,“火星快车”号探测器在火星大气层中发现了一种二氧化碳分子,它的化学式可表示为:C16O18O
14
(元素符号左上角的数字代表该原子中质子数和中子数之和)。回答:
(1)18O中的质子数是__8__,中子数是__10__。
(2)相同分子数的C16O2和C16O18O,分别与足量CaO化合全部转化为CaCO3,生成CaCO3的质量前者__小于__(选填“大于”“小于”或“等于”)后者。
18.(10分)下列为A、B、C、D四种原子的结构示意图,请回答下列问题:
(1)四种原子在化学变化中容易失去电子的是__C__(填序号,下同),容易得到电子的是__AD__。
(2)具有稳定结构的是__B__。
(3)化学性质相似的是__AD__。
(4)属于金属原子的是__C__,属于非金属原子的是__ABD__,属于稀有气体原子的是__B__。
19.(12分)元素周期表是学习和研究化学的重要工具。回答下列问题:
(1)元素周期表中不同种元素间最本质的区别是__A__(填字母)。
14
A.质子数不同 B.中子数不同 C.相对原子质量不同
(2)1869年,__B__(填字母)发现了元素周期律并编制出元素周期表。
A.张青莲 B.门捷列夫 C.拉瓦锡
(3)氟原子结构示意图为____,氟原子在化学反应中易__得到__(选填“得到”或“失去”)电子形成氟离子,氟离子有__2__个电子层;
(4)元素周期表中氟元素的有关信息(如图),又知钠能在氟气中燃烧生成氟化钠,试回答:
①钠是由__钠原子__构成;
②氟气与氯气构成相似。则氟气是由__氟元素__组成;
③上述反应的基本类型是__化合反应__,生成的氟化钠属__纯净物__(填物质类别)。从微观角度讲不变的粒子是__钠原子和氟原子__;反应前后发生变化的粒子是__氟分子__;
④现以一种氧原子质量的1/16为标准,其他原子的质量跟它相比所得的比值作为这种原子的相对原子质量。一个氧原子的质量为2.657×10-26 kg,一个铁原子的质量是9.288×10-26 kg,则铁原子的相对原子质量为__56__。
14
20.(6分)(2019·铁岭)如图中A是锡元素在元素周期表中的信息,B~E是四种粒子的结构示意图。请回答:
(1)锡元素属于__金属__(选填“金属”或“非金属”)元素。
(2)锡元素的相对原子质量是__118.7__,E粒子的符号是__S2-__。
(3)D粒子在化学反应中容易__失去__(选填“得到”或“失去”)电子。
(4)B、C、D、E四种粒子中属于同种元素的是__C__D__(填字母,下同),具有相对稳定结构的是__B__C__E__。
21.(4分)在下面(1)~(4)事实后的空格内,选择填写有关分子基本特征的序号。
A.分子很小 B.分子间有间隔 C.分子在不停运动
D.同种分子性质相同,不同种分子性质不同
(1)将50 mL酒精和50 mL水混合后,混合液体积小于100 mL。__B__
(2)湿衣服经晾晒一段时间后,会变干。__C__
14
(3)一滴水里的水分子个数由10亿人数,每人每分钟数100个,日夜不停,需用3万年才能数完。__A__
(4)如图所示,用长颈漏斗小心地将硫酸铜溶液(蓝色)注入水的下面,可以看到明显的界面。静置几天后,界面逐渐模糊不清了。__C__
22.(5分)在宏观、微观和符号之间建立联系是化学学科的特点。
(1)物质的组成及构成关系如图1所示,图中①表示的是__原子__,②表示的是__分子__。
(2)下列说法正确的是__A__(填字母)。
14
A.氯化氢是由氢、氯两种元素组成的
B.氯化氢是由氢气和氯气混合而成的
C.氯化氢是由一个氢原子和一个氯原子构成的
(3)图2是氧、硫、氯三种元素的原子结构示意图。
①氯原子的结构示意图中x的数值是__7__。
②氧和硫两种元素的化学性质具有相似性的原因是它们原子的__最外层电子数__相同。
23.(8分)(2019·大庆)元素周期表是学习和研究化学的重要工具。如图是元素周期表部分内容,请根据表中信息完成相关问题。
14
(1)铍原子的相对原子质量是__9.012__,它属于__金属__(选填“金属”或“非金属”)元素。
(2)第三周期中含有的非金属元素共有__5__种。
(3)元素周期表的纵行叫做族,分为主族、副族、Ⅷ族和0族。主族用字母“A”来表示,共有七个主族,依次用ⅠA族、ⅡA族、ⅢA族、ⅣA族、ⅤA族、ⅥA族、ⅦA族表示。同一主族元素化学性质相似。
①甲同学研究了同主族元素原子结构的共同点,提出将氦元素放在第ⅡA族,甲同学的依据是__最外层电子数为2__;乙同学进行了反驳,认为氦元素属于0族元素的一种,乙同学的依据是__第一层为最外层且2个电子已是稳定结构__。
②硒元素是人体必需的微量元素之一,有防癌、抗癌的作用。硒原子结构示意图如图,
14
请你分析硒元素在元素周期表中的位置是第4周期、第__ⅥA__族。
(4)核电荷数1~18的非金属元素A和B,可形成原子个数比1∶1和2∶1的两种常温下呈液态的化合物,写出这两种化合物的化学式__H2O2和H2O__。
四、实验与探究题(本大题包括1小题,共12分)
24.某同学设计如下实验探究“分子的性质”:
图Ⅰ是按课本进行的一个化学实验,大烧杯中的实验现象是__甲烧杯中酚酞溶液变红__,此实验说明__分子是在不断运动的__。但是在实验时同学们闻到了一股难闻的刺激性气味,于是小明对原实验装置进行了改进,装置如图Ⅱ,并进行如下操作:
a.向B、C、E三支试管中分别加入5 mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色。
b.在A、D试管中分别加入2 mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
14
【分析讨论】 E试管放有酚酞溶液的目的是:__与B、C中的酚酞溶液作对比__。由此可以得到的实验结论是①__酚酞遇浓氨水变红__,②__分子在不断运动,且温度越高,分子运动越剧烈__。③对比改进前的实验,改进后实验的优点是:__能够防止氨气扩散到空气中,污染大气;能够得出在不同温度下,分子运动剧烈程度的差异__。
14
相关文档
- 江苏省盐城市2020年初中毕业与升学2021-11-1011页
- 066—2019年湖北省孝感市中考语文2021-11-1010页
- 山西省2012年中考理综试题化学部分2021-11-106页
- 15届 荆门市文科综合 地理中考试2021-11-104页
- 吉林省2020年中考语文试题及答案2021-11-1023页
- 中考复习化学专题检测试题:第2讲构2021-11-106页
- 鲁教版九年级化学第10、11单元测试2021-11-107页
- 2019广东省中考数学试题(word版,含手2021-11-109页
- 鲁教版九年级化学上册期末测试题含2021-11-107页
- 教科版九年级物理同步测试题课件(7)2021-11-1020页