- 143.50 KB
- 2021-11-11 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
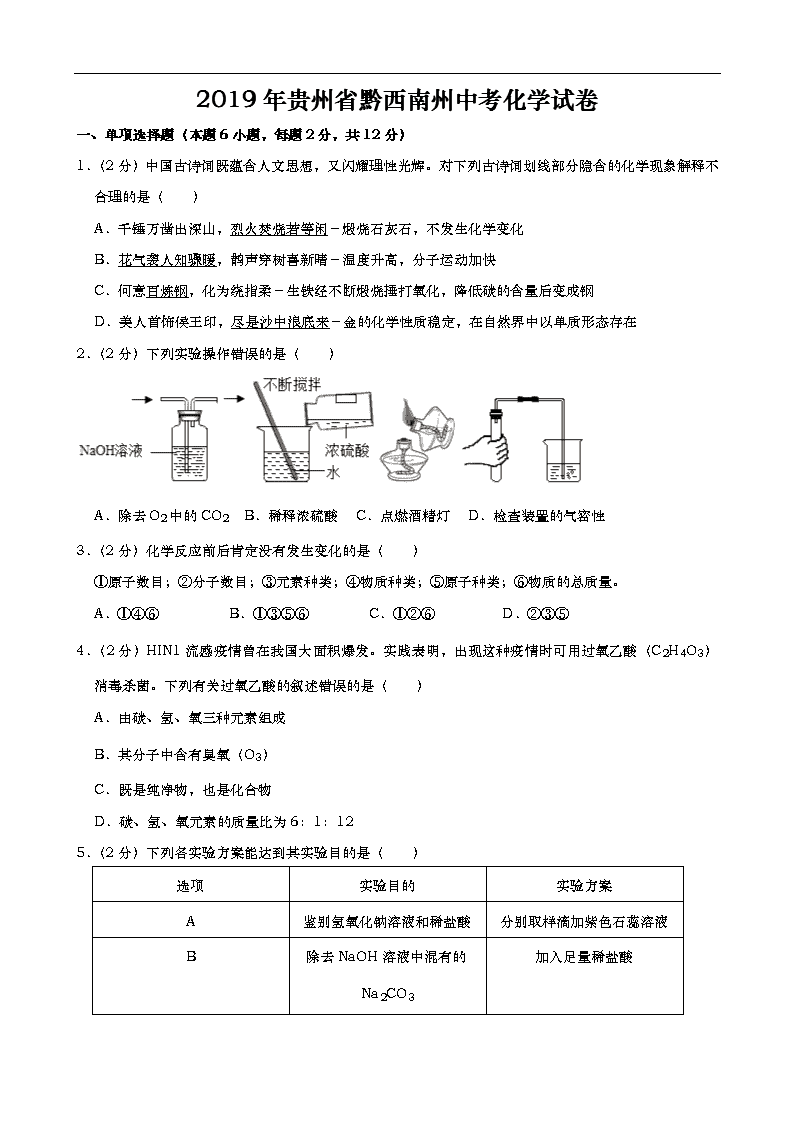
2019年贵州省黔西南州中考化学试卷
一、单项选择题(本题6小题,每题2分,共12分)
1.(2分)中国古诗词既蕴含人文思想,又闪耀理性光辉。对下列古诗词划线部分隐含的化学现象解释不合理的是( )
A.千锤万凿出深山,烈火焚烧若等闲﹣煅烧石灰石,不发生化学变化
B.花气袭人知骤暖,鹊声穿树喜新晴﹣温度升高,分子运动加快
C.何意百炼钢,化为绕指柔﹣生铁经不断煅烧捶打氧化,降低碳的含量后变成钢
D.美人首饰侯王印,尽是沙中浪底来﹣金的化学性质稳定,在自然界中以单质形态存在
2.(2分)下列实验操作错误的是( )
A.除去O2中的CO2 B.稀释浓硫酸 C.点燃酒精灯 D.检查装置的气密性
3.(2分)化学反应前后肯定没有发生变化的是( )
①原子数目;②分子数目;③元素种类;④物质种类;⑤原子种类;⑥物质的总质量。
A.①④⑥ B.①③⑤⑥ C.①②⑥ D.②③⑤
4.(2分)HIN1流感疫情曾在我国大面积爆发。实践表明,出现这种疫情时可用过氧乙酸(C2H4O3)消毒杀菌。下列有关过氧乙酸的叙述错误的是( )
A.由碳、氢、氧三种元素组成
B.其分子中含有臭氧(O3)
C.既是纯净物,也是化合物
D.碳、氢、氧元素的质量比为6:1:12
5.(2分)下列各实验方案能达到其实验目的是( )
选项
实验目的
实验方案
A
鉴别氢氧化钠溶液和稀盐酸
分别取样滴加紫色石蕊溶液
B
除去NaOH溶液中混有的Na2CO3
加入足量稀盐酸
C
除去CO2中混有少量的CO
在足够的氧气中点燃
D
鉴别氮气和二氧化碳
将燃着的木条分别伸入气体中
A.A B.B C.C D.D
6.(2分)下列各组离子在溶液中能大量共存的是( )
A.Na+、H+、Cl﹣、OH﹣ B.Ag+、K+、Cl﹣、NO3﹣
C.Na+、H+、NO3﹣、CO32﹣ D.H+、Mg2+、SO42﹣、Cl﹣
二、填空题(本题5小题,每空1分,共24分)
7.(5分)用化学用语填空:
(1)3个二氧化硫分子: 。
(2)保持氩气化学性质的最小粒子 。
(3)空气中含量最多的气体: 。
(4)氧化铁中铁元素的化合价: 。
(5)13号元素原子的结构示意图: 。
8.(6分)化学与人类生活、生产活动息息相关。根据所学化学知识回答下列问题:
(1)生活中常用 来区分硬水和软水。
(2)人的胃液里含有适量的 (填名称),可以帮助消化。
(3)食用“加铁酱油”可预防贫血,其中的“铁”是指 (填“元素”或“原子”)。
(4)厨房油锅着火,盖上锅盖可以立即灭火,其原理是 。
(5)将少量某塑料样品在密闭容器中与足量的O2反应,生成了CO2和H2O,由此可知该塑料中一定含有 元素。
(6)稀土有“工业的维生素”的美誉。稀土元素Tm在元素周期表中的信息如图,下列有关Tm的判断错误的是 (填序号)。
①原子的质子数为69
②属于金属元素
③原子的中子数为69
④相对原子质量为168.9
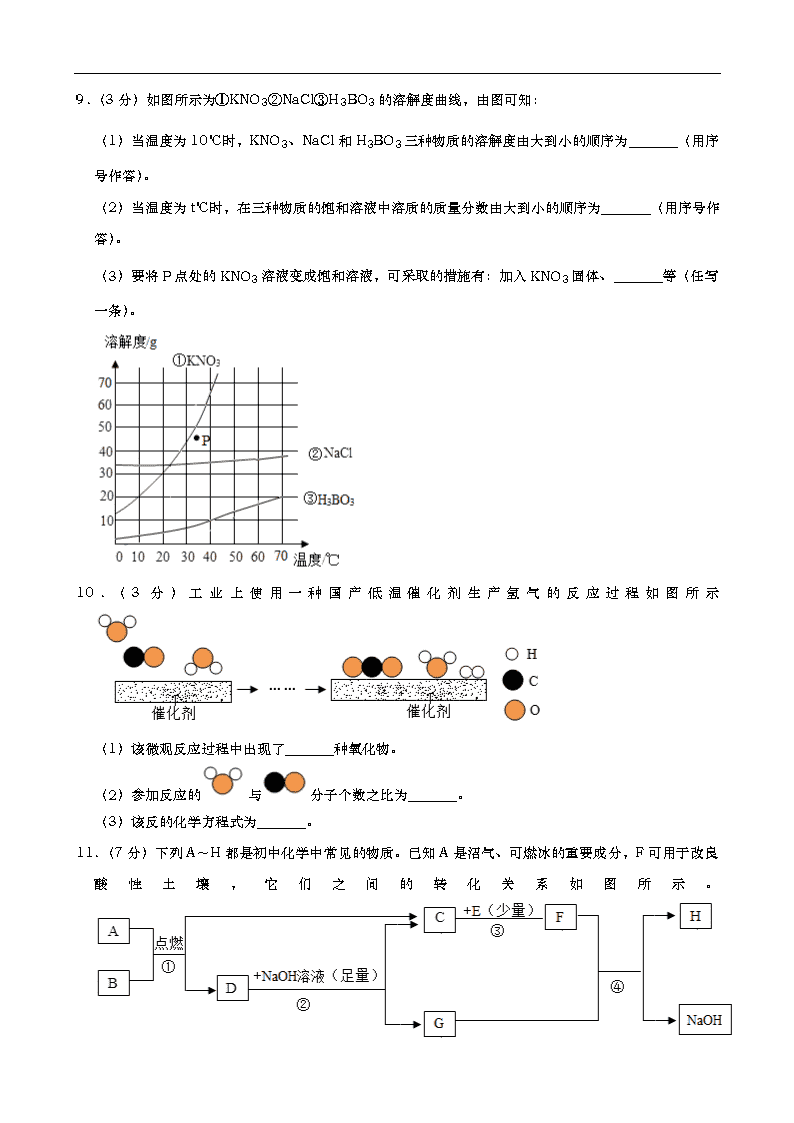
9.(3分)如图所示为①KNO3②NaCl③H3BO3的溶解度曲线,由图可知:
(1)当温度为10℃时,KNO3、NaCl和H3BO3三种物质的溶解度由大到小的顺序为 (用序号作答)。
(2)当温度为t℃时,在三种物质的饱和溶液中溶质的质量分数由大到小的顺序为 (用序号作答)。
(3)要将P点处的KNO3溶液变成饱和溶液,可采取的措施有:加入KNO3固体、 等(任写一条)。
10.(3分)工业上使用一种国产低温催化剂生产氢气的反应过程如图所示
(1)该微观反应过程中出现了 种氧化物。
(2)参加反应的与分子个数之比为 。
(3)该反的化学方程式为 。
11.(7分)下列A~H都是初中化学中常见的物质。已知A是沼气、可燃冰的重要成分,F可用于改良酸性土壤,它们之间的转化关系如图所示。
回答下列问题:
(1)A的化学式为 ,G俗称 。
(2)大气中D的含量过高会产生 ,从而导致全球气候变暖。
(3)反应③的化学方程式为 ,该反应过程中 (填“吸收”或“放出”)热量。
(4)反应④的化学方程式为 ,其基本反应类型为 反应。
三、实验与探究(本题2小题,每空1分,共16分)
12.(8分)实验室利用如图所示装置进行相关实验。
回答下列问题:
(1)写出装置图中标号仪器的名称:① ,② 。
(2)用高锰酸钾制氧气,应选用的发生装置是 (填字母序号),该反应的化学方程式为 ,其中转化为氧气的氧元素与高锰酸钾中氧元素的质量之比是 。
(3)常温下,用锌和稀硫酸反应制取氢气,若要随时控制反应的发生和停止,应选用的发生装置是 (填字母序号),反应的化学方程式为 ;点燃氢气前必须验纯,为确保安全,最好选用装置 (填字母序号)所示方法收集氢气。
13.(8分)某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。
【查阅资料】
经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。该反应的化学方程式为 。
【对比实验】
编号
操作
现象
甲
将表面未打磨的铝丝浸入CuSO4溶液中
无明显现象
乙
将表面打磨后的铝丝浸入CuSO4溶液中
铝丝表面析出红色固体
丙
铝丝表面析出红色固体
将表面未打磨的铝丝浸入CuCl2溶液中
(1)比较实验乙和实验 (填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
(2)实验乙中反应的化学方程式为 ,据此可知金属活动性A1比Cu (填强”或“弱”)。
(3)小明同学对实验丙的现象进行分析,认为H2O对氧化铝薄膜有破坏作用。但此观点马上被其他同学否定,否定的依据是 。
【猜测与探究】
小组同学针对实验丙的现象,经讨论后猜测:Cl﹣破坏了氧化铝薄膜。
为检验此猜测是否正确,他们首先向两支试管中加入相同的CuSO4溶液,并均浸入表面未打磨的铝丝,然后进行了新的探究:
操作
现象
结论
推论
(1)向一支试管中再加入NaCl固体
铝丝表面析出红色固体
氧化铝薄膜被破坏
Na+或① 能破坏氧化铝薄膜
(2)向另一支试管中再加入Na2SO4固体
②
氧化铝薄膜未被破坏
Na+和SO42﹣都不能破坏氧化铝薄膜
【结论与反思】
得出结论:前述猜测 (填“正确”或“不正确”)
总结反思:本次探究充分运用了比较法和控制变量法
四、计算题(本题共8分)
14.(8分)为测定某氧化铜和铜的固体混合物中氧化铜的质量分数,小勇同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验,测得数据如下:
次序
①
②
③
④
加入稀硫酸的质量/g
25
25
25
25
剩余固体的质量/g
16
a
10
10
回答列问题:
(1)原固体混合物中,氧化铜的质量分数为 。
(2)上表中,a的值为 ,实验③所得溶液中的溶质是 (填化学式)。
(3)计算该实验所用稀硫酸中溶质的质量分数。(写出计算过程,结果精确到0.1%)
2019年贵州省黔西南州中考化学试卷
参考答案与试题解析
一、单项选择题(本题6小题,每题2分,共12分)
1.【解答】解:A、烈火焚烧是石灰石高温分解生成氧化钙和二氧化碳,是化学变化,错误;
B、花气袭人知骤暖说明分子的运动与温度有关,温度高,分子的运动快,正确;
C、炼钢的过程是不断减少生铁中的含碳量的过程,正确;
D、尽是沙中浪底来说明金的化学性质稳定,在自然界中以单质存在,正确;
故选:A。
2.【解答】解:A、二氧化碳能与氢氧化钠溶液反应,氧气不能,图中装置起洗气功能时进气管与出气管的方向是“长进短出”,图中所示装置正确。
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时的扩散;一定不能把水注入浓硫酸中;图中所示操作正确。
C、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所示操作错误。
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确。
故选:C。
3.【解答】解:化学反应前后,原子的数目不变;分子的数目可能不变,也可能改变;元素的种类一定不变;物质的种类一定改变;原子的种类一定不变;物质的总质量一定不变,观察选项,
故选:B。
4.【解答】解:A.由化学式C2H4O3可知,过氧乙酸是由碳、氢、氧三种元素组成的,故正确;
B.分子是由原子构成的,过氧乙酸分子是由碳原子、氢原子和氧原子构成的,其中不含臭氧分子,故错误;
C.由化学式C2H4O3可知,过氧乙酸是由一种物质组成的,属于纯净物,该纯净物是由三种元素组成的,属于化合物,故正确;
D.过氧乙酸中碳、氢、氧三种元素的质量比为:(12×2):(1×4):(16×3)=6:1:12,故正确。
故选:B。
5.【解答】
解:A、氢氧化钠溶液和稀盐酸分别显碱性、酸性、分别能使紫色石蕊溶液变蓝色、红色,可以鉴别,故选项实验方案能达到其实验目的。
B、Na2CO3、NaOH溶液均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项实验方案不能达到其实验目的。
C、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质,故选项实验方案不能达到其实验目的。
D、氮气和二氧化碳均不能燃烧、不能支持燃烧,均能使燃着的木条熄灭,不能鉴别,故选项实验方案不能达到其实验目的。
故选:A。
6.【解答】解:A、H+与OH﹣两种离子能结合成水,不能大量共存,故选项错误。
B、Ag+、Cl﹣、两种离子能结合成氨气和水,不能大量共存,故选项错误。
C、H+、CO32﹣两种离子能结合成水和二氧化碳,故选项错误。
D、四种离子间不能结合成沉淀、气体或水,能大量共存,故选项正确。
故选:D。
二、填空题(本题5小题,每空1分,共24分)
7.【解答】解:(1)3个二氧化硫分子就是在二氧化硫化学式的前面加上数字3,故填:3SO2。
(2)保持氩气化学性质的最小粒子是氩原子,故填:Ar。
(3)空气中含量最多的气体是氮气,故填:N2。
(4)氧化铁中铁元素的化合价为+3,故填:2O3。
(5)13号元素原子的结构示意图为 ,故填:。
8.【解答】解:(1)生活中常用肥皂水来区分硬水和软水;
(2)人的胃液里含有适量的盐酸,可以帮助消化;
(3)物质是由元素组成的,食用“加铁酱油”可预防贫血,其中的“铁”是指元素;
(4)隔绝空气、降低可燃物的温度至着火点以下、移除可燃物都可以灭火。厨房油锅着火,盖上锅盖可以立即灭火,其原理是隔绝空气;
(5)将少量某塑料样品在密闭容器中与足量的O2反应,生成了CO2和H2
O,由此可知该塑料中一定含有碳元素和氢元素;
(6)根据稀土元素Tm在元素周期表中的信息可知:
①原子的质子数为69,故①正确;
②铥字是“金”字旁,属于金属元素,故②正确;
③质子数等核外电子数,根据中子数关系不大,故③错误;
④相对原子质量为168.9,故④正确。
故答案为:
(1)肥皂水;
(2)盐酸;
(3)元素;
(4)隔绝空气;
(5)碳、氢;
(6)③。
9.【解答】解:(1)由溶解度曲线可知,当温度为10℃时,KNO3、NaCl和H3BO3三种物质的溶解度由大到小的顺序为:NaCl>KNO3>H3BO3;故答案为:NaCl>KNO3>H3BO3;
(2)当温度为t℃时,在三种物质的饱和溶液中溶质的质量分数由大到小的顺序为:NaCl=KNO3>H3BO3;故答案为:NaCl=KNO3>H3BO3;
(3)要将P点处的KNO3溶液变成饱和溶液,可采取的措施有:加入KNO3固体、蒸发水分、降低温度等;故答案为:蒸发水分或降低温度;
10.【解答】解:由微观反应示意图可知,该反应是由水和一氧化碳在低温催化剂的作用下反应生成二氧化碳和氢气,化学方程式为:CO+H2OH2+CO2。
(1)氧化物是由两种元素组成,且其中一种元素是氧元素的化合物,所以一氧化碳、水和二氧化碳均属于氧化物;故填:3;
(2)由化学方程式可知,参加反应的水分子与一氧化碳分子的个数比为1:1;故填:1:1;
(3)由微观反应示意图可知,该反应是由水和一氧化碳在低温催化剂的作用下反应生成二氧化碳和氢气,化学方程式为:CO+H2OH2+CO2.故填:CO+H2OH2+CO2。
11.【解答】
解:(1)A~H都是初中化学中常见的物质,A是沼气、可燃冰的重要成分,所以A是甲烷,F可用于改良酸性土壤,所以F是氢氧化钙,甲烷和B点燃生成D和C,D会与氢氧化钠反应,所以D是二氧化碳,B是氧气,甲烷和氧气在点燃的条件下生成二氧化碳和水,所以C是水,水和E反应生成氢氧化钙,所以E是氧化钙,二氧化碳和氢氧化钠反应生成碳酸钠,所以G是碳酸钠,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,所以H是碳酸钙,经过验证,推导正确,所以A的化学式为CH4,G俗称纯碱;
(2)大气中D的含量过高会产生温室效应,从而导致全球气候变暖;
(3)反应③是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2,该反应过程中放出热量;
(4)反应④是碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,其基本反应类型为复分解反应。
故答案为:(1)CH4,纯碱;
(2)温室效应;
(3)CaO+H2O=Ca(OH)2,放出;
(4)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,复分解。
三、实验与探究(本题2小题,每空1分,共16分)
12.【解答】解:(1)①长颈漏斗;②水槽;
(2)高锰酸钾制取氧气需要加热,A装置适用;高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4K2MnO4+MnO2+O2↑;根据化学方程式可知每8个氧原子,转化成一个氧分子,所以转化为氧气的氧元素与高锰酸钾中氧元素的质量之比==25%;
(3)锌和稀硫酸反应制取氢气,属于固液常温型,并且要随时控制反应的发生和停止,适合用C装置作发生装置;化学方程式为:Zn+H2SO4=ZnSO4+H2↑;氢气具有可燃性,当混有一定量的空气时点燃会发生爆炸,因此收集到的气体纯度一定要高,可选用D装置收集。
故答案为:
(1)长颈漏斗;水槽;
(2)A;2KMnO4K2MnO4+MnO2+O2↑;25%;
(3)C;Zn+H2SO4=ZnSO4+H2↑;D。
13.【解答】
解:【查阅资料】金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜的化学方程式为4Al+3O2=2Al2O3,故填:4Al+3O2=2Al2O3。
【对比实验】(1)设计实验要注意控制变量,乙和甲一个是打磨的一个是没有打磨的,故的比较实验乙和实验甲可得知打磨能破坏氧化铝薄膜,故填:甲。
(2)实验乙中是铝和硫酸铜反应生成硫酸铝和铜,反应的化学方程式为2Al+3CuSO4═Al2(SO4)3+3Cu,据此可知金属活动性A1比Cu强,故填:2Al+3CuSO4═Al2(SO4)3+3Cu;强。
(3)H2O对氧化铝薄膜镁没有破坏作用。因为甲中硫酸铜溶液也含有水,没有明显现象,故填:甲中硫酸铜溶液也含有水,没有明显现象。
【猜测与探究】氯化钠中含有钠离子和氯离子,故可能是氯离子破坏了氧化铝薄膜,加入硫酸钠固体,氧化铝薄膜未被破坏,故不会有明显棉花,故填:
操作
现象
结论
推论
(1)向一支试管中再加入NaCl固体
铝丝表面析出红色固体
氧化铝薄膜被破坏
Na+或①Cl﹣能破坏氧化铝薄膜
(2)向另一支试管中再加入Na2SO4固体
②铝丝表面没有变化
氧化铝薄膜未被破坏
Na+和SO42﹣都不能破坏氧化铝薄膜
【结论与反思】
得出结论:根据实验可以看出,氯离子能破坏氧化铝薄膜,故前述猜测正确,故填:正确。
四、计算题(本题共8分)
14.【解答】解:
根据第一次固体减少4g,而第三次后质量不变,说明第二次也减少4g,所以a=12,第三次氧化铜完全反应,剩余的10g为铜单质,所以氧化铜的质量为10g,原固体混合物中,氧化铜的质量分数为×100%=50%,实验③中硫酸过量,所以所得溶液中的溶质是剩余的硫酸和生成的硫酸铜,对应的化学式为 H2SO4、CuSO4。
25g稀硫酸与4g氧化铜完全反应
设该实验所用稀硫酸中溶质的质量分数为x
CuO+H2SO4=CuSO4+H2O
80 98
4g 25gx
=
x=19.6%
故答案为:
(1)50%。
(2)12; H2SO4、CuSO4。
(3)19.6%。
相关文档
- 2019年全国各地中考化学试题-四川2021-11-119页
- 2019年全国各地中考化学试题-湖南2021-11-118页
- 2019年全国各地中考化学试题-山东2021-11-116页
- 2019年中考化学试题分类:化学研究和2021-11-112页
- 2019年中考化学试题分类:考点8 空气2021-11-111页
- 2019年中考化学试题分类:考点20 燃2021-11-114页
- 2019年中考化学试题分类:考点8 空气2021-11-114页
- 2019年中考化学试题分类:2研究化学2021-11-118页
- 2019年中考化学试题分类:考点7 化学2021-11-112页
- 2019年全国各地中考化学试题-吉林(2021-11-1114页