- 681.49 KB
- 2021-11-12 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
实验突破
(
三
)
影响过氧化氢分解速率因素的探究
回归教材
[
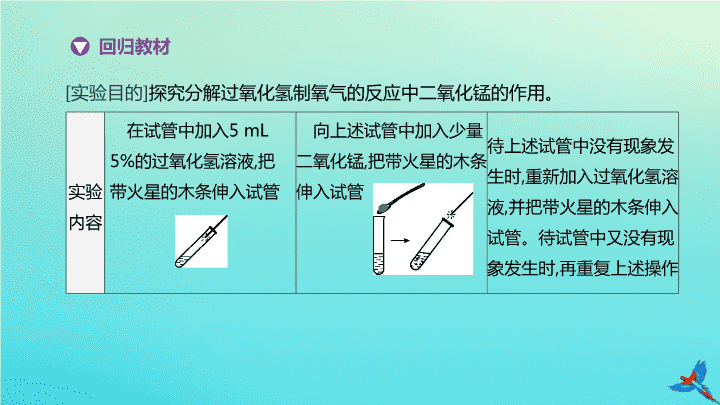
实验目的
]
探究分解过氧化氢制氧气的反应中二氧化锰的作用。
实验
内容
在试管中加入
5 mL 5%
的过氧化氢溶液
,
把带
火星的木条
伸入
试管
向上述试管中加入少量二氧化锰
,
把带火星的木条伸入
试管
待
上述试管中没有现象发生时
,
重新加入过氧化氢溶液
,
并把带火星的木条伸入试管。待试管中又没有现象发生时
,
再重复上述操作
实验
现象
①
_____________________
②
_____________________
③
_____________________
________________________
__________
解释
分析
④
_____________________
________________________
________________________
________
⑤
_____________________
________________________
_______________________
_
________________________
⑥
_____________________
________________________
________________________
________________
(续表)
带火星的木条不复燃
重新加入过氧化氢溶液后
,
带火星的木条又复燃
常温下过氧化氢分解速率慢
,
试管内氧气的浓度不足以使带火星的木条复燃
常温下
,
二氧化锰能加快过氧化氢分解的速率
,
试管内氧气的浓度升高
,
使带火星的木条复燃
氧气是过氧化氢分解产生的
,
二氧化锰只起加快过氧化氢分解产生氧气的作用
带火星的木条复燃
1.
小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题
,
进行如图
S3-1
所示探究实验
,
请回答有关问题。
(1)
向盛有过氧化氢溶液的试管中加入少量的二氧化锰后
,
再把带火星的木条伸入试管中
,
观察到的现象是
。
拓展训练
图
S3-1
溶液中有气泡产生
,
带火星的木条复燃
1.
小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题
,
进行如图
S3-1
所示探究实验
,
请回答有关问题。
(2)
要确定二氧化锰能对过氧化氢分解有催化作用
,
做了上述实验后
,
还需要确定两个因素
,
大龙同学补充设计了两个方面的探究实验
,
最终完成了对“命题”的实验证明。
①
第一方面的实验操作中包含了两次称量
,
其目的是
________________________
;
②
第二方面的实验想证明二氧化锰的化学性
质不变
,
方法是
__________________________
。
证明二氧化锰在反应
图
S3-1
取实验后的二氧化锰继续
前后质量不变
加入过氧化氢溶液
,
看是否还有氧气放出
1.
小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题
,
进行如图
S3-1
所示探究实验
,
请回答有关问题。
(3)
最后证明了二氧化锰是过氧化氢分解的催化剂
,
大楠同学利用此方法制取并收集了一集气瓶氧气
,
将带火星的木条伸入集气瓶内
,
木条没复燃
,
他说集气瓶内没有氧气
,
请你对大楠同学的结论进行评价
:_________________________________
。
不正确
,
将带火星的木条伸入集
图
S3-1
气瓶内
,
木条没复燃
,
只能说明集气瓶内氧气浓度较低
,
不能说明没有氧气
2.
科学探究是奇妙的过程
,
请你一起参与下列实验探究
,
并填写空白。
[
提出问题
]
小森同学在滴加氯化铁溶液时
,
不小心把滴加氯化铁溶液的滴管放入盛有过氧化氢溶液的试剂瓶中
,
发现有大量的气泡产生。小森联想到二氧化锰可作过氧化氢分解的催化剂
,
氯化铁溶液是否也可以作过氧化氢分解的催化剂呢
?
于是他做了以下探究。
[
猜想与假设
]
氯化铁溶液能作过氧化氢分解的催化剂。
[
设计与实验
]
实验步骤
实验现象
实验结论
在一支试管中加入
5 mL 15%
的过氧化氢溶液
,
然后滴入适量的氯化铁溶液
,
把带火星的木条伸入试管
氯化铁溶液可以作过氧化氢分解的催化剂
[
答案
] [
设计与实验
]
有气泡冒出
,
木条复燃
[
解析
] [
设计与实验
]
因为结论中
FeCl
3
溶液可以作
H
2
O
2
分解的催化剂
,
因此有氧气放出
,
木条复燃。
2.
科学探究是奇妙的过程
,
请你一起参与下列实验探究
,
并填写空白。
[
提出问题
]
小森同学在滴加氯化铁溶液时
,
不小心把滴加氯化铁溶液的滴管放入盛有过氧化氢溶液的试剂瓶中
,
发现有大量的气泡产生。小森联想到二氧化锰可作过氧化氢分解的催化剂
,
氯化铁溶液是否也可以作过氧化氢分解的催化剂呢
?
于是他做了以下探究。
[
猜想与假设
]
氯化铁溶液能作过氧化氢分解的催化剂。
[
讨论与反思
]
已知氯化铁溶液中含有水、铁离子和氯离子三种粒子
,
小森同学又做了以下三种猜想
:
猜想
1:
真正催化过氧化氢分解的是氯化铁溶液中的水
;
猜想
2:
真正催化过氧化氢分解的是氯化铁溶液中的铁离子
;
猜想
3:
真正催化过氧化氢分解的是氯化铁溶液中的氯离子。
(1)
你认为最不可能的是哪一种猜想
?
,
理由是
。
(2)
小森同学又对余下的猜想进行了实验探究
,
请你帮助他填写下表
:
(3)
你认为小森同学的哪一种猜想正确
?
,
理由是
。
实验步骤
实验现象
实验结论
向盛有
5 mL 15%
的过氧化氢溶液的试管中加入少量的盐酸
(
含有水分子和氯离子的一种溶液
),
然后把带火星的木条伸入试管中
无明显
现象
[
答案
]
[
讨论与反思
] (1)
猜想
1
过氧化氢溶液中有水
(2)
猜想
3
不正确
(3)
猜想
2
盐酸溶液中有水分子和氯离子
,
实验中无明显现象
[
解析
] [
讨论与反思
]
过氧化氢溶液中有水
,
因此猜想
1
不正确
;
小森同学向盛有
5 mL 15%
的
H
2
O
2
溶液的试管中加入少量的盐酸
,
然后把带火星的木条伸入试管中
,
无明显现象
,
说明猜想
3
不正确。则猜想
2
是正确的。
3.
同学们应用数字化实验探究外界条件对过氧化氢溶液分解速率的影响。实验装置如下
:
图
S3-2
[
进行实验
]
实验序号
主要实验步骤
装置内压强—时间图像
实验
1
①1
号抽滤瓶中不加任何试剂
,2
号抽滤瓶中加入
0.2 g MnO
2
粉末
,3
号抽滤瓶中加入
0.2 g FeCl
3
粉末
②
用三个分液漏斗分别加入
15 mL 4%
的
H
2
O
2
溶液
(续表)
实验序号
主要实验步骤
装置内压强—时间图像
实验
2
①
三个抽滤瓶中分别加入
0.2 g FeCl
3
粉末
②
分别用
1
号分液漏斗加入
15 mL 2%
的
H
2
O
2
溶液
,
用
2
号分液漏斗加入
15 mL 4%
的
H
2
O
2
溶液
,
用
3
号分液漏斗加入
15 mL 6%
的
H
2
O
2
溶液
(续表)
实验序号
主要实验步骤
装置内压强—时间图像
实验
3
①
三个抽滤瓶中分别加入
0.2 g FeCl
3
粉末
,
分别放入装有
10 ℃
、
20 ℃
、
40 ℃
水的水槽中
②
用三个分液漏斗分别加入
15 mL 4%
的
H
2
O
2
溶液
[
解释与结论
]
(1)
实验
1
的
2
号抽滤瓶中发生反应的化学方程式为
。
(2)
某同学得到“不同催化剂的催化效果不同”的结论
,
他的依据是
____________
。
(3)
通过上述实验得到
:
影响该反应速率的外界因素有
________________________
。
[
反思与评价
]
(4)
经过多次实验
,
有的同学对比实验
1
的
3
号瓶、实验
2
的
2
号瓶中同为
40 s
时的气体压强
,
发现存在较大的差异
,
可能的原因是
。
实验
1
中
2
、
催化剂种类、反应物
实验温度不同
3
号瓶曲线不同
浓度、温度
4.
用过氧化氢溶液制氧气
,
探究不同催化剂催化过氧化氢分解的效果。
[
查阅资料
]
①MnO
2
、
Cr
2
O
3
、
Fe
2
O
3
、
CuO
、
S
对过氧化氢的分解均具有催化作用。
②
海藻酸钠可以作为催化剂的载体支架
,
形成负载不同催化剂的海藻酸钠微球。
[
进行实验
]
①
制备五种负载不同催化剂
(MnO
2
、
Cr
2
O
3
、
Fe
2
O
3
、
CuO
、
S)
的海藻酸钠微球
,
每个微球大小相同
,
且负载催化剂的质量相等。
②
取
30
粒负载某种催化剂的海藻酸钠微球与
20 mL
质量分数为
5%
的过氧化氢溶液
,
在锥形瓶中迅速混合发生反应
,
实验装置如图
S3-3Ⅰ
所示
,
采集
200 s
内压强数据
,
绘制曲线如图
Ⅱ
。
图
S3-3Ⅰ
[
实验分析
]
①
每次实验时
,
海藻酸钠微球数应相同的原因是
______________________________
。
②
本实验中
,
通过一段时间内
来反映生成氧气的快慢。
③
本实验中
,
负载
MnO
2
的微球显示了良好的催化效果
,60 s
时竟将橡胶塞弹飞
,
在图
Ⅱ
中对应的曲线是
(
填“
a
”或“
b
”
);
负载
的微球催化效果较好
,
反应温和
;
负载
Fe
2
O
3
、
Cr
2
O
3
的微球催化效果一般
;
负载
的微球催化能力最弱。
控制变量
,
保证负载的催化剂
压强变化的数值
a
CuO
S
的总质量相等