- 167.72 KB
- 2022-04-13 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
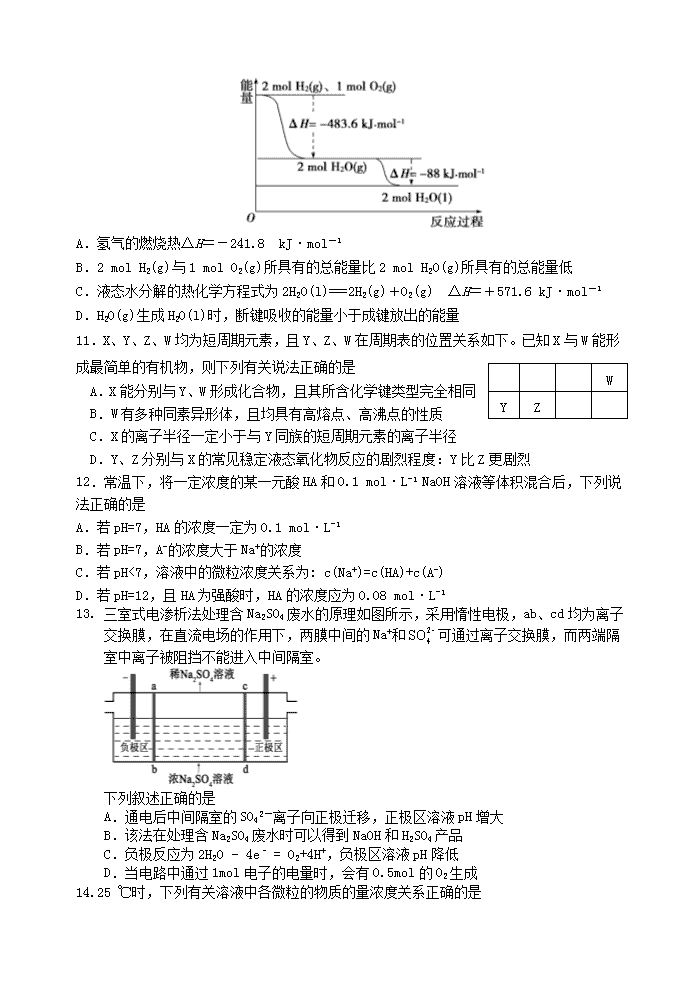
湛江一中2018-2019学年度第一学期“第一次大考”高二级化学科试卷A卷考试时间:70分钟满分:100分注意事项:1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、考试号填写在答题卡上。2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。可能用到的相对原子质量:H-1C-12N-14O-16Mg-24Al-27S-32Cl-35.5Ca-40Fe-56Zn-65一、选择题:(共14小题,每小题只有一个合理答案,每小题3分,共42分)1.我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指A.萃取B.渗析C.蒸馏D.干馏2.以下关于甲烷的说法中错误的是A.甲烷分子是由极性键构成的分子B.甲烷分子具有正四面体结构C.甲烷分子中四个C-H键是完全等价的键D.甲烷分子中具有非极性键3.类推是学习和研究的重要思维方法。下列类推结论正确的是化学事实类推结论AAl在O2中燃烧生成Al2O3Fe在O2中燃烧也生成Fe2O3BpH=3的盐酸稀释1000倍后pH=6pH=6的盐酸稀释1000倍后pH=9C用电解熔融MgCl2的方法冶炼金属镁用电解熔融NaCl的方法制取金属钠D将CO2和Na2O2反应生成Na2CO3与O2将SO2与Na2O2反应生成Na2SO3与O24.NA为阿伏加德罗常数的值.下列叙述正确的是A.在1.0mol·L-1的NaHCO3溶液中,含有的Na+数为1NAB.标准状况下,2.24LCCl4中含有的分子总数为0.1NAC.金属钠与水反应,生成22.4L氢气时,转移的电子数为2NAD.1mol氢氧根离子与1mol铵根离子所含电子数均为10NA5.下列有关实验装置进行的相应实验,能达到实验目的的是n稀盐酸(加3滴酚酞)饱和NaHCO3溶液 图(1) 图(2) 图(3) 图(4)A.图(1)用于除去CO2中的HCl气体B.图(2)表示已组装的铜锌原电池C.图(3)用于测定某稀盐酸的物质的量浓度D.用图(4)装置制备Fe(OH)2并能较长时间观察其颜色6.可逆反应:2NO2(g)⇌2NO(g)+O2(g),在2L的密闭容器中反应,达到平衡的标志是A单位时间内生成nmol O2的同时生成2nmol NOB.用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态C.混合气体的颜色不再改变的状态 D混合气体的密度不再改变的状态7.下列离子方程式正确的是A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO-B.双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2OC.用铜做电极电解CuSO4溶液:2Cu2++2H2O2Cu+O2↑+4H+D.Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O8.下列说法正确的是A.无论是纯水,还是酸性、碱性或中性稀溶液,其c(H+)·c(OH-)=1×10-14B.c(H+)=1×10-7mol·L-1的溶液一定是中性溶液C.常温下,Ksp[Mg(OH)2]=5.6×10−12,pH=10的含Mg2+溶液中,c(Mg2+)≤5.6×10−4mol·L−1D.加热蒸干AlCl3溶液然后灼烧得到Al(OH)3固体9.下列说法正确的是A.升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子百分数,从而使反应速率增大C.增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多D.催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率10.依据如图判断,下列说法正确的是nA.氢气的燃烧热ΔH=-241.8kJ·mol-1B.2molH2(g)与1molO2(g)所具有的总能量比2molH2O(g)所具有的总能量低C.液态水分解的热化学方程式为2H2O(l)===2H2(g)+O2(g) ΔH=+571.6kJ·mol-1D.H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量WYZ11.X、Y、Z、W均为短周期元素,且Y、Z、W在周期表的位置关系如下。已知X与W能形成最简单的有机物,则下列有关说法正确的是A.X能分别与Y、W形成化合物,且其所含化学键类型完全相同B.W有多种同素异形体,且均具有高熔点、高沸点的性质C.X的离子半径一定小于与Y同族的短周期元素的离子半径D.Y、Z分别与X的常见稳定液态氧化物反应的剧烈程度:Y比Z更剧烈12.常温下,将一定浓度的某一元酸HA和0.1mol·L-1NaOH溶液等体积混合后,下列说法正确的是A.若pH=7,HA的浓度一定为0.1mol·L-1B.若pH=7,A-的浓度大于Na+的浓度C.若pH<7,溶液中的微粒浓度关系为:c(Na+)=c(HA)+c(A-)D.若pH=12,且HA为强酸时,HA的浓度应为0.08mol·L-113.三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是A.通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品C.负极反应为2H2O−4e–=O2+4H+,负极区溶液pH降低D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成14.25℃时,下列有关溶液中各微粒的物质的量浓度关系正确的是nA.0.1mol/L的NH4Cl溶液:c(Cl-)>c(NH)>c(OH-)>c(H+)B.0.1mol/L的CH3COOH溶液:c(CH3COOH)>c(H+)>c(CH3COO-)>c(OH-)C.pH=4的FeCl3溶液:c(Cl-)>c(H+)>c(Fe3+)>c(OH-)D.pH=11的CH3COONa溶液:c(Na+)+c(H+)=c(CH3COO-)+c(CH3COOH)二、非选择题:(共4题,每空2分,共58分)15.(14分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液,在如图所示的装置中进行中和反应。测定强酸与强碱反应的反应热。 起始温度t1/℃终止温度t2/℃温度差(t2-t1)/℃HClNaOH平均值125.525.025.2528.53.25224.524.524.5027.53.00325.024.524.7526.51.75(1)从实验装置上看,图中尚缺少的一种玻璃仪器是_________。(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是______________________________。(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指______________________________温度。(4)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大”、“偏小”、“无影响”)。(5)计算该实验发生中和反应时放出的热量为________________kJ(中和后生成的溶液的比热容c=4.18J/(g·℃)(保留两位小数)。(6)如果用50mL0.55mol/L的氨水(NH3·H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,则△H会(填“偏大”、“偏小”、“无影响”),其原因是。16.(14分)某研究小组用下图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。Na2SO3固体(1)配制氯化铁溶液时,需先把氯化铁晶体溶解在盐酸中,再加水稀释,这样操作的目的是。(2)通入足量SO2时,装置C中观察到的现象为。(3)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。①写出SO2与FeCl3溶液反应的离子方程式;②检验有Fe2+生成的方法是;n③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-,该做法不合理,理由是。(4)D装置中倒置漏斗的作用是。(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有(填字母)。a.浓H2SO4b.酸性KMnO4溶液 c.碘水d.NaCl溶液17.(14分)活性氧化锌是一种多功能性的新型无机材料。某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如下:25%稀硫酸H2O2溶液ZnO粉Zn粉热NH4HCO3溶液滤渣ⅡCO2滤渣Ⅲ粗ZnO浸取液滤液滤渣(碱式碳酸锌)滤液活性ZnOII氧化I浸取IIIIV碳化煅烧已知各相关氢氧化物沉淀pH范围如下表所示:Zn(OH)2Fe(OH)2Fe(OH)3Cu(OH)2开始沉淀pH5.47.02.34.7完全沉淀pH8.09.04.16.7完成下列填空:(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯、量筒外,还需要 (选填编号)A.天平B.滴定管C.容量瓶D.胶头滴管(2)步骤II中加入H2O2溶液的作用是(用离子方程式表示);(3)用ZnO调节pH,以除去含铁杂质,调节pH的适宜范围是 。(4)步骤III中加入Zn粉的作用是:① ;②进一步调节溶液pH。(5)碱式碳酸锌[Zn2(OH)2CO3]煅烧的化学方程式为。(6)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):①取1.000g活性氧化锌,用15.00mL1.000mol·L-1硫酸溶液完全溶解,滴入几滴甲基橙。②用浓度为0.5000mol·L-1的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL。判断滴定终点的依据是;所得活性氧化锌的纯度为 。高温18.(16分)除去水蒸气后的水煤气主要含H2、CO、CO2及少量的H2S、CH4,继续除去H2S后,可采用催化或非催化转化技术,将CH4转化成CO,得到CO、CO2和H2的混合气体,是理想的合成甲醇原料气。(1)制水煤气的主要化学反应方程式为:C(s)+H2O(g)CO(g)+H2(g)n,此反应是吸热反应。①此反应的化学平衡常数表达式为;②下列能增大碳的转化率的措施是。A.加入C(s)B.加入H2O(g)C.升高温度D.增大压强(2)将CH4转化成CO,工业上常采用催化转化技术,其反应原理为:CH4(g)+O2(g)CO(g)+2H2O(g)△H=-519kJ/mol。工业上要选择合适的催化剂,分别对X、Y、Z三种催化剂进行如下实验(其他条件相同)①X在750℃时催化效率最高,能使正反应速率加快约3×105倍;②Y在600℃时催化效率最高,能使正反应速率加快约3×105倍;③Z在440℃时催化效率最高,能使逆反应速率加快约1×106倍;根据上述信息,你认为在生产中应该选择的适宜催化剂是(填“X”或“Y”或“Z”),选择的理由是。(3)合成气合成甲醇的主要反应是:2H2(g)+CO(g)CH3OH(g)△H=-90.8kJ·mol-1T℃时,此反应的平衡常数为160,此温度下,在密闭容器中开始只加入CO、H2,反应10min后测得各组分的浓度如下:物质H2COCH3OH浓度/(mol·L-1)0.20.10.4①该时间段内反应速率v(H2)=mol·L-1·min-1。②此时,正、逆反应速率的大小:(填“>”、“<”或“=”)(4)生产过程中,合成气要进行循环,其目的是。(5)甲醇可制成新型燃料电池,总反应为:2CH3OH+3O2+4KOH=2K2CO3+6H2O该电池负极的电极反应式为。湛江一中2018-2019学年度第一学期“第一次大考”高二级化学科试卷A卷(参考答案及评分标准)一、选择题:(共14小题,每小题只有一个合理答案,每小题3分,共42分)1.C2.D3.C4.D5.A6.C7.B8.C9.A10.C11.D12.D13.B14.B二、非选择题:(共4题,每空2分,共58分)15.(14分)(1)环形玻璃搅拌棒(2分)n(2)减少实验过程中的热量损失(2分)(3)完全反应后混合溶液的最高温度(2分) (4)偏小(2分)(5)1.31kJ(2分)(6)偏大(2分)NH3.H2O是弱电解质,电离需要吸热(或生成的盐会水解,要吸收热量等)(2分)16.(14分)(1)抑制氯化铁水解(2分)(2)溶液由棕黄色变为浅绿色(2分)(3)①2Fe3++SO2+2H2O=SO42-+4H++2Fe2+(2分,没有配平扣1分)②取少量C中反应后的溶液于试管中,向其中滴入酸性高锰酸钾溶液,若褪色,说明有亚铁离子,不褪色说明没有没有亚铁离子(2分,合理答法可以给分)③硝酸可以将溶解的SO2氧化为H2SO4,干扰试验(2分)(4)使气体充分吸收;防止溶液倒吸(2分);(5)b、c(2分,答1个对的得1分)17.(1)D(2分)(2)H2O2+2Fe2++2H+=2Fe3++2H2O(2分,没有配平扣1分)(3)4.1~4.7(2分);(4)除去溶液中的Cu2+(2分)高温(5)Zn2(OH)2CO3=2ZnO+CO2↑+H2O(2分,没有配平扣1分)(6)当滴入最后一滴0.5000mol·L-1的氢氧化钠溶液时,溶液由橙色变为黄色且半分钟内不变色(2分)97.2%(2分)18.(16分)(1)①(2分)②BC(2分,答1个对的给1分,若有1个错误,得0分)(2)Z(2分)催化效率高且活性温度低(或催化活性高、速度快,反应温度低)(2分)(3)①0.08(2分)②>(2分)(4)提高原料利用率(或提高产量、产率也可)(2分)(5)CH3OH﹣6e-+8OH﹣=CO32-+6H2O(2分)