- 621.17 KB
- 2022-04-12 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
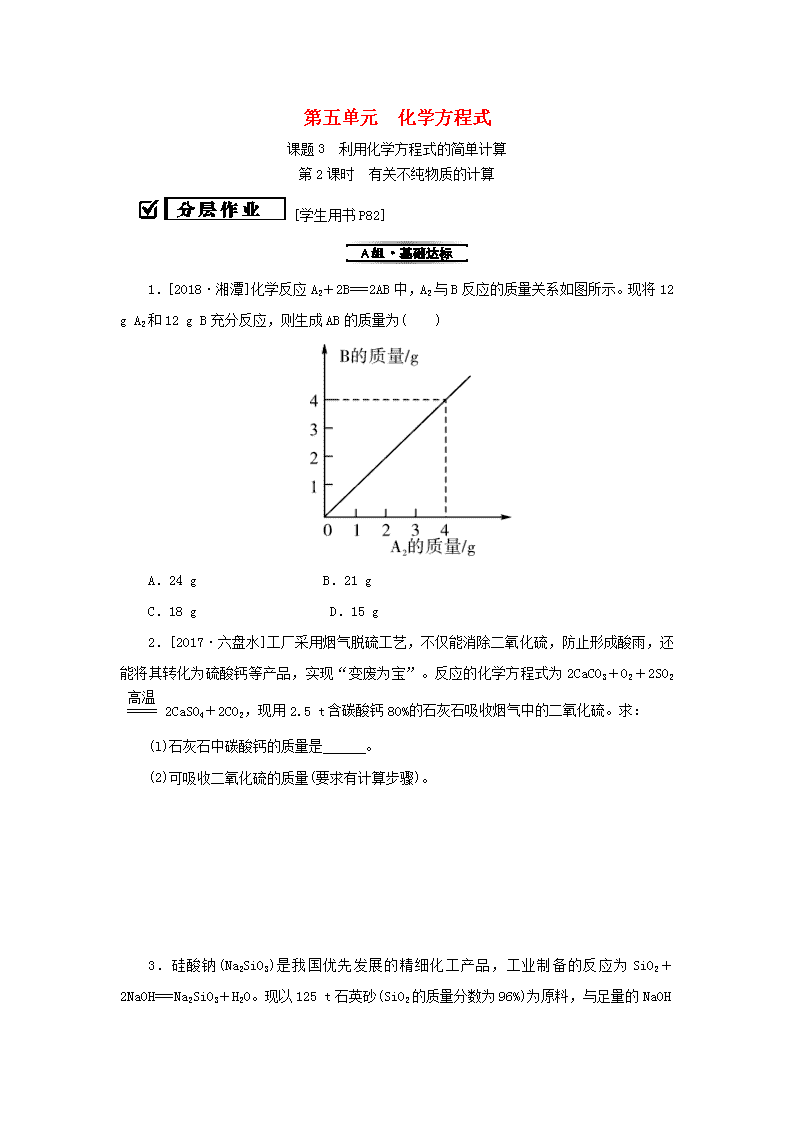
第五单元 化学方程式课题3 利用化学方程式的简单计算第2课时 有关不纯物质的计算[学生用书P82]1.[2018·湘潭]化学反应A2+2B===2AB中,A2与B反应的质量关系如图所示。现将12gA2和12gB充分反应,则生成AB的质量为( )A.24gB.21gC.18gD.15g2.[2017·六盘水]工厂采用烟气脱硫工艺,不仅能消除二氧化硫,防止形成酸雨,还能将其转化为硫酸钙等产品,实现“变废为宝”。反应的化学方程式为2CaCO3+O2+2SO22CaSO4+2CO2,现用2.5t含碳酸钙80%的石灰石吸收烟气中的二氧化硫。求:(l)石灰石中碳酸钙的质量是。(2)可吸收二氧化硫的质量(要求有计算步骤)。3.硅酸钠(Na2SiO3)是我国优先发展的精细化工产品,工业制备的反应为SiO2+2NaOH===Na2SiO3+H2O。现以125t石英砂(SiO2的质量分数为96%)为原料,与足量的NaOHn溶液反应。试计算:(1)125t石英砂中SiO2的质量。(2)理论上得到硅酸钠的质量。4.[2017·山西]在一次实验课上,同学们用加热氯酸钾和二氧化锰混合物的方法制取氧气。他们取了24.5g的混合物,其中二氧化锰的质量分数为20%,加热到完全分解。通过计算,得出他们制得氧气的质量是多少?n5.高铁酸钾(K2FeO4)是一种集吸附、凝聚、杀菌等多功能的新型、高效能水处理剂。198℃以下时能稳定存在,但受热易分解(4K2FeO42Fe2O3+4K2O+3O2↑)、遇水将变质[4K2FeO4+10H2O===4Fe(OH)3+8KOH+3O2↑]。根据要求回答下列问题:(1)取等质量的两份高铁酸钾固体分别加热、与水反应,请通过观察上述化学方程式,判断充分反应后产生氧气的质量(填“相等”“不相等”或“无法确定”)。(2)为检测实验室新买的高铁酸钾固体样品中高铁酸钾的质量分数,某同学取10g样品进行实验,共收集到氧气0.96g。试通过计算求该样品中高铁酸钾的质量分数。参考答案1.A【解析】根据关系图分析可知,参加反应的A2和B的质量比为1∶1,根据A2+2B===2AB可知,该反应为化合反应,12gA2和12gB充分反应,生成物的质量为两者之和,即12g+12g=24g。故选A。n2.(l)2t(2)解:设可吸收二氧化硫的质量是x。2CaCO3+O2+2SO22CaSO4+2CO22001282tx= x=1.28t答:可吸收二氧化硫的质量为1.28t。3.解:(1)石英砂中的SiO2的质量为:125t×96%=120t(2)设生成硅酸钠的质量为x。2NaOH+SiO2===Na2SiO3+H2O 60 122 120t x= x=244t答:(1)125t石英砂中SiO2的质量为120t;(2)理论上得到硅酸钠的质量为244t。4.解:24.5g氯酸钾和二氧化锰的混合物中,二氧化锰的质量分数为20%,则参加反应的氯酸钾质量为24.5g×(1-20%)=19.6g。设制得氧气的质量为x。2KClO32KCl+3O2↑ 245 96 19.6g x= x=7.68g答:制得氧气的质量是7.68g。5.(1)相等(2)解:设10g高铁酸钾固体样品中含高铁酸钾的质量为x。4K2FeO42Fe2O3+4K2O+3O2↑ 792 96n x 0.96g= x=7.92g所以样品中高铁酸钾的质量分数为:×100%=79.2%。答:该样品中高铁酸钾的质量分数为79.2%。