- 339.51 KB
- 2022-04-12 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
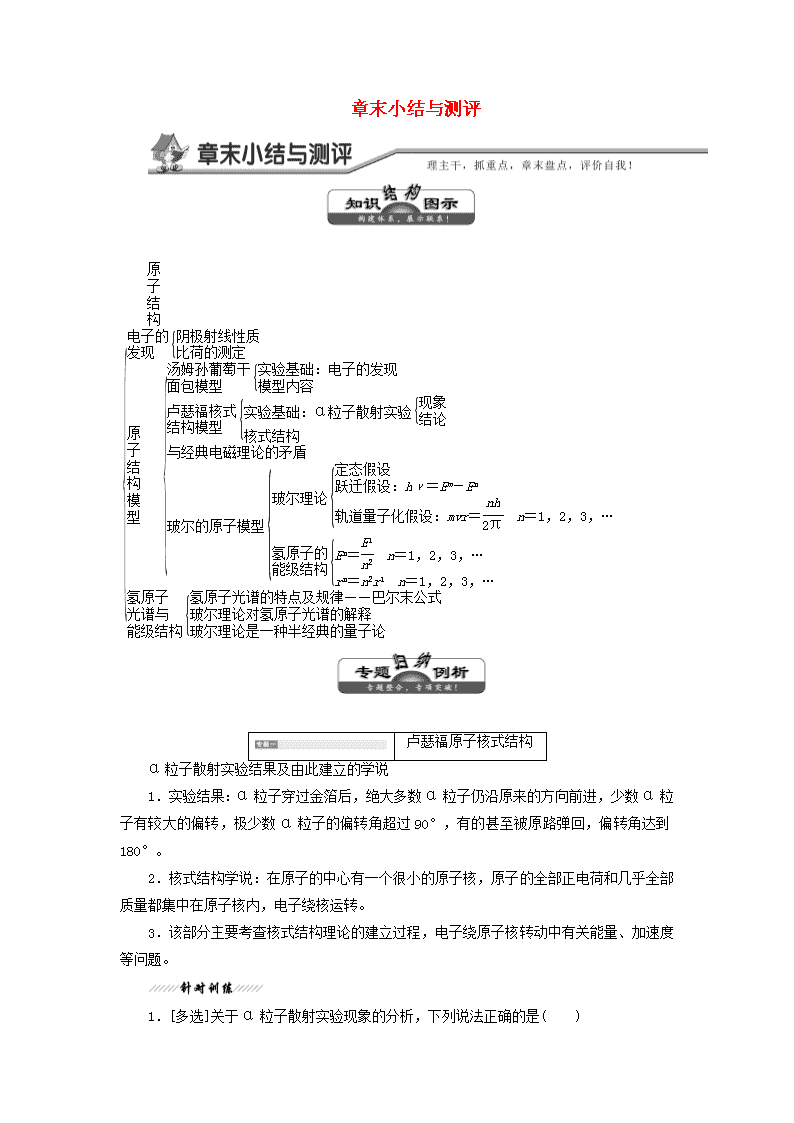
章末小结与测评卢瑟福原子核式结构α粒子散射实验结果及由此建立的学说1.实验结果:α粒子穿过金箔后,绝大多数α粒子仍沿原来的方向前进,少数α粒子有较大的偏转,极少数α粒子的偏转角超过90°,有的甚至被原路弹回,偏转角达到180°。2.核式结构学说:在原子的中心有一个很小的原子核,原子的全部正电荷和几乎全部质量都集中在原子核内,电子绕核运转。3.该部分主要考查核式结构理论的建立过程,电子绕原子核转动中有关能量、加速度等问题。1.[多选]关于α粒子散射实验现象的分析,下列说法正确的是( )nA.绝大多数α粒子沿原方向运动,说明正电荷在原子内均匀分布,是α粒子受力平衡的结果B.绝大多数α粒子沿原方向运动,说明这些α粒子未受到明显的力的作用,说明原子是“中空”的C.极少数α粒子发生大角度偏转,说明原子内质量和电荷量比α粒子大得多的粒子在原子内分布空间很小D.极少数α粒子发生大角度偏转,说明原子内的电子对α粒子的吸引力很大解析:选BC 在α粒子散射实验中,绝大多数α粒子沿原方向运动,说明α粒子未受到原子核明显的力的作用,也说明原子核相对原子来讲很小,原子内大部分空间是空的,故A错,B对;极少数发生大角度偏转,说明受到原子核明显的力的作用的空间在原子内很小,α粒子偏转,而原子核未动,说明原子核的质量和电荷量远大于α粒子的质量和电荷量,电子的质量远小于α粒子的质量,α粒子打在电子上,不会有明显偏转,故C对,D错。玻尔理论与能级跃迁1.轨道半径与能级公式rn=n2r1,En=,其中n=1,2,3,…为轨道量子数,r1=0.53×10-10m,E1=-13.6eV。2.原子的能级跃迁和电离(1)跃迁:跃迁是原子的电子从一个轨道跃迁到另一个轨道,即不能脱离原子核的束缚,所以在跃迁的过程中,原子放出或吸收的能量必须是量子化的。如当电子从m轨道跃迁到n轨道时,其能量变化必须是ΔE=-,当m>n时,ΔE<0,原子要放出能量;当m<n时,ΔE>0,原子要吸收能量。(2)电离:电离是将原子的电子变成自由电子,只要电离能大于一定值就可以,没有量子化要求,若有多余的能量,则以电子动能的形式存在。如将在m轨道的电子电离出来,原子吸收的能量ΔE>0-就可以了。3.辐射光子的种类或光谱线条数N=Cn2=4.氢原子的能量及其变化(1)En=Ekn+Epn,其中En、Ekn、Epn分别为原子能量(级)、电子动能、原子势能。(2)Epn=-。n(3)Ekn==。(4)En=-Ekn=-。当原子由低能级向高能级跃迁时,En增大,Ep增大,Ek减小。反之,则亦反之。2.处于n=3的氢原子能够自发地向低能级跃迁,(1)跃迁过程中电子动能和原子能量如何变化?(2)可能辐射的光子波长是多少?(普朗克常量h=6.63×10-34J·s)解析:(1)由于电子从外轨道进入内轨道,半径变小,由于=,则Ek=mv2=,由此可知动能增大;在此过程中,原子向外辐射光子,因此原子能量减少。(2)原子的可能跃迁及相应波长①从n=3到n=2而E3=-1.51eV E2=-3.4eV由hν=h=Em-En得λ1==m=6.58×10-7m。②从n=3到n=1而E1=-13.60eVλ2==m=1.03×10-7m。③从n=2到n=1则λ3==m=1.22×10-7m。答案:(1)电子动能增大,原子能量减少(2)6.58×10-7m 1.03×10-7m 1.22×10-7mn(时间:60分钟 满分:100分)一、选择题(共8小题,每小题6分,共48分)1.卢瑟福通过对α粒子散射实验结果的分析,提出了原子内部存在( )A.电子 B.中子C.质子D.原子核解析:选D 卢瑟福在α粒子散射实验中观察到绝大多数α粒子穿过金箔后几乎不改变运动方向,只有极少数的α粒子发生了大角度的偏转,说明在原子的中央存在一个体积很小的带正电的物质,将其称为原子核。故选项D正确。2.在卢瑟福α粒子散射实验中,金箔中的原子核可以看做静止不动;下列各图画出的是其中两个α粒子经历金箔散射过程的径迹,其中正确的是( )解析:选C 金箔中的原子核与α粒子都带正电,α粒子接近原子核过程中受到斥力而不是引力作用,A、D错误;由原子核对α粒子的斥力作用,及物体做曲线运动的条件,知曲线轨迹的凹侧应指向受力一方,选项B错、C对。3.氢原子从n=4的激发态直接跃迁到n=2的激发态时,发出蓝色光,则当氢原子从n=5的激发态直接跃迁到n=2的激发态时,可能发出的光是( )A.红外线B.红光C.紫光D.γ射线解析:选C 氢原子从n=4、5的能级向n=2的能级跃迁时辐射的光为可见光,且辐射光子的能量满足hν=Em-En,能级差越大,光频率越高,而紫色光的频率高于蓝色光的频率,综上所述,选项C正确。4.一个氢原子中的电子从一半径为ra的轨道自发地直接跃迁至另一半径为rb的轨道,已知ra>rb,则在此过程中( )A.原子发出一系列频率的光子B.原子要吸收一系列频率的光子C.原子要吸收某一频率的光子D.原子要辐射某一频率的光子解析:选D 电子的轨道半径减小,电子从高能级直接跃迁到低能级,只能放出具有对应该能量差的频率的光子,故D正确。5.如图所示为氢原子的能级图,用光子能量为13.06neV的光照射一群处于基态的氢原子,可能观测到氢原子发射的不同波长的光有( )A.15种 B.10种C.4种D.1种解析:选B 处于基态的氢原子吸收入射光子的能量后由低能级向高能级跃迁,处于不稳定状态,然后由高能级向低能级跃迁,根据题意,hν=E5-E1=13.06eV,故可能发射C52=10种光。6.[多选]玻尔在他提出的原子模型中所做的假设有( )A.原子处在具有一定能量的定态中,虽然电子做加速运动,但不向外辐射能量B.原子的不同能量状态与电子沿不同的圆轨道绕核运动相对应,而电子的可能轨道的分布是不连续的C.电子从一个轨道跃迁到另一个轨道时,辐射(或吸收)一定频率的光子D.电子跃迁时辐射的光子的频率等于电子绕核做圆周运动的频率解析:选ABC A、B、C三项都是玻尔提出来的假设,其核心是原子定态概念的引入与能级跃迁学说的提出,也就是“量子化”概念,原子的不同能量状态与电子绕核运动不同的圆轨道相对应,是经典理论与量子化概念的结合。电子跃迁辐射的能量为hν=Em-En,与电子绕核做的圆周运动无关。故D错。7.[多选]设氢原子由n=3的状态向n=2的状态跃迁时放出能量为E、频率为ν的光子。则氢原子( )A.跃迁时可以放出或吸收能量为任意值的光子B.由n=2的状态向n=1的状态跃迁时放出光子的能量大于EC.由n=2的状态向n=3的状态跃迁时吸收光子的能量等于ED.由n=4的状态向n=3的状态跃迁时放出光子的频率大于ν解析:选BC 原子跃迁时可以放出或吸收能量为特定值的光子,A错;由n=2的状态向n=1的状态跃迁时,放出的能量比由n=3的状态向n=2的状态跃迁时要大,所以放出光子的能量大于E,B项正确;由n=2的状态向n=3的状态跃迁时吸收光子的能量等于由n=3的状态向n=2的状态跃迁时放出的能量E,C项正确;由n=4的状态向n=3的状态跃迁时放出光子的能量较小,所以频率小于ν,D项错。8.[多选]氢原子能级如图所示,当氢原子从n=3跃迁到n=2的能级时,辐射光的波长为656nm。以下判断正确的是( )A.氢原子从n=2跃迁到n=1的能级时,辐射光的波长大于656nmB.用波长为325nm的光照射,可使氢原子从n=1跃迁到n=2的能级C.一群处于n=3能级上的氢原子向低能级跃迁时最多产生3种谱线D.用波长为633nm的光照射,不能使氢原子从n=2跃迁到n=3的能级解析:选CD 根据氢原子的能级图和能级跃迁规律,当氢原子从n=2能级跃迁到nn=1的能级时,辐射光的波长一定小于656nm,因此A选项错误;根据发生跃迁只能吸收和辐射一定频率的光子,可知B选项错误,D选项正确;一群处于n=3能级上的氢原子向低能级跃迁时可以产生3种频率的光子,所以C选项正确。二、非选择题(共4小题,共52分)9.(12分)氢原子第n能级的能量为En=,其中E1为基态能量。当氢原子由第4能级跃迁到第2能级时,发出光子的频率为ν1;若氢原子由第2能级跃迁到基态,发出光子的频率为ν2,求的值。解析:根据En=及hν=Em-En可得hν1=-,hν2=-E1,两式联立解得=。答案:10.(12分)已知氢原子量子数为n的能级值为En=eV,试计算处于基态的氢原子吸收频率为多少的光子,电子可以跃迁到n=2轨道上?解析:氢原子基态时的能量E1=eV=-13.6eV,氢原子在n=2能级的能量E2=eV=-3.4eV。氢原子由基态跃迁到n=2能级需要的能量ΔE=E2-E1=[-3.4-(-13.6)]eV=10.2eV=1.632×10-18J根据玻尔理论hν=ΔE得ν==Hz≈2.46×1015Hz。答案:2.46×1015Hz11.(14分)原子可以从原子间的碰撞中获得能量,从而发生能级跃迁(在碰撞中,动能损失最大的是完全非弹性碰撞)。一个具有13.60neV动能、处于基态的氢原子与另一个静止的、也处于基态的氢原子发生对心正碰,问是否可以使基态氢原子发生能级跃迁?(氢原子能级如图所示)解析:设运动氢原子的速度为v0,发生完全非弹性碰撞后两者的合速度为v,损失的动能ΔE被基态氢原子吸收。若ΔE=10.2eV,则基态氢原子可由n=1能级跃迁到n=2能级,由动量守恒和能量守恒得mv0=2mv①mv02=mv2×2+ΔE②mv02=13.60eV③由①②③得ΔE=6.8eV<10.2eV,所以不能使基态氢原子发生跃迁。答案:不能12.(14分)已知基态氢原子的电子的轨道半径r1=0.528×10-10m,根据玻尔假设,电子绕核的可能轨道半径是rn=n2r1(n=1,2,3,…)。电子在不同轨道上对应的能级如图所示。(1)有一群氢原子处于量子数n=3的激发态,在图上用箭头标出这些氢原子能发出哪几条光谱线?其中有几条属于巴尔末线系?(2)计算这几条光谱线中波长最短的一条的波长。(已知静电力常量k=9.0×109N·m2/C2,h=6.63×10-34J·s,e=1.6×10-19C)解析:(1)可能发出3条光谱线,如图:从3→2跃迁发出的光子属于巴尔末线系,故只有1条。(2)原子由n=3的激发态向基态跃迁发出的光子的波长最短。由h·=E3-E1得λ==m=1.03×10-7m。答案:(1)3条 图见解析 1条 (2)1.03×10-7m