- 878.71 KB
- 2022-04-12 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
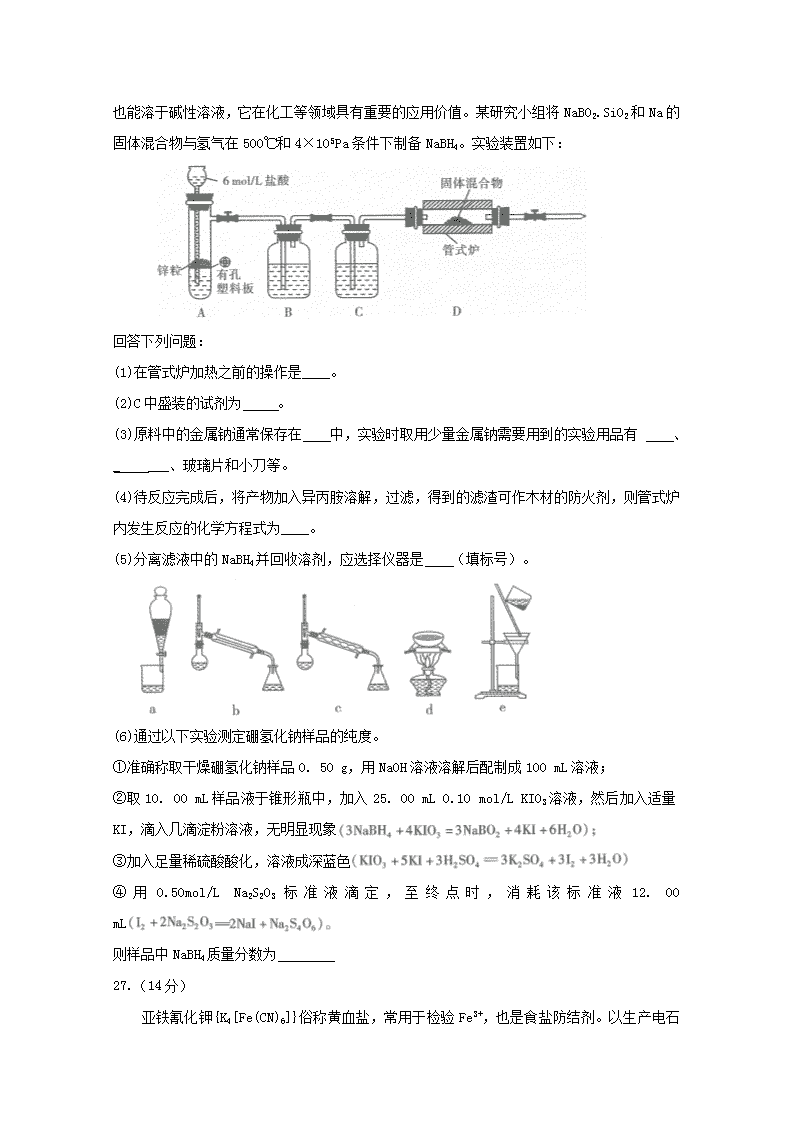
甘肃省白银市2019届高三化学模拟试题(一)可能用到的相对原子质量:可能用到的相对原子质量:H1811C12N14016Na23Mg24S32Fe56一、选择题:本题共7个小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。7.在日常生活中,下列做法值得提倡的是A.将生活垃圾分类处理B.将废旧塑料深挖填埋C.选用一次性碗筷和纸杯D.利用焚烧秸杆施肥8.某地区已探明蕴藏着丰富的赤铁矿、煤、石灰石和黏土,现拟建设大型炼铁厂和与之相关联的焦化厂、发电厂、水泥厂等。下图中工厂名称正确的是A.焦化厂B.炼铁厂C.发电厂D.水泥厂9.NA代表阿伏加德罗常数的值。下列说法正确的是A.将0.1molCO2溶于适量水,溶液中CO32-、HCO3-、H2CO3粒子总数为0.1NAB.在7.8gNa2O2与Na2S的混合物中,离子总数为0.3NAC.使0.5mol乙烯被溴的四氯化碳溶液完全吸收,断裂的共价键总数为0.5NAD.标准状况下,2.24LCl2与CH4反应完全,生成物中气体分子数目小于0.1NA10.下列实验过程可以达到实验目的的是n11.降冰片二烯类化合物是一类太阳能储能材料。降冰片二烯在紫外线照射下可以发生下列转化。下列说法错误的是A.降冰片二烯与四环烷互为同分异构体B.降冰片二烯的同分异构体可能是苯的同系物C.四环烷的一氯代物超过三种(不考虑立体异构)D.降冰片二烯分子中位于同一平面的碳原子不超过4个12.W、X、Y和Z为原子序数依次增大的四种短周期元素。常温常压下,Y的单质和氧化物均能与X的氢化物的水溶液反应生成一种相同的气体,该气体分子与CH4具有相同的空间结构。Z原子最外层的电子数是W原子的最外层电子数的2倍。下列叙述错误的是A.元素X的氢化物比其它三种元素的氢化物更稳定B.元素Y在自然界中只以化合态形式存在C.元素Z的含氧酸只有两种D.元素W、Y位于周期表中金属与非金属分界线附近13.电渗析法淡化海水装置示意图如下,电解槽中阴离子交换膜和阳离子交换膜相间排列,将电解槽分隔成多个独立的间隔室,海水充满在各个间隔室中。通电后,一个间隔室的海水被淡化,而其相邻间隔室的海水被浓缩,从而实现了淡水和浓缩海水分离。下列说法正确的是A.离子交换膜b为阳离子交换膜B.各间隔室的排出液中,①③⑤⑦为淡水C.通电时,电极l附近溶液的pH比电极2附近溶液的pH变化明显D.淡化过程中,得到的浓缩海水没有任何使用价值二、非选择题:共58分。(一)必考题:26.(15分)硼氢化钠(NaBH4)常温下能与水缓慢反应释放出氢气,能溶于异丙胺(沸点:33.5℃),n也能溶于碱性溶液,它在化工等领域具有重要的应用价值。某研究小组将NaBO2.SiO2和Na的固体混合物与氢气在500℃和4×105Pa条件下制备NaBH4。实验装置如下:回答下列问题:(1)在管式炉加热之前的操作是____。(2)C中盛装的试剂为。(3)原料中的金属钠通常保存在中,实验时取用少量金属钠需要用到的实验用品有、____、玻璃片和小刀等。(4)待反应完成后,将产物加入异丙胺溶解,过滤,得到的滤渣可作木材的防火剂,则管式炉内发生反应的化学方程式为____。(5)分离滤液中的NaBH4并回收溶剂,应选择仪器是(填标号)。(6)通过以下实验测定硼氢化钠样品的纯度。①准确称取干燥硼氢化钠样品0.50g,用NaOH溶液溶解后配制成100mL溶液;②取10.00mL样品液于锥形瓶中,加入25.00mL0.10mol/LKIO3溶液,然后加入适量KI,滴入几滴淀粉溶液,无明显现象③加入足量稀硫酸酸化,溶液成深蓝色④用0.50mol/LNa2S203标准液滴定,至终点时,消耗该标准液12.00mL则样品中NaBH4质量分数为27.(14分)亚铁氰化钾{K4[Fe(CN)6]}俗称黄血盐,常用于检验Fe3+n,也是食盐防结剂。以生产电石的副产物氰熔体[Ca(CN)2和NaCN的混合物]为原料,制备亚铁氰化钾的流程如下:回答下列问题:(1)“浸取”需控制在80℃以下进行,原因是____。(2)用硫酸亚铁晶体配制FeSO4溶液时还需加入。(3)对“滤液”处理可获得一种实验室常用干燥剂,它的化学式是。(4)“加热”使HCN气体逸出发生“反应Ⅲ”,生成亚铁氰化钾、二氧化碳和氢气,该反应化学方程式为____。(5)“反应Ⅲ”后的溶液经蒸发浓缩、冷却结晶、、__、干燥即得产品。(6)工业上,以石墨为电极,电解亚铁氰化钾溶液可以制备铁氰化钾{K3[Fe(CN)6],可用于检验Fe2+},阳极的电极反应式为。(7)设计如下实验探究牺牲阳极的阴极保护法原理。得出结论:①锌能保护铁;②____。28.(14分)乙炔可用于照明、焊接及切割金属,也是制备乙醛、醋酸、苯、合成橡胶、合成纤维等的基本原料。甲烷催化裂解是工业上制备乙炔的方法之一。回答下列问题:n(1)已知:则(2)某科研小组尝试利用固体表面催化工艺进行CH4的裂解。①若用分别表示CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程如图1所示。从吸附到解吸的过程中,能量状态最低的是(填标号),其理由是②在恒容密闭容器中充入amol甲烷,测得单位时间内在固体催化剂表面CH4的转化率[α(CH4)]与温度(to℃)的关系如图2所示,to℃后CH4的转化率突减的原因可能是____。(3)甲烷分解体系中几种气体的平衡分压(p/Pa)与温度(t/oC)的关系如图3所示。①t1℃时,向VL恒容密闭容器中充入0.12molCH4,只发生反应2CH4(g)=C2H4(g)+2H2(g),达到平衡时,测得p(C2H4)=p(CH4)。CH4的平衡转化率为____。在上述平衡状态某一时刻,改变温度至t2℃,CH4以0.01mol/(L.s)的平均速率增多,则tl____t2(填“>”、“=”或“<”)。②在图3中,t3℃时,化学反应2CH4(g)=C2H2(g)+3H2(g)的压强平衡常数Kp=Pa2。.(二)选考题:35.[化学——选修3:物质结构与性质](15分)n氢能被视为21世纪最具发展潜力的清洁能源,开发高效储氢材料是氢能利用的重要研究方向。(1)H3BNH3是一种潜在的储氢材料,其中N原子的价电子轨道表达式为。(2)制备H3BNH3的化学反应为(HB=NH)3是六元环状物质,与其互为等电子体的有机物分子式为__,CH4、H2O、CO2的键角由大到小的顺序为,B、C、N、0第一电离能由大到小的顺序为(3)C16S8是新型环烯类储氢材料,研究证明其分子呈平面结构如图1所示。①C16S8分子中C原子和S原子的杂化轨道类型分别为。②测得C16S8中碳硫键的键长介于C-S和C=S键之间,其原因可能是。(4)某种铜银合金晶体具有储氢功能,它是面心立方最密堆积结构,Cu原子位于面心,Ag原子位于顶点,H原子可进入由Cu原子和Ag原子构成的四面体空隙中。若将Cu、Ag原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图2)相似,该晶体储氢后的化学式为。(5)MgH2是金属氢化物储氢材料,其晶胞如图3所示,已知该晶体的密度为ρg/cm3,则该晶胞的体积为____cm3(用含ρ、NA的代数式表示)。36.[化学——选修5:有机化学基础](15分)化合物H是合成啶氧菌酯(农用杀菌剂)的一种中间体。由芳香化合物A为原料制备H的一种合成路线如下:回答下列问题:(I)A的化学名称为____。n(2)反应④的反应类型是____。(3)F的结构简式为。(4)H中的含氧官能团的名称是____。(5)反应②的化学方程式为。(6)芳香化合物X是H的同分异构体,能发生银镜反应、水解反应,也能与FeCl3溶液发生显色反应,X的核磁共振氢谱有四组峰,峰面积之比为6:2:1:1。写出一种符合题目要求的X的结构简式____。(7)PAA常用于纺织品和纸张的上胶,可由其单体在H2O2引发下制得。设计以乙炔、NaCN等为主要原料制备PAA的合成路线。n化学答案一、选择题:题号78910111213答案ADBDCCB二、非选择题:26.(15分)(1)装置尾部收集氢气,检验纯度 (2分)(2)浓硫酸 (2分)(3)煤油 镊子 滤纸 (3分)(4)NaBO2+2SiO2+4Na+2H2NaBH4+2Na2SiO3(3分)(5)b(2分)(6)85.5% (3分)27.(14分)(1)温度过高,促进CN-水解,生成有毒的HCN,污染环境(2分)(2)稀硫酸和铁屑 (2分)(3)CaCl2(2分) (4)2K2CO3+6HCN+Fe=K4[Fe(CN)6]+2CO2↑+H2↑+2H2O(2分)(5)过滤 洗涤 (2分)(6)[Fe(CN)6]4--e-=[Fe(CN)6]3-(2分)(7)铁被铁氰化钾氧化生成了Fe2+(2分)28.(14分)(1)+378(2分)(2)①A(2分) CH4的裂解为吸热反应,CH4分子活化需吸收能量(2分)②温度过高,催化剂活性降低(2分)(3)①66.7%(2分) > (2分)②104.7(2分)n5.[化学——选修3:物质结构与性质](15分)(1)(2分) (2)C6H6(1分)CO2>CH4>H2O (2分) N>O>C>B (2分)(3)①sp2sp3 (2分)②C16S8分子中碳硫键具有一定程度的双键性质(2分)(4)Cu3AgH8(2分)(5)(2分)36.[化学——选修5:有机化学基础](15分)(1)邻二甲苯或1,2-二甲苯(2分)(2)取代反应(1分)(3)(2分)(4)酯基 醚键 (2分)(5)(2分)(6)(2分)(7) (4分)