- 2.57 MB
- 2022-07-22 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
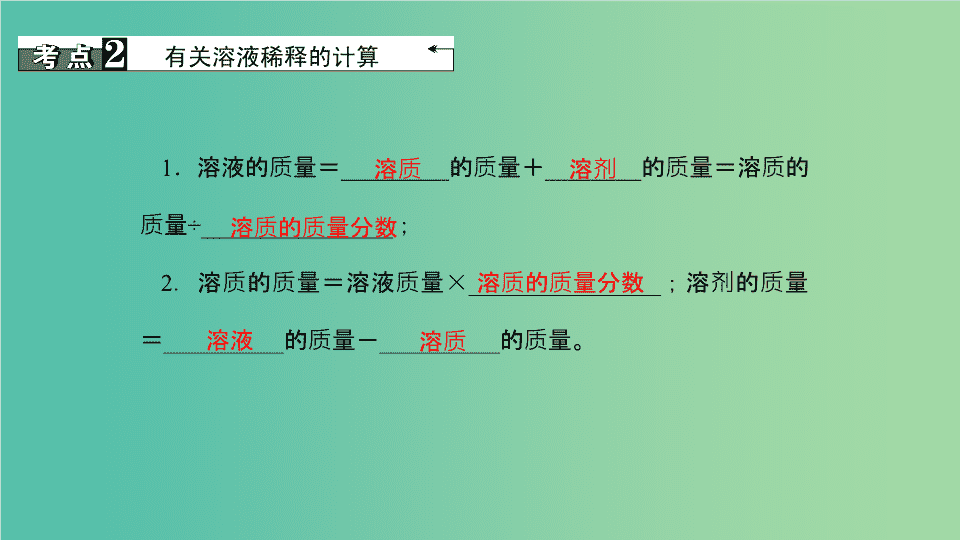
第17讲 溶液的浓度\n溶质质量分数的计算1.溶质质量分数的概念:________________________之比。2.溶质质量分数=____________________×100%。3.饱和溶液中溶质的质量分数=溶解度/(100g+溶解度)×100%溶质的质量与溶液的质量溶质质量/溶液质量\n有关溶液稀释的计算1.溶液的质量=_________的质量+________的质量=溶质的质量÷________________;2.溶质的质量=溶液质量×________________;溶剂的质量=__________的质量-__________的质量。溶质溶剂溶质的质量分数溶质的质量分数溶液溶质\n一定溶质质量分数的氯化钠溶液的配制(见实验突破)\n溶液的稀释[命题解读]溶液的稀释是化学中考常见的考点,主要以文字叙述出现在选择题或计算题中,常见的有溶液的稀释和浓缩。【例1】(2015·鄂州)取四份20℃时一定质量的饱和硝酸钾溶液,分别进行如下实验后,所得结论正确的是()A.保持温度不变,蒸发10g水后,溶液中溶质的质量分数增大B.保持温度不变,加入10g硝酸钾后,溶液中溶质的质量分数增大C.保持温度不变,蒸发10g水后,硝酸钾的溶解度增大D.降温至10℃时,硝酸钾的溶解度减小【方法指导】理解饱和溶液在温度保持不变的时候,溶质质量分数的变化情况是解决此类题的关键。D\n[对应练习]1.(2014·新乡模拟)某溶液溶质的质量分数为20%,加入50g水后变为10%,稀释后溶液中溶质的质量是()A.50gB.10gC.100gD.40g2.(2015·泉州)农业生产上通常用溶质质量分数为10%~20%的食盐溶液来选种。(1)现要配制120kg溶质质量分数为20%的食盐溶液,需要取用固体食盐______kg;(2)用60kg溶质质量分数为20%的食盐溶液,可稀释成12%的食盐溶液______kg。B24100\n根据化学方程式进行溶质质量分数的计算[命题解读]根据化学方程式进行溶质质量分数的计算是化学中考必考点,常以文字叙述或图表出现在计算题中,常见的命题点有求反应前溶液的溶质质量分数、反应后的溶液溶质质量分数、含杂质的溶液反应后的溶质质量分数计算等。【例2】(2015·十堰)某样品由氧化铜和铜组成,取10.0g该样品于烧杯中,向其中加入192.0g某浓度的硫酸,恰好完全反应,最终所得溶液质量为200.0g,(反应的化学方程式:CuO+H2SO4===CuSO4+H2O)(1)所取样品中含铜元素的质量为______g;(2)计算所得溶液中溶质的质量分数。8.4\n\n【方法指导】由最终所得溶液的质量可以求出氧化铜的质量,从而求出铜元素的质量,根据反应的化学方程式,计算出生成硫酸铜的质量,进而可计算出反应后所得溶液中溶质的质量分数。[对应练习]1.(2015·本溪)50g硝酸钙溶液与56g碳酸钾溶液混合后,恰好完全反应,过滤得到硝酸钾的不饱和溶液101g,反应的化学方程式为Ca(NO3)2+K2CO3===CaCO3↓+2KNO3。(1)生成碳酸钙沉淀的质量为____g;(2)计算反应后硝酸钾的不饱和溶液中溶质的质量分数。5\n\n一定溶质质量分数的氯化钠溶液的配制1.实验仪器:托盘天平、烧杯、玻璃棒、药匙、氯化钠、量筒(10mL、50mL)、胶头滴管。2.实验步骤:(1)用氯化钠固体配制50g溶质质量分数为6%的氯化钠溶液50g×6%=3g50g-3g=47g\n\n整个实验流程如图所示(2)用质量分数为6%的氯化钠溶液配制50g溶质质量分数为3%的氯化钠溶液(溶液稀释问题)50g×3%÷6%=25g50g-25g=25g\n\n3.溶液配制中的误差分析和原因归纳\n\n溶液的配制[命题解读]溶液的配制是中考常见的考点,主要在选择题或实验探究题,主要考查实验操作过程,实验操作误差的原因等。【例3】(2015·滨州)下图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:\n(1)用图中序号表示配制溶液的正确操作顺序____________;(2)图②中用来取用NaCl的仪器是______;(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码在标尺位置见下图,则称取的NaCl质量为________g;②⑤①④③药匙18.2(4)称量NaCl质量完毕放回砝码时,发现10g砝码有缺损,若其他操作步骤正确,则所配溶液的溶质质量分数______(填“大于”“小于”或“等于”)10%。【方法指导】熟练掌握溶液的配制过程以及配制过程操作的正误原因是解题的关键。小于\n1.(2015·佛山)下列有关溶液的说法正确的是()A.配制好6%的NaCl溶液,装瓶时不小心洒漏一部分,瓶中NaCl溶液浓度仍为6%B.长期放置后不会分层的液体一定是溶液C.KNO3饱和溶液一定比不饱和溶液溶质质量分数大D.降低饱和溶液的温度,一定有晶体析出A\n2.(2015·安阳模拟)实验室配制50g质量分数为6%的氯化钠溶液,整个配制过程如下图所示,其正确的操作顺序是()AA.③①②④⑤B.①③④②⑤C.③①④②⑤D.①④③②⑤\nD\n4.(2015·广州)配制并稀释一定质量分数的Na2SO4溶液。(1)配制50g质量分数为6%的Na2SO4溶液。①计算:需要Na2SO43.0g,水47.0g。②称量:用托盘天平称量3.0g的Na2SO4。天平调零后,分别在天平左右托盘放上质量相同的纸片,先______________________________________,然后_________________________,至托盘天平恰好平衡。③量取:用量筒量取47.0mL水。请在右图中画出47.0mL水的液面位置。④溶解。(2)稀释溶液。(由于整个配制过程中溶液很稀,其密度可近似看做1g/mL)①取1mL6%的Na2SO4溶液加水稀释至100mL,得到溶液a;②若用3.0gNa2SO4配制与溶液a浓度相同的溶液,其体积是________mL。在右盘添加3g砝码(或者移动游码至3g)向左盘中添加硫酸钠固体5000\n5.(2015·攀枝花)20℃时,将等质量的甲、乙两种固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1所示,加热到50℃时现象如图2所示,甲、乙两种物质的溶解度曲线如图3所示。请回答下列问题:(1)图1中一定是饱和溶液的是____溶液(填“甲”或“乙”);图2中乙溶液一定是________溶液(填“饱和”或“不饱和”)。(2)图3中表示乙的溶解度曲线的是______(填“M”或“N”);图2中乙溶液降温至30℃______(填“会”或“不会”)析出晶体。(3)50℃时甲的饱和溶液中溶质质量分数为__________(计算结果精确到0.1%)。甲不饱和N不会44.4%\n6.(2015·焦作模拟)马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:第1次第2次第3次第4次第5次加入稀盐酸的质量/g2020202020生成气体的总质量/g1.12.2m4.44.4试求:(1)m的值为____g;(2)12g石灰石样品中碳酸钙的质量等于____g;3.310\n(3)反应完全后最终溶液中氯化钙的质量分数?(写出计算过程,计算结果精确至0.1)