- 369.50 KB
- 2022-07-25 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
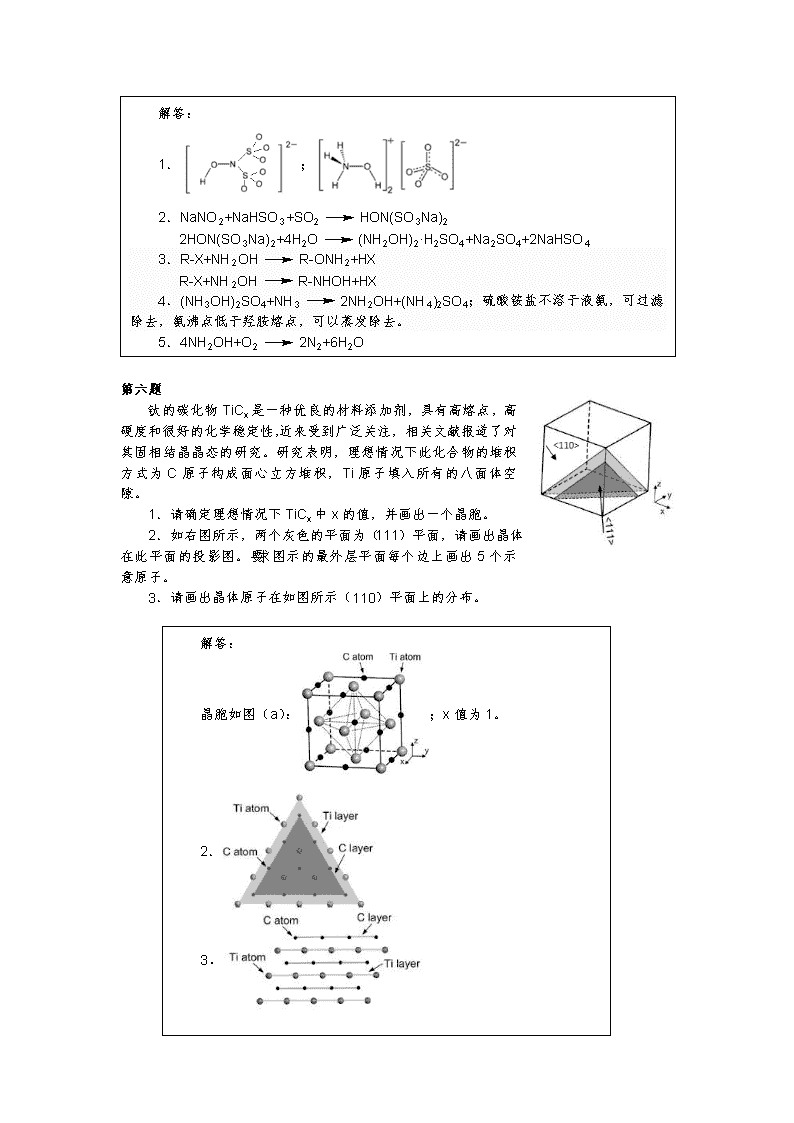
2012年全国高中化学竞赛冲刺模拟试题第一题说明为何AlF3和三卤化硼BX3均不形成双聚体的原因,比较B2H6与Al2Cl6结构上的异同点。解答:AlF3离子晶体,非共价分子。BX3,X提供2p孤对电子与B的空轨道形成π键。B2H6(3c-2e),Al2Cl6(3c-4e)均有多中心键。前者氢桥键,后者氯桥键。B2H6的3c-2e由H出1e,一个B出一个e。另一个B出空轨道形成。AlCl3的3c-4e由氯桥原子单独提供孤对电子给有空轨道的Al形成配键。第二题酸化的Co2+的溶液可在空气中保存较长时间,但加入氨水先得到红棕色的溶液,然后立即变成紫红色,分析原因。用适当的方程式表示。解答:Co2+(或Co(H2O)62+)还原性弱,不能被空气中的氧气氧化Co2++6NH3Co(NH3)62+4Co(NH3)62++O2+2H2O4Co(NH3)63++4OH-(注意:Co(CN)64-更易被氧化,除空气中的O2之外,水也能氧化它:4Co(CN)64-+O2+2H2O4Co(CN)63-+4OH-2Co(CN)64-+2H2O2Co(CN)63-+H2+2OH-其实,上述配位离子的氧化性或还原性可以从下列电极电势看出:Co(CN)63-+eCo(CN)64--0.81VCo(NH3)63++eCo(NH3)62+0.1VCo(H2O)63++eCo(H2O)62+1.84VCo(H2O)63+的氧化能力最强,Co(CN)64-的还原能力最强第三题下面列出了甲烷和甲苯的相关的键能数据和氯化反应的反应热,请解释实验数据。CH3-H+Cl-ClCH3-Cl+H-Cl键能(kJ/mol)435.1242.5351.5431ΔH=-104.9kJ/mol-CH2-H+Cl-Cl-CH2-Cl+H-Cl键能(kJ/mol)355.8242.5292.9431ΔH=-125.6kJ/mol\n解答:上面所列的氯化反应是按游离基历程进行的。由所给数据及所学知识,可以得出如下结论:(1)甲苯中甲基上的碳氢键的键能比甲烷中碳氢键的键能小,说明均裂时,甲苯中甲基上的碳氢键相对容易,这是由于生成的苯甲基自由基比甲基自由基稳定。(2)从反应的焓变可以看出,甲苯比甲烷的氯化反应容易进行。这是由于苯甲基自由基比甲基自由基稳定的结果。解答:因两者混合,反应生成绿色油状的高锰酸酐Mn2O7,它在273K(00C)以下稳定,在常温下会爆炸分解。注意:MnO2、O2和O3,这个氧化物还有强氧化性,因此不能在室温或加热的情况下混合固体KMnO4和浓H2SO4。2KMnO4+H2SO4(浓)Mn2O7+K2SO4+H2O4Mn2O78MnO2+3O2+2O3第四题在室温或加热的情况下,为什么不要把浓硫酸与高锰酸钾固体混合?第五题羟胺又称为胲,是无色,无嗅,易潮解的晶体,熔点为330C,加热容易爆炸。羟胺具有弱碱性,可以和硫酸,盐酸等强酸形成盐。羟胺及其盐是重要的有机合成中间体,在有机合成中用于合成肟,多种药物,己内酰胺等。以下是合成羟胺的一种方法:在00C时,将SO2缓慢通入亚硝酸钠和亚硫酸氢钠的混合溶液(三者摩尔比1:1:1)中,得到一种负二价阴离子A,A完全水解得到羟胺的硫酸盐溶液,所得溶液为强酸性。已知A中氮元素质量分数为7.33%,含N-O、N-S、S-O等四种类型的化学键。1.画出A以及羟胺的硫酸盐的结构式。2.写出合成羟胺的反应方程式。3.一定条件下羟胺可以与卤代烃(RX)反应生成两种不同类型的化合物,写出合成反应方程式,指出反应的类型。4.纯羟胺可以用液氨处理羟胺的硫酸盐得到,写出反应方程式,并说明如何除去杂质。5.纯羟胺在空气中受热容易爆炸,写出爆炸反应方程式。\n解答:1.;2.NaNO2+NaHSO3+SO2HON(SO3Na)22HON(SO3Na)2+4H2O(NH2OH)2·H2SO4+Na2SO4+2NaHSO43.R-X+NH2OHR-ONH2+HXR-X+NH2OHR-NHOH+HX4.(NH3OH)2SO4+NH32NH2OH+(NH4)2SO4;硫酸铵盐不溶于液氨,可过滤除去,氨沸点低于羟胺熔点,可以蒸发除去。5.4NH2OH+O22N2+6H2O第六题钛的碳化物TiCx是一种优良的材料添加剂,具有高熔点,高硬度和很好的化学稳定性,近来受到广泛关注,相关文献报道了对其固相结晶晶态的研究。研究表明,理想情况下此化合物的堆积方式为C原子构成面心立方堆积,Ti原子填入所有的八面体空隙。1.请确定理想情况下TiCx中x的值,并画出一个晶胞。2.如右图所示,两个灰色的平面为(111)平面,请画出晶体在此平面的投影图。要求图示的最外层平面每个边上画出5个示意原子。3.请画出晶体原子在如图所示(110)平面上的分布。解答:晶胞如图(a):;x值为1。2.3.\n第七题甲基异氰酸酯(MIC)是制造某些杀虫剂的中间体,是一种剧毒的物质,1984年印度Bhopal地区的泄露事件中造成了多人死亡。MIC的分子式为C2H3NO。1.MIC原子连接顺序为H3CNCO。写出其所有的路易斯结构式(三种),标出形式电荷,指出最稳定的结构。并分析分子中除H原子外的原子是否在同一直线上。2.分子式为C2H3NO的分子并非只有MIC,用路易斯结构式写出MIC的另外两个构造异构体,要求各原子形式电荷为零。3.在一定条件下MIC可以发生三聚生成环状的非极性的分子,画出其三聚体的结构。4.MIC可用如下方法制备:光气和甲胺反应得到MCC,MCC在叔胺(如二甲基苯胺)的作用下得到MIC,两步反应中均有相同的副产物。写出两步反应的方程式。解答:1.a:;b:;c:a为合理结构,N原子杂化类型为sp2,故四个原子不在一条直线上。2.(其他合理结构也可以)3.(孤对电子可以不画出)4.H3C-N=C=O+HCl5.A:;B:5.MIC可发生水解,放出大量的热。当水足量时,生成CO2和物质A(分子量为88,熔点为1060C);当MIC过量时,生成物质B(分子量为145,熔点为1250C),A、B分子中均有对称面。给出A,B的结构简式。第八题试剂A是一种无色液体,是有机合成和金属有机化学中一类重要碱试剂的中间体。A可由三甲基氯硅烷与氨气反应合成,有两种化学环境不同的氢,个数之比为18:1。1.给出合成A的化学方程式。2.A与丁基锂反应生成一种“非亲核性强碱”\nB,B在有机合成中有重要的用途,写出这种强碱的B的结构简式。为什么B是一种“非亲核性强碱”?3.B可以形成二聚体,给出二聚体的结构。4.B可以用来制备一些低配位数的配合物,如三配位的Fe(III)的配合物,分析原因。解答:1.2(CH3)3SiCl+3NH3[(CH3)3Si]2NH+2NH4Cl2.[(CH3)3Si]2NLi,两个三甲硅基体积很大,有很强的空间位阻(类似的还有LDA二异丙胺基锂)3.4.B的空间位阻很大,不利于形成高配位的化合物。5.[(CH3)3Si]3N;,三个硅原子与氮原子形成三个δ键,氮原子的孤对电子与三个硅原子的3d空轨道形成离域π键。5.三甲基氯硅烷与B反应,可以得到一种分子C,C的结构特征是具有平面正三角形的配位形式,给出C的结构简式,并通过其成键形式解释其结构特征。第九题下图为某论文中对某反应(记为反应X)的提出反应机理:A、B、C为含锰的配合物,回答如下问题:1.给出反应X的反应方程式。2.指出A在反应中的作用。3.分别指出A、B、C中锰元素的氧化态。4.下图为论文中的一幅图表,从中你能得出什么结论?\n解答:1.2.催化剂3.+2、+3、+34.随着pH的增大,反应的速率先增加后减小;当pH为7时,反应速率达到最大。第十题尼龙(英语:Nylon),又译耐纶,是一种人造聚合物、纤维、塑料,发明于1935年2月28日,发明者为美国威尔明顿杜邦公司的华莱士·卡罗瑟斯。今天,尼龙纤维是多种人造纤维的原材料,而硬的尼龙还被用在建筑业中。尼龙-6和尼龙-66是两种最重要的尼龙。1.羟胺是工业上合成尼龙-6的重要原料之一,其合成路径可以表示如下:其中A、B互为同分异构体,B含有酰胺键,请在上图中画出A、B及尼龙6的结构。2.尼龙-66可由己二酸和己二胺缩聚形成,画出其结构。3.下列分子量相同的尼龙-6和尼龙-66的关系说法正确的是A.聚合度相同B.互为同分异构体C.为同一物质D.性质差异较大4.尼龙与分子量相近的聚乙烯相比更容易结晶,试分析原因。\n解答:1.2.3.B4.尼龙可以形成分子间氢键,而聚乙烯不行,故尼龙熔沸点更高,容易结晶析出。实际上聚乙烯的熔点分布于从900C到1300C的范围,而尼龙的熔点范围为1900C-3500C。第十一题已知分子A的结构如下,回答有关问题:1.指出分子A中手性碳原子的构型。2.在DMF溶剂中,分子A与CH3SNa将发生亲核取代反应(SN2型),被CH3S-取代的CF3SO3-是一个很好的离去基团,很弱的亲核试剂,分析原因。3.若将CH3SNa换成C6H5SNa,反应的速度将会发生什么变化?解释你的结论。4.若将甲基换成叔丁基后,反应的速度将会发生什么变化?解释你的结论。解答:1.S2.三氟甲基的强吸电子诱导效应使负电荷分散。3.降低,负电荷被苯环分散,亲核能力下降。4.降低,空间位阻增大。5.生成E式烯烃5.若将反应的条件变为NaOH醇溶液,给出生成物的结构简式。第十二题以下为某实验室采用的测定金箔中金含量的方法。①准确称取经120~1300C烘过2小时的基准重铬酸钾(K2Cr2O7)15.0625g溶于少量1%H2SO4,并移入1L容量瓶中,用1%H2SO4稀释至刻度,摇匀备用。②称取15g硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]溶于500mL1%H2SO4溶液中,摇匀备用。③吸取20mL硫酸亚铁铵溶液置于250mL烧杯中,加入1%H2SO450mL,指示剂4滴,用重铬酸钾标准溶液滴定至近终点时,加入H3PO45mL,继续滴定,至从绿色变为紫红色为终点,消耗重铬酸钾标准溶液5.25mL。④将重为0.1234g的待测金箔片置于锥形瓶中,加入1:1的硝酸10mL,盖上表面皿,低温加热10分钟,小心倾倒出溶液后,加入3mL王水在水浴溶解,再加入20%KCl1mL,继续加热蒸干至较小体积,取下冷却,加入1%H2SO4\n50mL,在不断搅拌下,准确加入上述硫酸亚铁铵溶液40.00mL,放置10分钟,金全部转变为单质,加入4滴指示剂,以重铬酸钾标准溶液滴定,至近终点时加5mLH3PO4,继续滴定至溶液从绿色转变为紫红色为终点,消耗重铬酸钾5.59mL。1.在第四步操作中加入1:1的硝酸的目的是什么?反应接近终点时加入H3PO4的目的是什么?2.写出滴定反应涉及的方程式。3.计算待测金箔中金的含量。解答:1.除去铜和银,与生成的Fe3+络合,排除对终点颜色的干扰。2.Au3++3Fe2+Au+3Fe3+(写成AuCl4-配平也可以)6Fe2++Cr2O72-+14H+6Fe3++2Cr3++7H2O3.80.27%