- 1.11 MB
- 2022-07-26 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
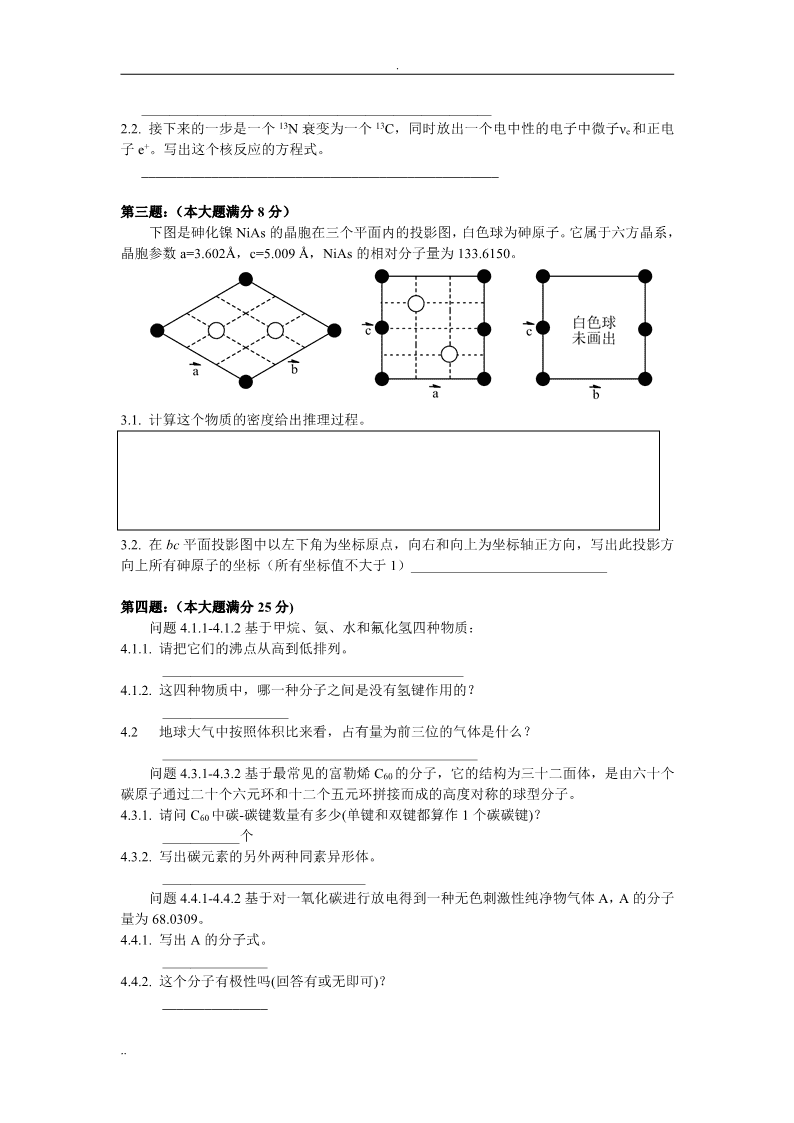
.中国化学会2013年全国高中学生化学竞赛(省级赛区)模拟试题(共计3小时)题号一二三四五六七八九十总分满分5282551410101011100得分名竞赛时间3小时。迟到超过半小时者不能进考场。开始考试后1小时内不得离场。时姓间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。试卷装订成册,不得拆散。所有解答必须写在指定的方框内,不得用铅笔填写。草稿纸在最后一页。不得持有任何其他纸张。姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。允许使用非编程计算器以及直尺等文具。校H相对原子质量He1.0084.003学LiBeBCNOFNe6.9419.01210.8112.0114.0116.0019.0020.18NaMgAlSiPSClAr22.9924.3126.9828.0930.9732.0735.4539.95KCaScTiVCrMnFeCoNiCuZnGaGeAsSeBrKr39.1040.0844.9647.8850.9452.0054.9455.8558.9358.6963.5565.3969.7272.6174.9278.9679.9083.80RbSrYZrNbMoTcRuRhPdAgCdInSnSbTeIXe场85.4787.6288.9191.2292.9195.9498.91101.1102.9106.4107.9112.4114.8118.7121.8127.6126.9131.3赛CsBaHfTaWReOsIrPtAuHgTlPbBiPoAtRn132.9137.3La-Lu178.5180.9183.9186.2190.2192.2195.1197.0200.6204.4207.2209.0[210][210][222]FrRaRfDbSgBhHsMt[223][226]Ac-Lr号名报第一题:(本大题满分5分)区在括号中写出正确的选项:治()1.1.下列哪种元素的单质不是汉弗莱∙戴维爵士首次制备的:自市A.钾B.钙C.镁D.氯省()1.2.苯是哪位科学家发现的:A.迈克尔∙法拉第B.弗里德里希∙凯库勒C.尤斯图斯∙冯∙李比希D.詹姆斯∙杜瓦()1.3.《怀疑派的化学家》是化学史上的里程碑,其作者是:A.安托万∙拉瓦锡B.约瑟夫∙普利斯特里C.罗伯特∙波义尔D.卡尔∙威廉∙舍勒区()1.4.地核的主要化学成分是:赛A.铁和镍B.硅酸盐C.碳酸盐D.氧化铁()1.5.木星大气外层的主要化学成分是:A.氦B.氢C.甲烷D.氮气第二题:(本大题满分2分)比太阳重的恒星中,将氢转化为氦的一种主要过程是贝斯-魏茨泽克循环。2.1.这个循环的第一步是一个12C和一个质子发生融合,仅产生一种氮元素的核素和一个高能光子。写出这个核反应的方程式。..\n.__________________________________________________2.2.接下来的一步是一个13N衰变为一个13C,同时放出一个电中性的电子中微子νe和正电子e+。写出这个核反应的方程式。___________________________________________________第三题:(本大题满分8分)下图是砷化镍NiAs的晶胞在三个平面内的投影图,白色球为砷原子。它属于六方晶系,晶胞参数a=3.602Å,c=5.009Å,NiAs的相对分子量为133.6150。3.1.计算这个物质的密度给出推理过程。3.2.在bc平面投影图中以左下角为坐标原点,向右和向上为坐标轴正方向,写出此投影方向上所有砷原子的坐标(所有坐标值不大于1)____________________________第四题:(本大题满分25分)问题4.1.1-4.1.2基于甲烷、氨、水和氟化氢四种物质:4.1.1.请把它们的沸点从高到低排列。___________________________________________4.1.2.这四种物质中,哪一种分子之间是没有氢键作用的?__________________4.2地球大气中按照体积比来看,占有量为前三位的气体是什么?_____________________________________________问题4.3.1-4.3.2基于最常见的富勒烯C60的分子,它的结构为三十二面体,是由六十个碳原子通过二十个六元环和十二个五元环拼接而成的高度对称的球型分子。4.3.1.请问C60中碳-碳键数量有多少(单键和双键都算作1个碳碳键)?___________个4.3.2.写出碳元素的另外两种同素异形体。_____________________________问题4.4.1-4.4.2基于对一氧化碳进行放电得到一种无色刺激性纯净物气体A,A的分子量为68.0309。4.4.1.写出A的分子式。_______________4.4.2.这个分子有极性吗(回答有或无即可)?_______________..\n.问题4.5.1-4.5.3基于铁的某种分子量介于300和400之间的羰基化合物A,A含铁量为30.7025%。4.5.1.写出A的分子式。_________________4.5.2.写出基态铁原子的电子排布式。______________________________4.5.3.画出某价电子数符合有效原子序数规则的物种Fe(CO)xCly的结构(包括了两个立体异构体,请都画出来)。已知这两个分子都是八面体型的。问题4.6.1-4.6.4基于某短周期元素X,其次外层电子数恰等于最内层电子数和最外层电子数之和。一价金属元素Y的单质和X的单质可以化合成一种2:1型(阳离子比阴离子)的含X为12.9398%的化合物A。X和氢元素可以构成一系列化合物,其中的一种化合物B含氢3.0476%。4.6.1.写出X在周期表中的位置。______________________4.6.2.写出Y的英文名称。______________________4.6.3.画出B的立体结构。4.6.4.写出B在足量氧气中点燃时发生反应的化学方程式。_______________________________________________________________问题4.7.1-4.7.2基于元素X。X的四氯化物A中X的质量分数为25.2360%。A在足量水中迅速分解产生白色沉淀B。A溶于浓盐酸,可以得到一种黄色的C溶液,往C中加入适量锌粉然后适当稀释溶液,则C会逐渐变成紫色的D溶液。4.7.1.写出A、B、C和D的化学式。A:_______________;B:______________;C:_____________;D:______________4.7.2.预测D溶液中水合金属离子物种的磁矩。__________________B.M.第五题:(本大题满分5分)仅含有一个九元环的烃A含氢11.5469%,A中仅有四种化学环境不同的氢和五种化学环境不同的碳,在戊烷溶液中A光照下反应产生包括B、C和E三种不含烷基或芳基取代基的烃。B、C、E和A是同分异构体,已知B被酸性高锰酸钾氧化成D(分子式C9H16O4);C中有八种化学环境不同的氢,双键在反应前后不发生迁移,它被二亚胺氢化得到二环[6.1.0]壬烷;E被酸性高锰酸钾氧化仅得到庚二酸和二氧化碳。画出A、B、C、D和E的结构。..\n.第六题:(本大题满分14分)近年来,人们发展了大量的方法对目标超分子进行合成,以及通过修改分子结构来实现更高的分子识别能力,金属阳离子配位则是一个重要分支。根据这些信息,结合题目要求,请回答下列问题6.1.近年来,穴醚被广泛运用在金属离子螯合的用途中,这部分是因为穴醚对金属离子往往具有更强的结合力,一般要高于其冠醚衍生物。下列路线展示了两种穴醚衍生物的合成(n=1,n=2),请预测出穴醚的结构以及中间体A的结构。6.2.第一问中我们说过穴醚的螯合特定金属阳离子的能力同比都要高于其冠醚衍生物的,另外一方面,同样是钾金属离子的螯合剂,球苑(下半图)的结合系数更是远远高于18-冠-6的(上半图)请根据各自下图中螯合前后的分子结构变化对此给出热力学角度的解释(穴醚也比冠醚具有更强的螯合能力的原因也是一样的):..\n.6.3.一种针对Li+进行螯合的球苑的合成可以参考下图的合成路线:6.3.1.写出第二步使用Fe3+的原因:6.3.2.最后一步加入盐酸可能的用途:6.3.3.在方框中写出目标产物球苑的完整结构6.4.超分子中广泛涉及的理论就是主客体化学。主客体的结合往往是一个可逆反应,其形式上的表达通式如下:其中H(Host)表示主体,G(Guest)表示客体,H·G表示结合体。下面为简化讨论首先假定[G]0=[G](即客体的初始浓度=客体的平衡浓度)。在此假定下,下式eq.2用实验可测的物理量近似地描述出了结合体平衡浓度([H·G]):其中Ka为结合反应的结合平衡常数,[H]0和[G]0分别为主体和客体的初始浓度。6.4.1.首先在[G]=[G]0假设成立的前提下,根据eq.1推导出eq.2,并定性地说明在什么情况下[G]0=[G]的假设是合理的。推导过程:[G]0=[G]假设成立条件:6.4.2.当[G]0=[G]假设不再成立的时候,eq.2不能直接使用,必须要使用下列关系由[G]0和先行得到平衡浓度[G]再进行计算:请根据eq.1推导出这个式子,并说明接下来的计算过程。推导过程:后续计算过程:..\n.第七题:(本大题满分10分)由汽车尾气排放的NO是一种大气污染物,在空气流中通入水里会发生如下反应:7.1.写出这个反应的两个电池半反应:__________________________________;________________________________7.2.事实上反应1的产物亚硝酸并不能完全解离,有人构造了如下电池来测定亚硝酸的电离常数,其中A代表的负极电极材料为含有单质Ag的二元混合物:7.2.1.写出A所代表的电极材料使得这个电池有测定电离常数的意义________________7.2.2.写出电池反应:______________________________________________7.2.3.在298oC下有电池的电极电势E=0.683V。计算HNO2的电离常数。(已知电池反应转移2mol电子的ΔθθrHm=-80.182kJ/mol,ΔrSm=-125.29J/mol*T,法拉第常数取96485C/mol)7.2.4.另一种测定HNO2电离常数的方法是以0.1000mol/LNaOH滴定20.00mL0.1000mol/L的HNO2,加入19.98mLNaOH时pH计读数为6.26,假设电化学测定的电离常数Ka值是近似准确的,计算滴定法测的Ka的相对误差Err(%),说明误差产生原因。误差原因:7.3.反应1的动力学研究给出了如下的机理(NO*3是活性中间体):7.3.1.通过计算写出下表中a的值,其中vi表示初始速率vi(-Δ[NO]/Δt)(mol/L*s)加料序号[NO](mol/L)[O2](mol/L)T=23oCT=37oC11.0*10-52.5*10-40.21*10-60.24*10-622.0*10-51.25*10-3a无需考虑7.3.2.计算反应1的活化能Ea..\n.第八题:(本大题满分10分)Suzuki反应是一种经典的有机金属反应。带有硼酸/硼酸酯的底物和带有卤素的底物在过渡金属Pd的催化下经历如下循环:8.1.填空:三个中间体的金属外围电子构型为M1_____;M2_____;M3_____。反应1可能是_________反应(填“氧化”或“还原”);反应2可能是________反应(填“氧化”或“还原”)。反应2得到的产物将会是______________。8.2.如过下面这个反应能以1:1的化学计量发生和上面催化循环类似的反应写出下面各反应的最终产物,不需要给出中间过程..\n.第九题:(本大题满分10分)含有α位卤素的酮在碱溶液中能发生各种反应,发生的反应类型和碱的强弱有关。有人将3.5eq的氯酮1和1.0eq苯甲醛在14%KOH乙醇溶液中在室温下搅拌3小时,企图获得分子式为C112H14O2的化合物A,并且预测了A的HNMR谱图(δ1.50ppm6H;6.50ppm2H;7.30ppm5H;10.0ppm1H),但是实际上主产物是A的同分异构体B,而A仅为副产物,B无法让溴水褪色。9.1.下图中完成α-氯酮1分别在40%NaOH水溶液中和20%Na2CO3水溶液中的反应:9.2.写出A和B的结构,并通过描述反应机理说明为什么无法高产率得到预测的A:..\n.9.3.写出化合物B的系统命名:_____________________________________________,并且化合物B有_________种磁.不.等.性.的氢。9.4.预测下面这个反应的产物:第十题:(本大题满分11分)盐酸赛庚啶是常用的H1受体拮抗剂,可以用于治疗支气管哮喘等过敏性疾病,它的一种制取路线如下图所示:路线中A的分子量不大于150,B具有并环结构和环外碳碳双键,化学当量的苯酐和A反应得到B的反应前后有机物的质量损失了22%。反应3经历了自由基过程。10.1.写出A至H的中间产物或反应物的化学结构..\n.10.2.对于反应2来说在不改变E和F的前提下,对底物D进行某些官能团修饰后无法得到对应反应产物。在下面的几个产物中哪些不.可.以.通过这个反应得到?10.3.氯雷他定商品名为开瑞坦,它和盐酸赛庚啶有类似的化学结构。它的结构式如下左图所示,基.于.本.题.给.出.的.合.成.路.线.,写出合成氯雷他定时所用的有机原料,催化剂除外。..