- 2.00 MB
- 2022-07-30 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
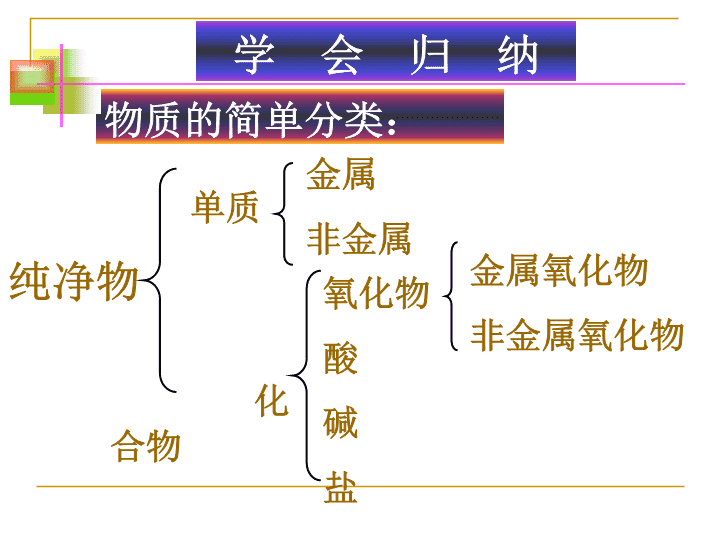
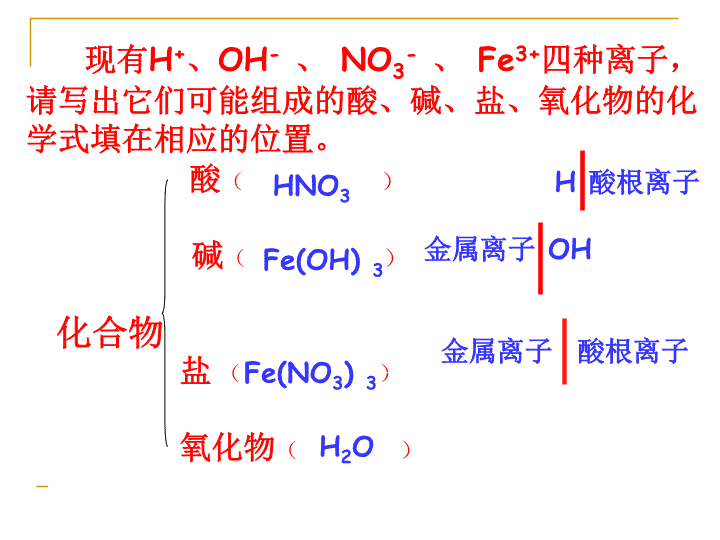
盐碱酸中考链接习题酸碱盐的总复习古柳中学隋红\n学会归纳单质化合物金属非金属氧化物酸碱盐金属氧化物非金属氧化物物质的简单分类:纯净物\n酸()碱()化合物盐()氧化物()现有H+、OH-、NO3-、Fe3+四种离子,请写出它们可能组成的酸、碱、盐、氧化物的化学式填在相应的位置。H酸根离子金属离子OH金属离子酸根离子HNO3Fe(OH)3Fe(NO3)3H2O\n盐碱酸中考链接习题酸几种常见的酸酸的通性溶液PH值盐酸硫酸\n盐碱酸中考链接习题盐酸物理性质氯化氢气体的水溶液1,无色有剌激性气味的液体2,易挥发,在空气中形成白雾3,有酸味4,工业品:黄色(含Fe3+)\n盐碱酸中考链接习题硫酸的物理性质1,无色、粘稠、油状液体2,不易挥发浓硫酸的特性:吸水性、脱水性、强氧化性做干燥剂\n4、酸+碱→盐+水3、酸+金属氧化物→盐+水5、酸+(某些)盐→新酸+新盐1、酸与指示剂作用:使紫色石蕊溶液变红,使无色酚酞溶液不变色酸2、酸+活泼金属→盐+H2酸的通性\n想一想:PH值的测定方法盐碱酸中考链接习题溶液PH值含义:表示溶液酸碱性强弱程度范围01234567891011121314碱性增强酸性增强PH=7,溶液呈中性PH<7,溶液呈酸性PH>7,溶液呈碱性放、蘸、滴、比\n盐碱酸中考链接习题碱几种常见的碱碱的通性氢氧化钠氢氧化钙\n盐碱酸中考链接习题氢氧化钠物理性质1,白色片状固体2,极易溶于水且放大量热3,易吸收水分而潮解5,俗称火碱、烧碱、苛性钠4,水溶液有涩味和滑腻感氢氧化钙物理性质1,白色粉未状固体2,微溶于水且放热水溶液叫石灰水3,俗称熟石灰,消石灰\n新盐+新碱←盐+碱碱+非金属氧化物→盐+水碱+酸→盐+水碱溶液与指示剂作用使紫色石蕊溶液变蓝使无色酚酞溶液变红碱碱的通性想想氢氧化铜具有何性质?\n盐的通性盐+金属新盐+新金属盐+酸新盐+新酸盐+碱新盐+新碱盐+盐另外两种盐\n盐碱酸中考链接习题注意:一金属的位置越靠前,它的活动性就越强二位于氢前的金属能置换出盐酸、硫酸中的氢三位于前面的金属能把位于后面的金属从它们的化合物的溶液中置换出来KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu金属活动性顺序由强逐渐减弱金属活动性顺序:在金属活动性顺序中\n\n1、下列哪几组物质在水溶液里能发生复分解反应:KNO3+NaClNa2CO3+KNO3BaCl2+Na2SO4FeCl3+NaOHZn+H2SO4(稀)CaCO3+HCl√√√小试牛刀\n鱼胆弄破后会使鱼肉粘上难溶解于水的胆汁(一种酸)而变苦,要减少这种苦味,用来洗涤的最佳物质是()。A、水B、食盐C、纯碱D、食醋C生活知多D\n成份:氢氧化铝、碘甲基蛋氨酸等3HCl+Al(OH)3==AlCl3+3H2O生活知多D用化学方程式表示斯达舒治疗胃酸过多症的原理:\n善于观察的小明看见爸爸常常用稀盐酸给铁制器皿除锈,他自己想亲自试一试。于是,他找出一颗生锈铁钉出来,放入足量稀盐酸中,然后,就跟小刚出去玩了……生活知多D可是,当他回来之后,发现铁钉不见了,你知道为什么吗?用两个化学方程式表示出来。\n为了证明长期暴露在空气中的氢氧化钠溶液已经部分变质,实验前请选用三种不同物质类别的试剂.实验方案方案一方案二方案三步骤一取样2ml于试管中取样2ml于试管中取样2ml于试管中步骤二(选用试剂并写出相关化学方程式)稀硫酸或稀盐酸氢氧化钙或氢氧化钡溶液氯化钡或硝酸钡溶液能力提升\n酿酒厂生产白酒时,常加入适量稀硫酸来控制酸度,发酵完成后进行蒸馏,即可得到白酒,盐酸的价格比硫酸低,同样能控制酸度,试说明不用盐酸的原因______________________。拓展延伸\n拓展延伸1、某厂以空气、铜、硫酸为原料制取硫酸铜2、另厂以石灰石、水、纯碱为原料制取烧碱请问你有办法吗\n1、向某无色溶液中加入稀HCl,产生气体,将气体通入澄清的石灰水中,石灰水变浑浊,证明原溶液中可能有_______离子。2、向某无色溶液中加入硝酸银溶液,出现白色沉淀,再加几滴稀硝酸,沉淀不消失,证明原溶液中有________离子。CO32-Cl-3、无色溶液中加Ba(NO3)2溶液,出现白色沉淀,再加入几滴稀硝酸,沉淀不消失,证明原溶液中含有离子;沉淀消失,则原溶液中可能含有离子。SO42-CO32-\n4.将200克溶质的质量分数是16.25%的氯化铁溶液跟200克氢氧化钠溶液混合后,恰好完全反应。试计算:(1)原氢氧化钠溶液溶质的质量分数;(2)反应后溶液中溶质的质量分数。\n本节课你有哪些收获?你还有什么疑问吗?小结\n