- 802.60 KB
- 2022-08-02 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
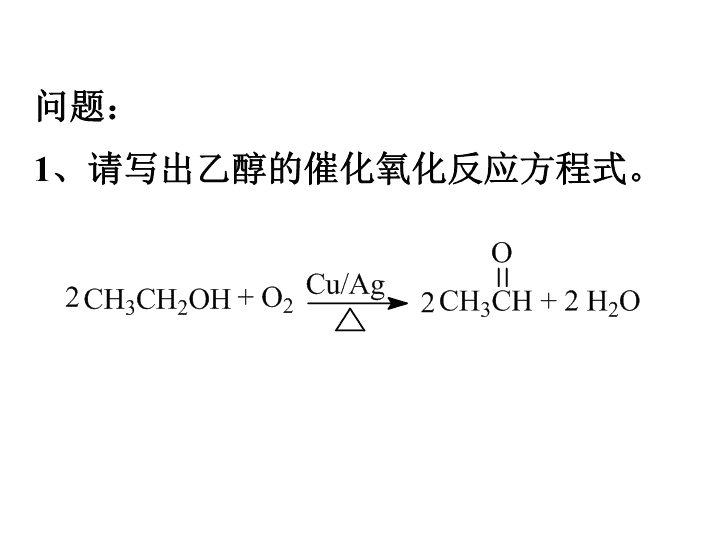
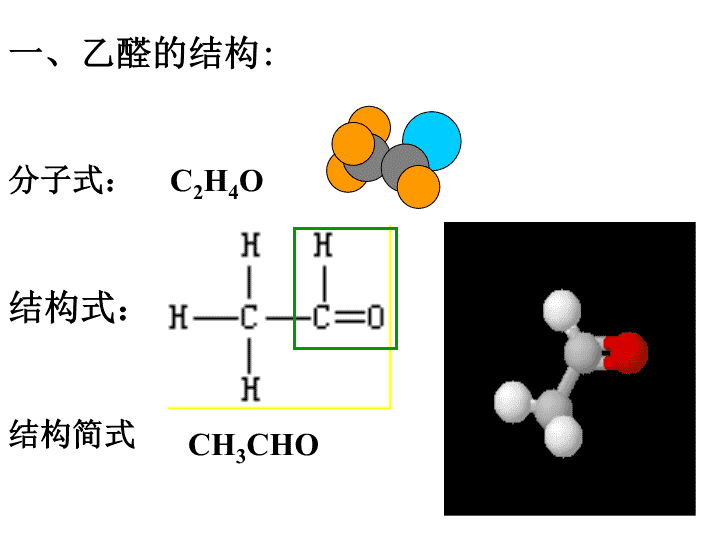
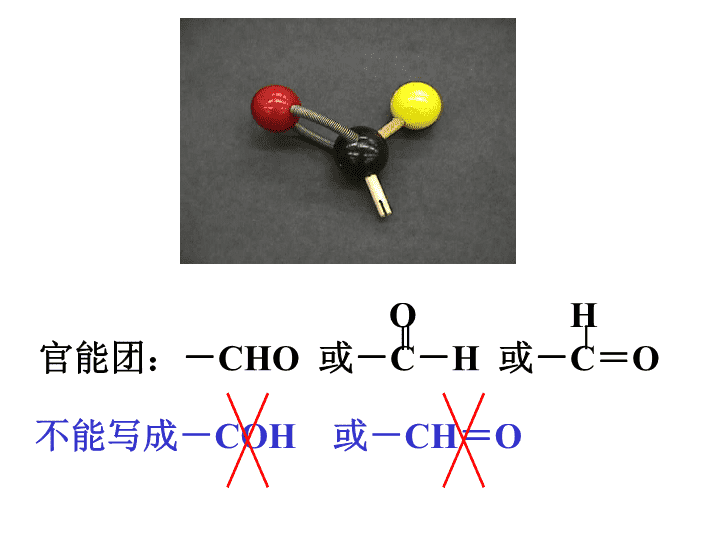
问题:1、请写出乙醇的催化氧化反应方程式。\n一、乙醛的结构:分子式:结构式:结构简式C2H4OCH3CHO\nOH官能团:-CHO或-C-H或-C=O不能写成-COH或-CH=O╳╳\n二、物理性质乙醛常温下为无色有刺激性气味的液体,密度比水小,能与水、乙醇、乙醚氯仿等互溶。问题:怎样鉴别乙醛、苯和溴苯?水\n三、乙醛的化学性质:*写出CH3CHO加成H2的反应方程式。CH3CHO+H2CH3CH2OH催化剂C=O的双键中的一个键打开。1、加成反应(碳氧双键上的加成)体现乙醛具有一定的氧化性在有机化学中加氢反应看成什么反应?(还原反应)\n通常C=O双键加成:H2C=C双键加成:H2、X2、HX、H2O得氧或去氢还原反应:加氢或失氧。氧化反应:加成规律:\n三、乙醛的化学性质:2、氧化反应O-C-HOO-C-O-H2CH3CHO+O22CH3COOH催化剂(醛基的C-H中加O成羧基)体现乙醛具有一定的还原性\n三、乙醛的化学性质:2、氧化反应(醛基的C-H中加O成羧基)在洁净的试管中加入1mL2%的AgNO3溶液中滴加2%的氨水,边滴边振荡至沉淀恰好消失。氢氧化二氨合银-银氨溶液[Ag(NH3)2]+-银氨络(合)离子Ag++NH3·H2O→AgOH↓+NH4+AgOH+2NH3·H2O→[Ag(NH3)2]++OH-+2H2O——银镜反应(1)银氨溶液的配置:[演示]银氨溶液放置会产生叠氮化银,易爆炸,应临时配置\n(三)乙醛的化学性质:2、氧化反应(醛基的C-H中加O成羧基)⑵向银氨溶液中加入0.5mL的乙醛,水浴加热CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O银镜问题:怎样除去试管中的银镜?现象:在试管内壁形成光亮的银镜稀硝酸此反应可以检验醛基存在,或定量测定醛基的数量\n(三)乙醛的化学性质:2、氧化反应(醛基的C-H中加O成羧基)CH3CHO+2[Ag(NH3)2]OHCH3COONH4+2Ag↓+3NH3+H2O银镜反应:实验注意事项:(1)试管内壁应洁净。(2)水浴加热(不能用酒精灯加热)时不能振荡试管和摇动试管。(3)配制的银氨溶液不能长时间放置,否则回生成爆炸物。(4)实验完毕要及时用稀HNO3清洗试管,处理废液-用于制镜、保温瓶胆等\n(三)乙醛的化学性质:2、氧化反应(醛基的C-H中加O成羧基)(1)新制Cu(OH)2悬浊液配置2mL10%的NaOH溶液中滴加几滴2%的CuSO4溶液。Cu2++2OH-→Cu(OH)2↓——与新制Cu(OH)2悬浊液反应碱要过量\n(三)乙醛的化学性质:2、氧化反应(醛基的C-H中加O成羧基)(2)向新制Cu(OH)2悬浊液中滴加0.5mL乙醛,煮沸CH3CHO+2Cu(OH)2CH3COOH+Cu2O↓+2H2O(砖)红色沉淀用途:1、实验室检验醛基的存在2、医院检验病人是否患有糖尿病(葡萄糖)\n问题:1、乙醛能否使酸性KMnO4溶液褪色?2、能否使溴水褪色?酸性KMnO4,溴水的氧化性比氧气的氧化性要强,所以酸性KMnO4,溴水都会退色。以上两个反应:1、可用于鉴定-CHO的存在。2、都能被弱氧化剂氧化,乙醛具有较强还原性,做还原剂。\n能使KMnO4,溴水都褪色。②银镜反应(生成羧酸盐)③与氢氧化铜生成红色沉淀的反应(生成羧酸)乙醛的性质小结1、加成反应(与H2)2、氧化反应①被空气中的氧气氧化(生成羧酸)写出乙醛燃烧的化学方程式\n乙醛还原(加H)乙醇氧化(失H)氧化(加O)乙酸写出下列方程式:乙酸乙酯\n四、乙醛的工业制法1、乙醇的催化氧化法2、乙烯氧化法2CH2=CH2+O22CH3CHO催化剂2CH3CH2-OH+O22CH3CHO催化剂3、乙炔水化法:CH≡CH+H2OCH3CHO催化剂\n四、醛类1、定义:2、命名:OR-C-H3、饱和一元醛的结构通式:4、化学性质与乙醛相似分子里由烃基和醛基相连而构成的化合物根据醛的组成中碳原子的数目称某烷分子通式:CnH2nO写出乙二醛与O2的反应方程式\n练习1、对乙醛叙述正确的是A、看成-CH3和-CHO直接相连的化合物B、所有原子都在一个平面上C、具有还原性D、工业上大量用于制乙醇2、下列用于检验有机物中醛基的试剂是:A、硝酸银溶液B、新制的氢氧化铜C、银氨溶液D、氢氧化钠溶液3、做过银镜反应的试管最好用下面哪种试剂洗涤:A、稀硝酸并微热B、乙醛溶液C、烧碱溶液D、30%的氨水\n5、下列有机物在反应中被氧化的是:A、CH2=CH2转化成CH3CH3B、CH3CH2OH转化成CH3CHOC、CH3CHO转化成CH3CH2OHD、CH3CHO转化成CH3COOH6、在2HCHO+NaOH(浓)HCOONa+CH3OH反应中,关于HCHO的叙述正确的是:A、只被氧化B、只被还原C、既未被氧化,又未被还原D、既被氧化又被还原7、写出乙醛跟:(1)银氨溶液(2)新制氢氧化铜反应的化学方程式。4、乙醛与氢气在一定条件下反应生成乙醇,此反应属于:A、还原反应B、氧化反应C、加成反应D、消去反应\nOCH3CCHCH2CH2CCHCHCH3CH34、已知:柠檬醛的结构为:请设计实验证明存在碳碳双键?先加足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化。然后再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色\n五:甲醛(蚁醛)1、结构2、性质:与乙醛相似HCOH平面结构\n甲醛又称蚁醛,英文名称是Formaldehyde,化学式为CH2O,分子质量为30.03,密度为1.067,熔点-92℃,沸点-19.5℃,爆炸界限是7-73%。易溶于水和乙醇,40%水溶液俗称福尔马林,是具有刺激性气味的无色液体。具有防腐作用,通常被用来固定病理标本及动物标本等。\n不同点:1、常温下甲醛为无色有刺激性气味的气体2、甲醛中有2个活泼氢可被氧化HCHO+H2CH3OH催化剂HCHO+2[Ag(NH3)2]OHHCOONH4+2Ag↓+3NH3+H2OHCHO+2Cu(OH)22HCOOH+Cu2O↓+2H2O\n合成酚醛树脂——缩聚反应\n3、应用:(1)甲醛的水溶液叫福尔马林,具有防腐和杀菌能力。(2)能合成酚醛树脂(3)在农业上制缓效肥料(4)制氯霉素、香料、染料的原料。\n如何去除甲醛:一、采用没有或浓度低的含有甲醛的建材、油漆。如果建材中含有甲醛,则让其表面装饰的不含甲醛的油漆、涂料,充分固化,形成抑制甲醛散发的稳定层后才可入住。二、植物消除法(吊兰、芦荟)吊兰、芦荟、虎尾兰能大量吸收室内甲醛等污染物质,消除并防止室内空气污染\n三、吸附法(活性炭)吸附是一种固体表面现象。它是利用多孔性固体吸附剂处理气态污染物。使其中的一种或几种组分,在分子引力或化学键力的作用下,被吸附在固体吸附剂表面,从而达到分离的目的。\n四、去除甲醛危害的最佳方法就是新装修的房子要保持长时间的通风,有可能的话提高房间的室内温度,让甲醛加快挥发。一般来说新装修好的房子不要马上搬进去住,最好能把所有的窗户打开放置数月。\n甲醛主要来自复合木材中的酚醛树脂,脲醛树脂,内墙涂料,装修布,电器绝缘材料,黏合剂等。(1)室内装修生活中甲醛的来源\n(2)水产品用甲醛处理过的海产品如海参、鱿鱼、海蛰等,外观好看,食用要谨慎。在碱性中甲醛与海产品中的蛋白质反应,形成缩醛化合物,使水浸泡过的海参、鱿鱼、海蛰变得挺直。但进入人体胃中,在酸性环境下又会放出甲醛,放出的甲醛可能会与人体蛋白质中的氨基酸重新结合,而危害人的健康。\n(3)衣物整理剂甲醛是纺织品上的有害残留物质之一。通过缩合作用,甲醛分子把两分子纤维连接起来,从而达到防缩水,防皱的目的。常用于以纤维素纤维为主的织物和以蛋白质为主的蚕丝织物的防缩防皱。由于含甲醛的纺织品做成服装后,在人们穿着过程中会逐渐释放出游离甲醛,通过人体呼吸及皮肤接触对呼吸道粘膜和皮肤产生强烈刺激,引发呼吸道炎症和皮肤炎。\n另外,在生产过程中为了保持印花,染色的耐久性或为了改善手感,也需要在助剂中添加甲醛。目前用甲醛印染助剂比较多的是纯棉纺织品,因为纯棉纺织品比较容易皱,使用含甲醛的助剂能提高棉布的硬挺度。对于丝织品其作用原理同海产品。\n因此,在成衣上,微量的甲醛是不可避免的。一是来自整理剂中的游离甲醛,二是整理剂分解。如衣物与汗接触,甲醛就会被释放出来。随着人们环保意识的加强,国际上对纺织品中的甲醛进行了严格的限制。纺织品和服装中的甲醛问题已受到世界各国的普遍重视,现在日本、美国、欧洲以及有关国际组织的标准都对甲醛含量做出了明确的限制和规定。\n(4)啤酒的甲醛啤酒中为什么会有甲醛呢?这是由于啤酒是一种不稳定的胶体溶液,在生产和贮存过程中很容易产生浑浊沉淀现象而影响产品外观。如果在啤酒生产的糖化阶段添加微量甲醛,不仅可以抑制啤酒麦芽中多酚物质的氧化和溶出,使啤酒澄清透亮,还能大大缩短出酒的时间。国内外传统的啤酒酿造工艺都是在啤酒加工生产中加入微量甲醛。但啤酒甲醛含量应符合安全标准。\n实验材料:高锰酸钾固体,酸式滴定管,碱式滴定管,
针筒,烧杯,玻璃棒,1L的容量瓶,电光天平(精确到0.0001g),三角锥瓶,药匙,
硫代硫酸钠固体,实验方程式:4KMnO4+5HCHO+6H2SO4→
4MnSO4+5CO2↑+2K2SO4+11H2O8KMnO4+5Na2S2O3+7H2SO4→
5Na2SO4+8MnSO4+7H20+4K2SO4\n实验方法:1、用塑料瓶装满水,旋好瓶塞,走进已装潢好、时间不等的房间内。待走进房间后,打开瓶塞,到出水,使塑料瓶内充满该房间内的气体,再旋好瓶塞,这样已收集好一瓶气体。用这种方法再收集2瓶气体。\n2、用针管直接刺破塑料瓶的塑料盖,然后往里面注水,并不停地摇晃塑料瓶,使甲醛充分溶于水中,当注水至2∕3处时,(因为继续注水会使瓶内压强过大,从而不易继续注水),然后停止注水,反复振荡塑料瓶,使甲醛充分溶于水。\n3、用电子天平称量0.2000g高锰酸钾固体溶于烧杯中,再由1L的容量瓶内配成c=0.00013mol/L的高锰酸钾溶液1L.4、用电子天平称量0.2000g硫代硫酸钠固体溶于烧杯中,再由1L的容量瓶内配成c=0.00013mol/L的硫代硫酸钠溶液1L\n5、取25mL的高锰酸钾溶液装入酸式滴定管中,将配好的硫代硫酸钠溶液装入碱式滴定管中,将配好的甲醛溶液装入三角锥瓶中,用高锰酸钾溶液滴定甲醛溶液(含稀硫酸),当溶液变成微红后,再用硫代硫酸钠溶液反滴高锰酸钾溶液,当溶液红色褪去时,实验停止。\n实验数据:实验V高锰酸钾(mL)V硫代硫酸钠(mL)V甲醛(L)参加反应的甲醛的物质的量(molL)超标倍数11.000.5053.16×10-723.721.000.6056.32×10-84.731.000.6251.26×10-80.94\n\n实验结果:通过实验我们得到,实验一:装潢完4月,测出甲醛浓度为标准的0.94倍;实验二:装潢完35天,测出甲醛浓度为标准的4.7倍;实验三:装潢完3天,测出甲醛浓度为标准的23.7倍;由实验可知:装潢完,搬入新家时间最好约为3—4个月。但建议半年后入住较好。