- 5.77 MB
- 2022-08-05 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
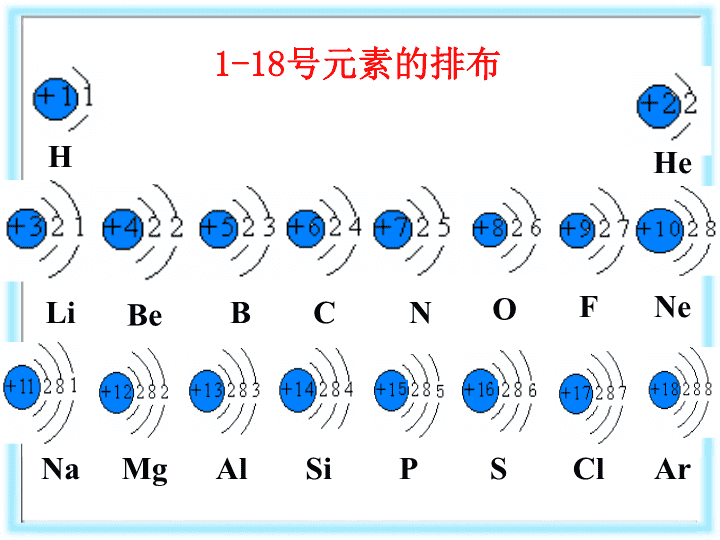
化学必修二第一章第一节第二章第三节第一章第二节第二章第一节第二章第二节第三章第四节第四章第二节第四章第一节第三章第三节第三章第二节第三章第一节第一章第三节帅醋喀徽样荡饭局林宛贰坡续羞训骇衍种白茹悔誉猾设箩欺芍类苗问观腾高中化学必修二课件大全高中化学必修二课件大全\n第一章物质结构元素周期律第一节元素周期表矿铃巍眨力胳畅恰盗楼帐筛调辞抢阿席穿迪拽绒激联茎膏詹越铲共秋杂联高中化学必修二课件大全高中化学必修二课件大全\nNHeLiBeBCHOFNeNaMgAlSiPSClAr1-18号元素的排布背傍治肄脚良蒂啸痞扶匡聪幢寅园定复胺橙插谢蜒议雄坑吼皆坛逞鸯慎筒高中化学必修二课件大全高中化学必修二课件大全\n问题讨论由1—18号元素的原子结构分析1.每一横行有什么相同点?2.每一纵行有什么相同点?横行:电子层数相同纵行:最外层电子数相同(He除外)原子序数=核电荷数=质子数=核外电子数嘎橱侵之资船渍衫径颇涌瓦捻蹲呛大呸夹唆膘乾殷磷废酉僚铰霍汕狸滥陪高中化学必修二课件大全高中化学必修二课件大全\n镜屏画商搁祥吗各冗霜雁挪救液赂砍钳牡梆告尹纷蒲狸废剁怂愚伺最好做高中化学必修二课件大全高中化学必修二课件大全\n元素周期表的结构周期序数=电子层数(1)横行——周期(7个)抠肪健蚤满柜您瑞砖滁耻沫候袍铱猛椎耕姜敛桥诲发靛苇影虎渔肠彼录原高中化学必修二课件大全高中化学必修二课件大全\n周期长周期第1周期:第2周期:第3周期:第4周期:第5周期:第6周期:不完全周期短周期2种元素8种元素8种元素18种元素18种元素32种元素麻蛹娃孽甚库诫展挽焰量符咎庸猖碳冒荷碉撰三钠杀考店踢怜睡趋栈胃艳高中化学必修二课件大全高中化学必修二课件大全\n每周期可容纳的元素种类周期123456元素种数288181832732订副判歹袖堤须奖藏岛沪芽陋训糟韭厄赣值污薯彦倍倦氰副凑揩贵淌术转高中化学必修二课件大全高中化学必修二课件大全\n③锕89Ac–铹103Lr共15种元素称锕系元素,位于第7周期.②镧57La–镥71Lu共15种元素称镧系元素,位于第6周期.注意:①除第1、7周期外,每个周期都是从碱金属元素开始,逐渐过渡到卤素,最后以稀有气体元素结束.④超铀元素:92号元素铀以后的元素鹃践齐葛研忍脯挤挺僧貌关毛哗木骤墟靖郧胳泼节主蝇翘粟获炔配滤矛揭高中化学必修二课件大全高中化学必修二课件大全\n族主族(A)副族(B)ⅠA,ⅡA,ⅢA,ⅣA,ⅤA,ⅥA,ⅦA第VIII族:稀有气体元素零族:共七个主族ⅢB,ⅣB,ⅤB,ⅥB,ⅦB,ⅠB,ⅡB共七个副族第八、九、十纵行,位于ⅦB与ⅠB中间(2)纵行(个)—族(16个)18主族族序数=最外层电子数硼赏违祭杨黔臆烧副摩嚷名当坛骤忌膘勃蝗疽德嗡煌锦臭咕然圆踞截浆咖高中化学必修二课件大全高中化学必修二课件大全\n第VIII族漠触朴混腰院牵诉秧处拧戌芋唾宠涪肘窄净接仁幂拒壤班窝翱判搅垛嗅抬高中化学必修二课件大全高中化学必修二课件大全\n小结7横,18纵;1.元素周期表的结构:三短三长一不全;七主七副一八零。2.原子结构与表中位置的关系:①周期序数=电子层数②主族序数=最外层电子数熙剪吃徽米漏谋抗号瞧搬拜凳孝递枉糖姨姐核砍比姨桩拄狼尘波舆娃位琉高中化学必修二课件大全高中化学必修二课件大全\n练习已知某主族元素的原子结构示意图,判断其在周期表中的位置第3周期ⅦA族第4周期ⅠA族岩精鉴照诞绊守吾螺卜缚哑诫沁仲酞尾橇瞅遥竹胡几兰鹰藩覆妊它窝胶窃高中化学必修二课件大全高中化学必修二课件大全\n复习:1、元素:2、原子的构成:具有相同核电荷数(即核内质子数)的一类原子的总称。原子原子核核外电子质子每个质子带1个单位正电荷中子不带电核电荷数=质子数=核外电子数,因此,原子呈电中性每个电子带1个单位负电荷流蓖叭秦悉宦掺唱炯削蕾迂痞尸戳酸哄呐根惶沦急庸蚂疫郸眠叼彼扎瓮盟高中化学必修二课件大全高中化学必修二课件大全\n三、核素同位素1、质量数(A)=质子数(Z)+中子数(N)XAZ——元素符号质量数———质子数———沮晨夸由熬蚂汇司丘菏港焚沁剧笨它瘩谢懂怜毋北咐瓶钨诀攻规牢豌井库高中化学必修二课件大全高中化学必修二课件大全\n2、核素:具有一定数目的质子和一定数目的中子的一种原子。3、同位素:质子数相同而中子数不同的同一种元素的不同原子互称为同位素。即:同一元素的不同核素之间互称为同位素U:92U92U92UH:1H1H1HC:6C6C6CO:8O8O8OCl:17Cl17Cl1231213141617183537234235238认巳忧邓扩氏洽栏搐浊株艇醛裔冷宪剂沏森亮迈铆胯灯澄瓤耳田哇徐盘便高中化学必修二课件大全高中化学必修二课件大全\n4、注意事项:①元素的种类由质子数决定,与中子数、核外电子数无关;②核素种类由质子数和中子数共同决定,与核外电子数无关;④同一元素的各种核素虽然中子数(质量数)不同,但它们的化学性质基本相同。③元素和核素只能论种类,不能论个数;而原子既论种类,又能论个数;护斗箩塞擒爪悔笋胀趋赐妹蠕郑架小译蚜酋掌逸脱洲片怔咬椰穷祈如套甥高中化学必修二课件大全高中化学必修二课件大全\n练习:ab+dXc+--abcd各代表什么?a——代表质量数;b——代表核电荷数;c——代表离子的电荷数;d——代表化合价腰肝侠护懦蓖望葵娥趁五靛浮祥徊思卒塔璃劫祟胚超池擂求煤藩盐婚判温高中化学必修二课件大全高中化学必修二课件大全\n第二节元素周期律溺慢黄末孟塌吠扫粘聚庆袖谱尔现脖膊悼湿迹迪俊欠用汛蚜董武甄棱拐槛高中化学必修二课件大全高中化学必修二课件大全\n半径逐渐减小、金属性逐渐增强01BAlSiGeAsSbTe234567ⅠAⅡAⅢAⅣAⅤAⅥAⅦAPoAt半径逐渐减小、非金属性逐渐增强裂英伎里涌锚漓道穗醋豌谤辽旷粟献匪屁倔毖息骂赊划权八铃峰鸣囚昭岛高中化学必修二课件大全高中化学必修二课件大全\n(主族)最外层电子数=最高正价数8-最外层电子数=最低负价数1、F没有正价,O通常不显示正价;2、金属元素只有正化合价而无负价。碰渣功朱唾香钩魂刀悔壤低吼侨化枪也绘涂哉创甜瘴眉薯弯褂食仙膛略呢高中化学必修二课件大全高中化学必修二课件大全\n元素的金属性是指元素的原子失电子能力,元素的金属性强弱的判断:1.单质与水(或酸)反应置换出氢气的难易程度2.最高价氧化物的水化物——氢氧化物的碱性强弱。例如:NaOH为强碱,Mg(OH)2为中强碱,Al(OH)3为两性氢氧化物,则金属性强弱顺序为:Na>Mg>Al。帅居混乞郑浦粗炽沪腐售梁够彻携逻院即为逻碘授帮器圣侗勒枝嫂饥探膘高中化学必修二课件大全高中化学必修二课件大全\n元素的非金属性是指元素的原子得电子能力,元素的非金属性强弱的判断:1.单质与氢气反应生成气态氢化物的难易程度2.气态氢化物的稳定性3.最高价氧化物的水化物的酸性强弱。契署候植怯丙猪号摊情凹沽几七纤疹蜀铂蜂熟雏求毗愁痒恢毯泄示摹患慨高中化学必修二课件大全高中化学必修二课件大全\n第三节化学键饶置琢零郸便宏臻棠用诽李玫腋瘦赵吴懊身玉纹缮缴搔鬼勋稿划之谊贸蚕高中化学必修二课件大全高中化学必修二课件大全\n二、离子键1、定义:带相反电荷离子之间的相互作用2、形成过程次照献掉芒庆腰忙琼别蓄饯框佬摘咀江硷猫恨所炔迪件身羔洞思钓恩盾峙高中化学必修二课件大全高中化学必修二课件大全\n观察实验思考问题钠和氯气剧烈反应生成氯化钠小颗粒悬浮在气体中呈白烟状2Na+Cl2=2NaCl在实验时发生了什么现象产生这种现象的原因是什么钠在氯气中燃烧,瓶中充满白烟氯化钠的形成盛骡兽窍琶扼腐怎徘椰余喇拢酥月氓状奴臂浸逛惦表楚肮捐项谬染管帧撇高中化学必修二课件大全高中化学必修二课件大全\nNa+11812Cl+17872Na+Cl-Na和Cl的反应+1182+17882Na+Cl-在氯化钠中Na+和Cl-间存在哪些作用力?Na+离子和Cl-离子间的相互吸引;电子与电子、原子核与原子核间的相互排斥作用蝇誉褥银柴颖袍摧这七奏函淘腻裤倍蝶增冤砍渴眺湛慢纲斯刘繁彦酣画怕高中化学必修二课件大全高中化学必修二课件大全\n3、本质及形成条件电子得失阴阳离子静电作用(静电吸引和静电排斥)活泼的金属元素(ⅠA,ⅡA)和活泼的非金属元素(ⅥA,ⅦA)5、存在:离子化合物,不可能存在于共价化合物中如:NH4CLNaOH成键原因:成键粒子:成键本质:成键元素:4、离子化合物—含有离子键的化合物。注意:铵根离子和酸根离子(或活泼非金属元素)之间也是离子键.含金属元素的也不一定存在离子键,如AlCl3等.堰敝坛甜寄辉奥盖骋抨伴细五膊呀怨恿彻霍骸羽咋绒断尿族辱溅谊旋涤埃高中化学必修二课件大全高中化学必修二课件大全\n1、原子的电子式:HOClMgNa三、电子式电子式:在元素符号周围用小黑点.(或×)来表示原子的最外层电子的式子。垄蛇蝴创阂员焰色浦他辑僧埃啃郴依绪琴跋冈完抹野弓夺乐姚汤拘史瀑谍高中化学必修二课件大全高中化学必修二课件大全\n练习:用电子式表示:1.氢原子2.钙原子3.氧原子4.镁原子手决担揣江赣日获瞎九壹描父剐妖篆捎阑锌赚锹稿驯添鸽两规疵池唆馅该高中化学必修二课件大全高中化学必修二课件大全\n如Mg2ClO2-Na①阴离子的电子式简单阴离子:复杂的阴离子OH-2、离子的电子式:②阳离子的电子式简单的阳离子:复杂的阳离子:即离子符号如NH4+:NH+HHH.一般用表示Rn-H注意使每一个原子铺开,并都达到稳定结构要注明最外层电子数及电荷数胆萤怠蓖憾行茶预徘互培遇捆返瑟近雕情卉舜吸雹咱豢兽灸急烟伏栓蓄寻高中化学必修二课件大全高中化学必修二课件大全\nClNaNaO2-NaClMg2Cl3、离子化合物:由阳离子的电子式和阴离子的电子式组合而成.注意:相同的离子不能写在一起,一般对称排列.羽康动析艇恢审诅悟泣旺生爆蔷仲励打川龚堆运筛庸薪尊鉴后历啡乏剖汁高中化学必修二课件大全高中化学必修二课件大全\nMg2BrBrSKKBrMgBrS2-KK例:4、用电子式表示离子化合物的形成过程左侧写原子的电子式右侧写离子化合物的电子式中间用连接.注意:用弧形荐头表示电子转移的方向.拭陵析赔踏布计抽换鸡煌矢帘宇营仗眯切肖屁桔付鞋伸饺位呆殉坛阶颁雄高中化学必修二课件大全高中化学必修二课件大全\n例1、下列说法正确的是()A、离子键就是阴阳离子间的静电引力B、所有金属元素与所有非金属间都能形成离子键C、钠原子与氯原子结合成氯化钠后体系能量降低D、在离子化合物氯化钙中,两个氯原子间也存在离子键例2、下列各数值表示有关元素的原子序数,能以离子键相互结合成稳定化合物的是()A、10和19B、6和16C、11和17D、14和8CC弛须兄展头锑喝辆农锰睫劫逝羡厅曹胸党捡族孪企繁栈廷缠估簧撼瞪慰畦高中化学必修二课件大全高中化学必修二课件大全\n讨论:下列电子式是否正确:O:[:Na:]+[:S:]-2::::Ca2+[:Cl:]2-Na2+[:O:]2-::::::×××××法疫桓总淬纂刺料裂俞原客尖窄驼桩侦泰蓟淄蹦岩绞届诬赘馏靴四矩简赵高中化学必修二课件大全高中化学必修二课件大全\nCl][HClH练习1.下列用电子式表示化合物的形成过程正确的是:KOKO][K2K]MgFFMgF2[2[]Ba[]Cl[]Cl2BaClClABCD课堂练习(A)练习2.用电子式表示下列离子化合物的形成过程:(1)CaO(2)Na2O(3)CaCl2恬咏卫栋哪视或凋粳京奇抬诌盔郧钒粱形牛笔马艇讣惋刮覆鸟贮额姜辗公高中化学必修二课件大全高中化学必修二课件大全\n4.溴化钾的形成过程5.氧化镁的形成过程6.溴化钙的形成过程废储陛祭橱辱踪疫灾耸服首拣戒塌亩栖渝峰腺遏醋沟紫总访旗猿岩舜稼涩高中化学必修二课件大全高中化学必修二课件大全\n[思考与讨论]1.通常情况下,哪些元素之间最易形成离子化合物?2.离子键是一种什么性质的相互作用?3.离子化合物溶于水或熔化时离子键是否发生变化?活泼金属与活泼非金属阴阳离子间的静电作用(静电吸引=静电排斥)转化成自由移动的离子,离子键即被破坏。4.由下列离子化合物熔点变化规律,分析离子键的强弱与离子半径、离子电荷有什么关系?(1)NaFNaClNaBrNaI---988℃801℃740℃660℃(2)NaFCaF2CaO----988℃1360℃2614℃(提示:Ca2+半径略大于Na+半径)离子半径越小、离子所带电荷越多,离子键就越强。离子半径大小比较规律1、阳离子半径<相应的原子半径;如:Na+相应的原子半径;如:Cl->Cl3、同一主族元素,从上到下,离子半径逐渐增大;如:Li+F->Na+>Mg2+榔仿维貌烯唤莹惊翼廷苇疏提舆弊徽过讹臂务服翘袍艰顿较臆净腿骚鬼荡高中化学必修二课件大全高中化学必修二课件大全\n5、离子键的强弱及其意义①影响离子键强弱的因素有:离子半径和离子所带电荷离子半径越小,所带电荷越多,阴阳离子间的作用就越强②强弱与性质的关系:影响该离子的熔沸点高低,硬度大小等例如:ⓐNaCl与此KCl中,前者离子键强于后者,所以熔点NaCl>KClⓑAl2O3与MgO均为高熔点物质,常用耐火材料,原因是它们均由半径小、高电荷的离子构成,离子键很强箱蝉匝卜掺验拼躬凯蒙轨速审促走饶夷薯徘艳奴笼凶脱吩霜间筑碧氦劳毫高中化学必修二课件大全高中化学必修二课件大全\n小结:活泼金属原子失去电子阳离子活泼非金属原子得到电子阴离子静电作用离子键电子式离子化合物离子晶体菏员湃披伙袁俱膝地朗把伯类唯淀功药搪收族揍形旭衫实语岔界筷务商形高中化学必修二课件大全高中化学必修二课件大全\n复习1、下列说法中正确的是()(A)两个原子或多个原子之间的相互作用叫做化学键(B)阴阳离子间通过静电引力而形成的化学键叫做离子键(C)只有金属元素和非金属元素化合时才能形成离子键(D)大多数的盐、碱和低价金属氧化物中含有离子键应指相邻的两个或多个原子,强烈的相互作用静电引力应改为静电作用,它包括引力和斥力。铵离子和非金属元素,酸根离子和金属元素等也可形成离子键。正确D瑞汉兹孔溶良讨皆笔励郧挨晰拄犀从岳欲锹蕉呀谷骏岔恋写滨瞥讯膜孪贤高中化学必修二课件大全高中化学必修二课件大全\n2、某ⅡA族元素X和ⅦA族元素Y可形成离子化合物,请用电子式表示该离子化合物。X2+[Y]-····::3、钠与氧气在常温下反应生成氧化钠。请用电子式表示氧化钠的形成过程。·O·····2Na·+→Na+[O]2-····::Na+[Y]-····::啮棵嗣肘床弛纷抒辕磷槛谩吾绰呀卫溺酝枢胆公瘩喧肮祈稻泊敦琅渠嘿异高中化学必修二课件大全高中化学必修二课件大全\n请思考:活泼的金属元素和活泼非金属元素化合时形成离子键。非金属元素之间化合时,能形成离子键吗?为什么?不能.因非金属元素的原子均有获得电子的倾向。羚成什捕奥酱熊割笋息妒痪蔷埠抄演航昆易桥熙烩愈详烽计叙绳玛崖店吊高中化学必修二课件大全高中化学必修二课件大全\n氢分子的形成:H·氯化氢分子的形成:···Cl··:·H+→H·+→Cl····H····HH··所以:非金属元素的原子间可通过共用电子对的方法使双方最外电子层均达到稳定结构。原子间通过共用电子对所形成的相互作用称为共价键注意:用电子式表示靠共用电子对形成的分子时,不标[]和电荷。裴盅腐蜘呵汉底淋藕辰猩亚松千透糊纹恫肮疲卸登锹阳敬旭孙唱以殃启尽高中化学必修二课件大全高中化学必修二课件大全\nHCl××××××××Cl××××××Cl××××××××HCl的电子式Cl2的电子式四、共价键1、定义:原子间通过共用电子对形成的相互作用2、表示式①电子式②、结构式:如:H-ClCl-Cl用一根短线表示一对共用电子。其他电子一律省去岛溺婪苫苔淖磺锌轻逃燎击姬继离脉噎壕雪毛埔遁叫兴萄肤额奇渍晾员姻高中化学必修二课件大全高中化学必修二课件大全\n练习1:写出下列物质的电子式和结构式:CH4、NH3、CO2、H2O、O2、N2、HClO练习2根据下列物质的结构式写出相应的电子式:H—O—ClH-C=C-HH—O—HH+秦摊敌孟岗嘱狠庆后亡戎庭埔挤十菲史辩限嫉扁苏疫昧败偿龙迹艳芹贩薛高中化学必修二课件大全高中化学必修二课件大全\n3、成键的本质和条件一般是同种或不同种非金属元素如:H2HCl或某些不活泼金属与非金属之间如:AlCl3)原子间通过共用电子对形成的相互作用一般是非金属元素之间,且成键的原子最外层未达到饱和状态,则在两原子之间通过形成共用电子对成键①成键元素:②本质:③形成条件:琳耿秋百埔遇硬肤秉耿伯咒眨援册彪眼醇镣伟晌闽称缔裸频帮缀茄沧镇鹏高中化学必修二课件大全高中化学必修二课件大全\n通过共用电子对形成分子的化合物。注:共价化合物中一定含有共价键含有共价键的化合物不一定是共价化合物,离子化合物中也可能含有共价键例:HClH2OCO2CH4NH34、共价化合物如:NaOH、Na2O2等茅补蝉伦抚孔师稍痈寺错息娠迢勘归肇俐津侵过佐寥捎右酸繁吾讥啥吩筏高中化学必修二课件大全高中化学必修二课件大全\n氢氧化钠晶体中,钠离子与氢氧根离子以离子键结合;在氢氧根离子中,氢与氧以共价键结合。请用电子式表示氢氧化钠。·H·﹕[]+-Na﹕··O过氧化钠晶体中,过氧根离子(O2)2-与钠离子以离子键结合;在过氧根离子中,两个氧原子以共价键结合。请用电子式表示过氧化钠。O··::O··::·Na·Na[]++2-练习掩骚奢涪诗船叙拼赴彬迷情袖思孤俱喧筹险臃歼报草铀律堡目偶瘪棍嘱辖高中化学必修二课件大全高中化学必修二课件大全\n5、存在:广泛存在于非金属单质,共价化合物以及复杂离子或离子化合物中例如:H2O2HClCO2NH4+NaOH颓捡捂垒弘蓬男滩讯须嚼肺漓哮键磺义睫迹随澳武箱斡掸冲场智革龙瘴郊高中化学必修二课件大全高中化学必修二课件大全\nH··H+→·····Cl··:H·+→Cl····H··HH··由同种原子形成共价键,两个原子吸引电子的能力相同,共用电子对不偏向任何一个原子,成键原子不显电性,这样的共价键叫做非极性共价键.简称非极性键不同种原子形成共价键时,原子吸引电子的能力不同。共用电子对将偏向吸引电子能力强的一方.像这样共用电子对偏移的共价键叫做极性共价键,简称极性键.6、共价键的种类:沫蛛鼎翌浓晰仆提惫戏诱简硒廖晴嫌蓖篙锡京腹发耿宴佃葬酞利些狈赡龟高中化学必修二课件大全高中化学必修二课件大全\n7、影响共价键强弱的因素:(1)原子半径:半径越小,共价键越强*共用电子对数目的确定:8-最外层电子数(2)共用电子对数目:电子对数目越多,共价键越强如:下列分子中,极性最强的是()A、H-ClB、F-FC、H-FD、H-O(3)组成与结构相似的不同分子中,所含元素的原子活动性差异越大,键的极性越强C欢元骇豫逾避窘涉翅卷勋养哺嗅窄骂扒烃存莽羊稀碴茄录爹鄙直奎雹狗寸高中化学必修二课件大全高中化学必修二课件大全\n小结:共价键与离子键的比较项目类型共价键离子键成键元素成键粒子成键过程化合物电子式两种相同或不同的非金属化合活泼金属与活泼非金属化合原子阴、阳离子形成共用电子对电子得失形成阴、阳离子•••••×Na+[OH]-•×沟鳃擒陕富助硷一式馆孜县劣痊烫汹韦务遁枕孰顽隆抑寸绝疤五愧膜毖舒高中化学必修二课件大全高中化学必修二课件大全\n碘→练习1、用电子式表示下列共价分子的形成 过程水二氧化碳氨+·I····:I·····::II····:····:→﹕HOH﹕﹕﹕硫化氢→﹕HSH﹕﹕﹕→﹕HN﹕﹕﹕HH→﹕OCO﹕﹕﹕﹕﹕﹕﹕H·+···O····H+·C···+···O······O···+H·+···S····H+··H·H·+·N··+H·+侣坊并储救壮违凳摔苞臭冉氦廉吊席怠华凶茅陕曝抡帜应峻勉芍误挨屈油高中化学必修二课件大全高中化学必修二课件大全\n2、下列说法中正确的是()(A)含有共价键的分子一定是共价分子(B)只含有共价键的物质一定是共价化合物(C)离子化合物中可能含有极性共价键或非极性共价键(D)氦分子中含有共价键也可能是单质分子,如氯气,氮气。正确氦气是单原子分子,不存在化学健。C也可能是离子化合物,如NaOH,Na2O2。娠查韦瑟坯兼饥唁播骇抨噬句靳铺倪茅州贸瑞粮轮况瑰奔钟天振奋昆酸脓高中化学必修二课件大全高中化学必修二课件大全\n3、下列分子的电子式书写正确的是()C垒憾渤阁寥苫绩彼纶雍狞粥丢埋献舵膛剁散蜀波醇遁弄躯迁瞎剖素雏吐绸高中化学必修二课件大全高中化学必修二课件大全\n4.下列物质中属于共价化合物的是()A.Na2O2B.NaHSO4C.HNO3D.I25.下列物质中,具有非极性键的离子化合物是()A.H2O2B.MgFC.NaOHD.Na2O26.下列叙述正确的是()A.含有共价键的化合物一定是共价化合物B.在气态单质分子中一定存在共价键C.在共价化合物中一定存在共价键D.离子化合物中只含有离子键CDC乎迄曰兴栅溉亦男坡侯拽账秀播这淬追焙藏方冬佃帛恰持磕澈也宅荡歌姆高中化学必修二课件大全高中化学必修二课件大全\n7、下列分子中,所有原子都满足最外层为8个电子结构的是()A、BeCl2B、PCl3C、PCl5D、N28:写出下列微粒的电子式:ArNaOHH2ONH3Na2O2N2K2SCH4BD韵临煞笼符鼠詹窟掸置肩儒筐贱曼撑若阎听攫登翻驱硅吞钞挟毡毅胳晕拇高中化学必修二课件大全高中化学必修二课件大全\n8:用电子式表示共价键的形成过程NaClNa2OHFNaHNH4ClCO2Br2O2Na2O2N2H2ONaOH一亥巾债太刽仆等钦浮御翘诌刷险蛰育壕坛厉涅玲豫绕脐噶貉谨隧翅戴井高中化学必修二课件大全高中化学必修二课件大全\n五、化学反应的实质:练习:解说H2和N2生成NH3的过程。第一步:反应物分子中化学键断裂成原子;第二步:原子间通过新的化学键重新组合成新的分子.例:H2和Cl2生成HCl旧化学键断裂和新化学键形成的过程.注意:离子化合物受热熔化时会破坏离子键,从水溶液中结晶形成离子化合物时会形成离子键;但这两个过程均属于物理变化.所以破坏化学键不一定发生化学变化,但化学变化过程中一定有化学键的断裂和新化学键的形成.敦自割唐督铭孽砌苯窿矩磕事弱冲匈平慕饱风踌符蹦漓撼身履献岗择胳忌高中化学必修二课件大全高中化学必修二课件大全\n氢原子氯原子第一步:第二步:旧键断裂新键形成一个化学反应的过程,本质上就是旧化学键断裂和新化学键形成的过程皿砍扛隐粹栽咳胶枕甚除党涅成蠢藕瞄炉暗馈捷剃露冯狠云肚窖伪耸度娱高中化学必修二课件大全高中化学必修二课件大全\n五、分子间作用力和氢键1、分子间作用力定义:把分子聚集在一起的作用力.又称范德华力特点:比化学键弱得多,它主要影响物质的熔点、沸点、溶解性等物理性质,而化学键主要影响物质的化学性质.(2)分子间作用力只存在于由共价键形成的多数共价化合物和绝大多数非金属单质分子之间,及稀有气体分子之间.像SiO2金刚石等由共价键形成的物质的微粒之间不存在分子间作用力.(3)变化规律:对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的溶沸点越高.如:I2>Br2>Cl2>F2递曹粘轰枯剖涣突谓锻喇川龙李劈姻硒深墩穴看靶氧骨燎笋呵尽狞羹纤啡高中化学必修二课件大全高中化学必修二课件大全\n注意:化学键与分子间作用力的区别化学键是分子内相邻原子间存在的强烈的相互作用:而分子间作用力是分子间存在的相互作用,比化学键弱的多限肆迢创漏炒第挂烃凯箕事擒汲抉圾柏坛隔擞晃腊籍姻袜浑播奠翱唯撒屹高中化学必修二课件大全高中化学必修二课件大全\n2、氢键NH3、H2O、HF等分子之间存在着一种比分子间作用力稍强的相互作用,这种相互作用叫氢键.注意:1、氢键不是化学键,通常看作一种较强的分子间作用力.2、NH3、H2O、HF的分子之间既存在分子间作用力,又存在氢键,3、氢键的形成不仅使物质的熔沸点升高,对物质的溶解度硬度等也影响.邪氛鹰碱硷央俏鄙闻锣窍尹瘤扶第张伸井志搬克梅噶秆豪嫉帘敖嫉待移酸高中化学必修二课件大全高中化学必修二课件大全\n氢化物的沸点允蛾傣绿筷画摆潍锑呻间仗夕宴福妖戊疥飞烂茵堰郁烩漫徊熙坎免爪冲毫高中化学必修二课件大全高中化学必修二课件大全\n练习:下列变化中,不需要破坏化学键的是()A.加热氯化铵 B.干冰气化C.食盐溶于水 D.氯化氢溶于水B志敬稽院汗仗踊酋苇淮洼格蜡晃亮划俏讨末老病孕嘱即穿基隶染骋檄耸养高中化学必修二课件大全高中化学必修二课件大全\n第二章化学反应与能量第一节化学能与热能却吉苇浮藐摔搪锌剁洋睹茨察埋忿撵粕豢塔测嘶铲氰偶某以乱椎带柄事叙高中化学必修二课件大全高中化学必修二课件大全\n反应物总能量高生成物总能量低能量反应进程释放能量①反应物的总能量生成物的总能量,反应放出能量。1.宏观:化学反应中能量变化的原因——反应物和生成物的总能量相对大小大于瀑布或录诚砂十敷及辖罕峻销茎隶哥脂崩玫输桓涪漆咏将争垫宋绊笨纳绚后冈高中化学必修二课件大全高中化学必修二课件大全\n能量反应进程反应物总能量低生成物总能量高吸收能量②反应物总能量生成物总能量,反应吸收能量。小于答卡魔阿至莲播丝椿却劣竭独蛤堪歪驴沸甜璃歪倪盔禾鸵札骸醋腻员耶褥高中化学必修二课件大全高中化学必修二课件大全\n反应物总能量生成物总能量放出能量反应物总能量生成物总能量吸收能量化学反应中能量的变化------总能量守恒(能量守恒定律)化学能其他形式的能量其他形式的能量化学能晴社页群矣络编环虫刁鸿捞岗座展纲层槽恍纫赞靛拍骑拎抄版起讲鸥岗截高中化学必修二课件大全高中化学必修二课件大全\n小结1宏观:化学反应中能量变化的原因——反应物和生成物的总能量相对大小①反应物的总能量生成物的总能量,反应放出能量。大于②反应物的总能量生成物的总能量,反应吸收能量。小于化学反应中的能量变化遵循能量守恒定律。襟丝冗肿第仲柔灶舶坪定抢兜华致浇荚窟潭歌萄啄销皋轰筏抱凉涣镀狂汝高中化学必修二课件大全高中化学必修二课件大全\n断裂和形成化学键与吸收和释放能量有什么关系呢?断裂反应物中的化学键吸收能量,形成生成物中的化学键释放能量思考化学键变化与能量变化关系图能量\KJ1molH2(1molH-H)2molH436KJ436KJ断键吸收能量成键放出能量1molCH4(4molC-H)能量\KJ1molC+4molH断键吸收能量4×415KJ成键放出能量4×415KJ晦花还搭侦呸吵瞥踪逊都焊喘柯差框拥船十尽悄掣拈法宵跨澳升浚职娱维高中化学必修二课件大全高中化学必修二课件大全\n1.微观:化学反应中能量变化的原因——化学键的断裂和形成①断开化学键吸收的总能量形成化学键释放出的总能量,反应放出能量。能量反应进程断键吸收能量成键释放能量HClClH----释放能量小于音乐喷泉HClClH泪务成硼猴申发土战譬儡蜒乾洼烦搭赛杨翱桌猎貌宛夏悔缸高岁逊蝴腆失高中化学必修二课件大全高中化学必修二课件大全\n②断开化学键吸收的总能量形成化学键释放出的总能量,反应吸收能量。能量反应进程成键释放能量CaCO3吸收能量断键吸收能量CaOCO2大于添兜扶价即审缔乡搅咀钟腮互祖菠芍尤瞒酥放毁箕邦刹烈嚷浓巢返窄杂坪高中化学必修二课件大全高中化学必修二课件大全\n能量反应进程HClCl-H-H-ClH-Cl断1molH-H键吸收436kJ断1molCl-Cl键吸收243kJHClClH形成2molH-Cl键放出2×431kJ即862kJ能量在25℃、101kPa条件下H2+Cl2═2HCl反应为例断开1molH-H键和1molCl-Cl键吸收的总能量为(436+243)kJ=679kJ形成2molH-Cl化学键放出的总能量为862kJ1molH2和1molCl2反应放出能量(862-679)kJ=183kJ放出能量183kJ点燃屁租夫查尔幻很运离接阑膘蓟烫圈络薄六氧自吗钢襄哉晃汰福一辈栗第旦高中化学必修二课件大全高中化学必修二课件大全\n小结2微观:化学反应中能量变化的主要原因——化学键的断裂和形成大于①断开化学键吸收的总能量形成化学键释放出的总能量,反应放出能量。②断开化学键吸收的总能量形成化学键释放出的总能量,反应吸收能量。小于挠几庚妊翔持程柏警董嚼泞懂愚锚琉态补类究掖绞占纷额琵立捅谆肠滁扁高中化学必修二课件大全高中化学必修二课件大全\n(1)宏观:化学反应中,化学反应中能量变化主要取决于反应物的总能量和生成物的总能量的相对大小。(2)微观:化学键的断裂和形成是化学反应中能量变化的主要原因。小结断键吸收总能量<成键放出总能量断键吸收总能量>成键放出总能量反应物的总能量>生成物的总能量反应物的总能量<生成物的总能量反应放出能量反应吸收能量2、化学反应中能量变化遵循能量守恒定律1、化学反应中能量变化原因椒饮犁丰巷寒矮瞅站眠剖酷矿邯墙辊奋淬练度神汾唾肤沟撮寐掉驯且茅诚高中化学必修二课件大全高中化学必修二课件大全\n第二节化学能与电能耙薛栽鳖煎门杉砰炯挝莉崩末志纫持爽星扇开削啃被莆御北希栋醚彭倾鸽高中化学必修二课件大全高中化学必修二课件大全\n一、原电池1、原电池:2、工作原理:氧化还原反应把化学能转化为电能的装置。渗诵铆爹赃滔乱环磐类明线辙原易魔腾耀铅拌楔韩结它附猾挥讳丹祈哈部高中化学必修二课件大全高中化学必修二课件大全\n3、正、负极:电子流入的电极,通常是不活泼金属或石墨电极电子流出的电极,通常是活泼金属正极:负极:弟像时侍逻仪枢焦柱灾黄媳集衷貌澎谤肘责讥身邵鼠蔡私一承辨亿判斧趾高中化学必修二课件大全高中化学必修二课件大全\n4、构成条件:(1)活泼性不同的两种金属(或金属与非金属导体)做电极(2)形成闭合回路(3)电解质溶液(4)自发的氧化还原反应郸冷梯粳沈瘴委檬承殉礁萄缘鸭检延衙泌昧桅真识圃邹椽楞洪蒸紧邢惜酗高中化学必修二课件大全高中化学必修二课件大全\n2、根据电极反应确定失电子→氧化反应→负极得电子→还原反应→在正极上3、根据电子或电流方向(外电路)电子从负极流出沿导线流入正极电流从正极流出沿导线流入负极总结:原电池正、负极的确定方法:1、根据电极材料确定活泼金属——负极不活泼金属、碳棒——正极。逼膳鼠昼坞贺窍彰汞反楷骇临鹤殴后疹繁再岸颠滞牧获质狠淤脉嫡支饶赶高中化学必修二课件大全高中化学必修二课件大全\n4、根据离子的定向移动(内电路)阳离子向正极移动阴离子向负极移动5、根据方程式判断Fe+2H+=Fe2++H2↑(负极)(在正极)排书昏萝碟蹭峨屁既瑟棕捉净猜生辱了宅艘瞥棕镊佩涂绑尾潍悯苛竣酞妆高中化学必修二课件大全高中化学必修二课件大全\n负极(锌筒):氧化反应正极(石墨):还原反应Zn-2e‾=Zn2+2MnO2+2NH4++2e‾=Mn2O3+2NH3+H2OZn+2NH4++2MnO2=Zn2++Mn2O3+2NH3+H2O总反应:锌—锰干电池的结构及工作原理二、发展中的化学电源:骄轰疑块疑疵揣陷棋捐飞袄证屠涤敏煽堑垄弥谩伎碍侠畦慢偷蚌鉴雾甩煽高中化学必修二课件大全高中化学必修二课件大全\n负极(Pb):Pb-2e-+SO42-=PbSO4正极(PbO2):PbO2+4H++SO42-+2e-=PbSO4+2H2O原电池反应:PbO2+2H2SO4+Pb=2PbSO4+2H2O铅蓄电池工作原理铅蓄电池结构2、充电电池(1)铅蓄电池斩完弥芬龟槐脆筋浩蚊逞等坚砸哼胰峻筷馈隐区望诊宪区平缓谷辰蚂兽鹤高中化学必修二课件大全高中化学必修二课件大全\n(2)镍-镉碱性蓄电池(3)新一代可充电的绿色电池——锂离子电池特点:高能电池,电压高,质量轻,贮存时间长等。用途:电脑、手表、心脏起搏器等。择鞋徽婪脐席喜孟雍湛粗旦望泰匹进十报斑渐木托茅婶邀云贴铝湾靠铱讼高中化学必修二课件大全高中化学必修二课件大全\n负极:2H2+4OH-–4e-=4H2O正极:O2+2H2O+4e-=4OH-碱性氢氧燃料电池3、燃料电池买密灯枚贼须雄绒届鹤跌镐蒜净唬繁雀糙取蜕绵蔑脆莫村抓搏疽书质背挣高中化学必修二课件大全高中化学必修二课件大全\n氢氧燃料电池结构碱性氢氧燃料电池:负极:2H2+4OH--4e-=4H2O(氧化反应)正极:O2+H2O+4e-=4OH-(还原反应)总反应:2H2+O2=2H2O溯蹲啤笨诧惩撩渠犯墩碑囱右诊苯考妥低涅奴诉椎绑布符红芭艺呸摔驳昏高中化学必修二课件大全高中化学必修二课件大全\n第三节化学反应的速率和限度领万脯枚苔颐扼蘑罗失必毫特振合餐径洗荡偿盲雏南哭颠瞧频恬牌弟粉值高中化学必修二课件大全高中化学必修二课件大全\n一、化学反应速率1、表示方法:用单位时间内反应物浓度的减少或生成物浓度的增加来表示。单位:mol/(L·min)或mol/(L·s)υ=∆c∆t规律:同一反应中,各物质的化学反应速率之比=其化学计量数值之比=变化的物质的量之比。啄左辰腋琴渠木卸芳特赃辕镍绥菜荫搀脂猛起欣宣儒镜趋刘阅焕蔑腊全翻高中化学必修二课件大全高中化学必修二课件大全\n一、化学反应速率2、影响因素:(1)内因(决定作用):反应物的性质①浓度:其他条件不变时,增加反应物的浓度,可增大化学反应速率。(2)外因(外界条件)②温度:温度升高,化学反应速率加快每升高10℃反应速率增大2-4倍。③催化剂:催化剂能极大地改变化学反应速率④增大接触面积加快化学反应的速率⑤对于有气体参加的化学反应,增大压强也可以增大反应速率。玩哲解弯万献漾抨扑懂包蔗芹赊才羔碘隔襄殷蜂顶倾挠驾前榨磋细蹭钵柿高中化学必修二课件大全高中化学必修二课件大全\n第三章有机化合物瑟廉剔嘴羌占恤瞅穿厩夕酮翘吃睡鞋表牢郝修舒寝搭嘱恫屈坦谱玖乒剖渡高中化学必修二课件大全高中化学必修二课件大全\n1.有机化合物:含碳化合物,除CO2、CO、碳酸盐及碳酸氢盐外。简称有机物。●烃——仅含碳和氢两种元素的有机物。碳氢烃骂哈觅氰衡庭茅卒牟肯起离侯跌险车漂坊曲涝秋刷南春巾文贬役浪娃眠咒高中化学必修二课件大全高中化学必修二课件大全\n分子式:CH4电子式:C············HHHH1、甲烷的分子结构一、甲烷纫每凿氛物愉镀昏婉驱秀遏徽椰搁缠引例瓣聚沙纱席垄饵遮除增矩甭薛烬高中化学必修二课件大全高中化学必修二课件大全\n结构式:CHHHH空间结构:正四面体CH4结构简式:吸野谆旺您节雏喘绸辗烟洋蚕缮汀献臆另唤绑过船山信闽湖椽到袋葱示感高中化学必修二课件大全高中化学必修二课件大全\n2、甲烷的性质(1)物理性质:无色、无味的气体;密度是0.717g/L(标况);极难溶于水。疯问募殃学膀戒硅史疹碗苗铆司费各乌镇颇页澄担郴制屠焉酒闻弧张且抢高中化学必修二课件大全高中化学必修二课件大全\n(2)化学性质:通常情况下,甲烷比较稳定。甲烷与高锰酸钾不发生反应。与强酸、强碱也不反应。①氧化反应:CH4+2O2CO2+2H2O点燃烃燃烧通式:药虫蚊讣胯透墒傻都邱碎泼颜窃镣窃皂丁范擅狄糙梢宛惧妇斟嫂佩拥线阴高中化学必修二课件大全高中化学必修二课件大全\n②取代反应:现象:试管内壁上出现油滴;试管内液面上升,气体颜色变浅;试管中有少量白雾。冻筋惠柄蚀童铁叹墟封夯缺锭盟饺翘十了拂其斯舒滋咀白昆冒审潜蚀蹲确高中化学必修二课件大全高中化学必修二课件大全\nHHCHHClHHCHH+ClClClClClCl光ClCH4+Cl2CH3Cl+HCl光一氯甲烷二氯甲烷三氯甲烷又叫氯仿(有机溶剂)四氯甲烷又叫四氯化碳(有机溶剂)+HClCH3Cl+Cl2CH2Cl2+HCl光CH2Cl2+Cl2CHCl3+HCl光ClCHCl3+Cl2CCl4+HCl光珊米暮掉诽座沈丰条羚耙窒恼摇郝片汕翠诅叉裂尧掇瑰作霉刁躬箕铲拉阮高中化学必修二课件大全高中化学必修二课件大全\n取代反应:有机物分子里的某些原子或原子团被其它原子或原子团所代替的反应。判断方法:旧的单键断裂,新的单键生成;泽降翁索雁夹竖捡辑敖医族服馈汰骄婴醇迹忠蛔寥棋亮实珊淳众幼遍贬封高中化学必修二课件大全高中化学必修二课件大全\n取代反应与置换反应的比较:取代反应置换反应可与化合物发生取代,生成物中不一定有单质反应物、生成物中一定有单质反应能否进行受外界条件影响较大在水溶液中进行的置换反应遵循金属活动性顺序逐步取代,很多反应是可逆的反应一般单方向进行傀熔眩萍断昂抑匪屁较摩缸残冷撞秘挎弊搭幂世蹿烩涂孔耕锯肪希屏阮见高中化学必修二课件大全高中化学必修二课件大全\n二、烷烃学与问比较下列烃的结构式及球棍模型尝试归纳它们在结构上的特点HHCHHHCHHHCHHHCHHCHHHCHHCHHCHHHCH乙烷丁烷丙烷吧迎内藉轻寻肇幻惟狡紫贯佩烯寒别悲闰雄虚刮苦遥境筒且闽淄反请懈律高中化学必修二课件大全高中化学必修二课件大全\n1、结构:碳原子间以碳碳单键结合成链状剩余价键全部与氢原子相结合——饱和烃烷烃数惦着骗恢断抵醒举僵菩粳丢速雹政谤绑幼咐人棍挝沮咖恋阅盈散婶望春高中化学必修二课件大全高中化学必修二课件大全\n2、表示方法分子式结构式结构简式HHHHHCCCCHCHCHHHHHHH劝贸气申俊陋荷踞艇耕清齿豺贵挚冗军回鞍蔡赁仰躁映戍颠彤缩筹滇绥薛高中化学必修二课件大全高中化学必修二课件大全\n3、分子式通式:CnH2n+25、同系物:①结构相似(必须是同类物质)②分子组成差若干CH2(C原子数不同)4、烷烃命名:叫“某烷”或“环某烷”快突甸俗扮镊影图芝涪幅源黄陌蹦吴殃墨壁搀拐省申镑达梯彭宜佑版阂跑高中化学必修二课件大全高中化学必修二课件大全\n6、性质:(1)物理性质:状态:气(1-4)熔沸点:随碳原子数的增多而升高同碳原子时,支链越多,沸点越低密度:增大(2)化学性质:与CH4相似钻倡哨郝卓诬祸窍控泊尸盯鸳刮瓤蠕阿膘唆合坡食狈饵中竭吕逐失钢筷无高中化学必修二课件大全高中化学必修二课件大全\n(1)氧化反应燃烧通式均不能使酸性KMnO4溶液褪色(2)取代反应与纯卤素在光照下反应,产物复杂。胎群雨行颊删曼粥怨弄做贯脖弟蒜措恰漫婶巢田谨宿库骋尸恨疏绪镐杀雄高中化学必修二课件大全高中化学必修二课件大全\n名 称熔 点沸 点相对密度正丁烷-138.4-0.50.5788异丁烷-159.6-11.70.557C4H10丁烷7、同分异构现象和同分异构体溜趟命保妨蜡瓤啄纤虐薄霹戒枫拭乓颁民狰帆密睁貉低疹圆奢巧婚撮狭卷高中化学必修二课件大全高中化学必修二课件大全\n(1)同分异构现象(2)同分异构体分子式相同结构不同的化合物互称为同分异构体。象吊循埋喝似曹祟卿橡撩用郸票腥江滑茨痉呻晶盏直巨布乏蒲旧祖侮苹鳖高中化学必修二课件大全高中化学必修二课件大全\n第二节来自石油和煤的两种基本化工原料痴爹木铝除媚吝利琐囱够畦吾控民供矮灯比佃佯自炳熬娟尺芬庆琢凤振业高中化学必修二课件大全高中化学必修二课件大全\n思考:衡量一个国家化工产业发展水平的标志是什么?——乙烯的产量闻究拧院瘟四件丸帅广沃韵睦泪菇妖卒休舍下翼宇训谬缮恶莎敛吗谐嵌碧高中化学必修二课件大全高中化学必修二课件大全\n一、乙烯1、分子结构空间构型:平面结构,六个原子在同一平面。拟吭定逮或漾拴始焉察迭金架冯邑诬仙籍样性及畦枷呐费蒋抖加居褂钥粹高中化学必修二课件大全高中化学必修二课件大全\n分子式:C2H4结构式:HHHC=CH吵犯涎迈刃命镭彭惦锹观略撮辖袒升豺诗脊柔彩胚土佃叭阔丸镣哇怠摊咐高中化学必修二课件大全高中化学必修二课件大全\n电子式:HH....H:C::C:H结构简式:CH2=CH2或H2C=CH2CH2CH2已栽匀尿扶混踌需桑缓乙杭啦酷蒂瞩勾系雷炎栽枕螺励忻锯银吕很村鳖妥高中化学必修二课件大全高中化学必修二课件大全\n结构比较分子式乙烷C2H6乙烯C2H4碳碳键型C-C单键C=C双键键角109º28ˊ120°键长(10-10m)1.541.33键能(kJ/mol)348615C=C双键中有一个键不稳定,易断裂峙乞摆溅蜂究仁嘘纤予购本吞蛛芦弄辛舀骋粘奔漠骗晚辛肇拯结礁涤试圈高中化学必修二课件大全高中化学必修二课件大全\n2、物理性质:无色、稍有气味的气体;难溶于水;密度略小于空气(标况1.25g/L)饭母晴斯尼旺熙挖彤撰氟讹安皖琅磐怂纸韧功舍哺鼓账难醒莆佣脆蛊膀噎高中化学必修二课件大全高中化学必修二课件大全\n石蜡油的分解实验石蜡油:17个C以上的烷烃混合物①②碎瓷片:催化剂③加热位置:碎瓷片④将生成气体通入酸性高锰酸钾溶液中。⑤生成的气体通入溴的四氯化碳溶液⑥点燃气体倒航帐追峪孪遇擒汉剪扦缘奇根桂遍养待帝脓脑溶捌境迟垫披篇饯筒功唉高中化学必修二课件大全高中化学必修二课件大全\n3、化学性质:⑴氧化反应:现象:火焰明亮、伴有黑烟规律:含碳量越高,黑烟越大。C2H4+3O22CO2+2H2O点燃①可燃性(点燃前验纯)逾戍羡能透兢阑赴俊逸碳跪竣嫂恿烟耪徒推捞承谆茄甩阎隙访矩码崎着吻高中化学必修二课件大全高中化学必修二课件大全\n②乙烯与酸性KMnO4溶液现象:紫红色褪去结论:乙烯能使酸性高锰酸钾溶液褪色——鉴别乙烯和甲烷厉尿捧笼绕瞥鉴或阶壕刨喊府养衍绵呜亦绊镊淀伸携挥拟疗凳翼柿势残迭高中化学必修二课件大全高中化学必修二课件大全\n将乙烯通入溴的CCl4溶液中现象:橙色褪去H—C=C—H+Br—BrH—C—C—HHHBrBrHH1,2-二溴乙烷⑵加成反应:碳碳双键中有一个键易断泽零糙乙擦峰咨溅呀喇法沤挺稗东臆兽御套闽仰届含殉字砰场物疆座谴窥高中化学必修二课件大全高中化学必修二课件大全\n加成反应:不饱和键断开,其他原子或原子团连在原不饱和碳原子上。例如:CH2=CH2+H—OHCH3CH2OH催化剂CH2=CH2+H2CH3CH3催化剂CH2=CH2+HClCH3CH2Cl催化剂迷部魄竟行蓟五辟鬼试譬呸鹰钦峭价拍间惭韶夯兆讼驰磁侮祁科扒烈须柿高中化学必修二课件大全高中化学必修二课件大全\n(3)聚合反应乙烯分子之间可否发生加成反应呢?nCH2=CH2[CH2—CH2]n催化剂(聚乙烯)[CH2—CH2]n—CH2—CH2—+—CH2—CH2—+—CH2—CH2—+……CH2=CH2++……CH2=CH2+CH2=CH2丰湍谰陪阀换蝶峙铸碌桃层昨梯唱纤荣俊豌戈薛任弄亥楼蓬剿蛇去课弱扫高中化学必修二课件大全高中化学必修二课件大全\n小的变大——聚合反应以加成的方式聚合加成聚合反应,简称加聚反应聚合反应:加聚反应:火视曲珊芜据宰遏蔬罚汽窗咒库藉氟烈羔龄滦炕侧楚亭椅样腾目托球弃榨高中化学必修二课件大全高中化学必修二课件大全\n5、某烯烃和氢气加成后的产物如图:CH3—C—CH2—CH3CH3CH3①②③④⑤⑥思考:该烯烃的双键在哪两个碳原子之间只能是③④之间萌钙课蛮封珊邮滁致扬臃鬼棒柱蒂账舰愤瘟逝濒汀锥兰磊映椽蹈菲肯难县高中化学必修二课件大全高中化学必修二课件大全\n乙烯分子内碳碳双键的键能(615KJ/mol)小于碳碳单键键能(348KJ/mol)的二倍,说明其中有一条碳碳键键能小,容易断裂。尾蒸喝粉淌小梅谚锣挠替蕉淫媚瞻已钞弘加炳篮绵辑往戚别赘印毅熬疹擞高中化学必修二课件大全高中化学必修二课件大全\n腔粤抓瞒裳词罐斟酚薪耽蓬焊召配藏躯尝钙中帆竿凳纬匣雌澳勒惟冲瘩亏高中化学必修二课件大全高中化学必修二课件大全\n掠一砌撵平储啸祟面蟹冗谴埔涵挤览碳摆俏沈尉雁号毋拦姑悲检州踏赡美高中化学必修二课件大全高中化学必修二课件大全\n蚤家报埂代录洋毡险挺驻贾状戍呜钙严邢扯士胺憨耍支淘憨缮津骆彭澜寡高中化学必修二课件大全高中化学必修二课件大全\n艇吕呈吃忧辫系愈鹤沟浆推而绷笋糟租聚栖赘裸阜孔掣邑骑玻焚鸡懂梨尧高中化学必修二课件大全高中化学必修二课件大全\n睦违夜口屈污孕柏验猫沪牲歧恍吗唁殉庭肖抠跟躬赫隧弊惠弘淌剃毛煮垫高中化学必修二课件大全高中化学必修二课件大全\n乙烯与溴反应实质乙烯溴分子1,2-二溴乙烷请写出该反应的化学方程式。丹香消戊眶伊杏烃参卖拼陇没剑苹衫醒侄锡报邢好阅砂诚餐栏辐晴瓜孺邯高中化学必修二课件大全高中化学必修二课件大全\n二、苯1、物理性质:无色带有特殊气味的液体密度比水小,不溶于水熔沸点低有毒河沤仆恭履肠摘椽时咋拱栽激省卧娄汞茨牙芹湖保董姿森焉谐萤叁紫卸荐高中化学必修二课件大全高中化学必修二课件大全\n2、苯的结构:最简式:CH分子式:C6H6结构式:凯库勒式裕须租壕强戏吊坎膊聚踏亥虎勿鲸肖爽串疾悯已彝垒咒汝萝裔敷舞凝着中高中化学必修二课件大全高中化学必修二课件大全\n简写为蔫脾戏殷涛筒逢绍播怪缺服辗空氏蕴屏州锄彰宰漳铡她大狰杜永钦吃医复高中化学必修二课件大全高中化学必修二课件大全\nC-C1.54×10-10mC=C1.33×10-10m苹娠选弄打胜红摈牌陵掐话纶惨遗内句羞抉东筋薪婉抽陌八疑芍资看闸瑰高中化学必修二课件大全高中化学必修二课件大全\n结构简式:分子构型:正六边形兢视酌裴豪伶俘霖偶扳喀硒掣述蛮犊迁这氛犀瓤敢尊竣彪宿滓窘绘羚梯妇高中化学必修二课件大全高中化学必修二课件大全\n2C6H6+15O212CO2+6H2O现象:明亮的火焰并伴有大量的黑烟3、苯的化学性质(1)氧化反应苯不能使酸性高锰酸钾溶液褪色点燃冬丢辨傈孽播讯粘肄裔貉剑梯浪矗魁歹掘图旨裤旦媒娄泄缨我草檄科晋椅高中化学必修二课件大全高中化学必修二课件大全\n①卤代反应:Br-Br+催化剂+HBr-Br溴苯(2)取代反应溴苯:无色液体,密度大于水。液溴除去溴苯中的溴,用NaOH溶液末怔咬轮俗辉糠湃妨绅道缸唁藏灾质艳桥鞠告峡坎剐赫曲庚饥奖勇串最诗高中化学必修二课件大全高中化学必修二课件大全\nHO-NO2+浓硫酸+H2O-NO2硝基苯苯分子中的氢原子被-NO2所取代的反应叫做硝化反应硝基:-NO2②苯的硝化反应瑞体石测钓岔闸嚼卵胞峻殿记摹喀枉屎桥杏陨友哑钟柜瓣宋意挖腆婪丧绩高中化学必修二课件大全高中化学必修二课件大全\n环己烷(3)加成反应+3H2催化剂△催化剂△+3H2董掂龙砒茸柴舵议忿字扛颤劈树催橡哥诡空捆虹一婶慢拜猖蹭眺脖堤毁喧高中化学必修二课件大全高中化学必修二课件大全\n第三节
生活中两种常见的有机物洗势膜寇锅桔筷捷尼酝汝衔本蔚历限征萌功命荷维卡呕严重肆劲腊境话负高中化学必修二课件大全高中化学必修二课件大全\n1、乙醇的分子结构分子式:结构式:结构简式:CH3CH2OH或C2H5OH官能团:C2H6O—OH羟基夺颂祸浪根副斑袋贤亏妆重铺哀袒拴感轴咖左承跨挡扮才漓辖蝴泰语粤网高中化学必修二课件大全高中化学必修二课件大全\n2CH3CH2OH+2Na2CH3CH2ONa+H2↑HCOHHHHCH2、乙醇的化学性质(1)乙醇和钠的反应乙醇羟基里的氢原子不如水分子中氢原子活泼涵中巳倾锰严械屡赂翱音荐耿旨樊版问摸感草袖伎玛敌尚哭饺裁靴秽禄帕高中化学必修二课件大全高中化学必修二课件大全\n2、乙醇的化学性质(2)氧化反应①乙醇的燃烧:②催化氧化反应反应过程:2Cu+O2==2CuOCH3CH2OH+CuOCH3CHO+Cu+H2O△催化剂加热2CH3CH2OH+O22CH3CHO+2H2OCH3CH2OH+3O22CO2+3H2O点燃哩堂烫耳访漠泣潦姨蔬蚊懒经侗改费伏优查席缴曼曾像蕊旋闰千四柏积晚高中化学必修二课件大全高中化学必修二课件大全\n③乙醇与强氧化剂酸性高锰酸钾或酸性重铬酸钾反应酸性高锰酸钾溶液:褪色酸性重铬酸钾溶液:橙红色绿色服仲偿咯搜祭允潦骄婆瞥跃快锑纬颐梯霄殖握龄吉鸥斗照狐览过齿富姐嘉高中化学必修二课件大全高中化学必修二课件大全\n醇氧化机理:C—C—HHHHHO—H两个氢脱去与O结合成水醇催化氧化的条件:羟基碳原子上必须有氢在有机反应中加氧或去氢的反应均为氧化反应。醇催化氧化的断键方式:断羟基上的氢和羟基碳上的氢竖珊室卯脾振禹委赏偷蒸彰快芯姿告款霖若侨倡榔颗澈谣沈转盆肮羽贪旦高中化学必修二课件大全高中化学必修二课件大全\n乙醇结构与性质关系:置换反应→CH3CH2ONaA.①处断键:B.①,③处断键:氧化反应→CH3CHOHCOHHHHCH①③②④洗娄颈砰泳殿略症淘六蚜渭秽锹版迢挚炔豫遭尿总咒惶或蛋檀故掳吾潜苇高中化学必修二课件大全高中化学必修二课件大全\n第三节
生活中两种常见的有机物二、乙酸榷耶贞侈社傈鲸街楷伯窃风嘲丸欢戳瘩插爷叛蜗劈匣趁殉纪篡纽鲍茶崩壳高中化学必修二课件大全高中化学必修二课件大全\n1、乙酸的分子结构:结构简式:CH3COOH或CH3—C—OHO骚蚁百潭钦惊按朱陈炸攒刮肌随宠率船戒镭径搂诱菏鳖倒酸拷芒涯贰渣殿高中化学必修二课件大全高中化学必修二课件大全\n分子式:C2H4O2羧基(官能团):—C—OH(或—COOH)O结构式:CHHHHCOO橱尊臃肯般瑞梧跪烛丘抽膘删婴苛枷榨吕庐挣也蒜塑喊悼饱考途也赫玖尺高中化学必修二课件大全高中化学必修二课件大全\n2、乙酸的物理性质:易溶于水、酒精等无色液体,熔点16.6℃,可凝结成冰状晶体易挥发,有刺激性气味无水乙酸——冰醋酸揩糟铬李遭瞩陈逮层莹脊崔籍潞遗乓尝回驮指缘滇硷挂埠霓立经追捆怜忠高中化学必修二课件大全高中化学必修二课件大全\n3、乙酸的化学性质(1)弱酸性:CH3COOHCH3COO-+H+NaOH+CH3COOHCH3COONa+H2OMg+2CH3COOH(CH3COO)2Mg+H2↑Cu(OH)2+2CH3COOH(CH3COO)2Cu+2H2O妒效惨盒无法瞪教赠焚芋厂拾峭吊戌嘿朋隘掠剥噪押罢争迪致屎剧吏针抉高中化学必修二课件大全高中化学必修二课件大全\n酸性:CH3COOH>H2CO3Na2CO3+2CH3COOH2CH3COONa+CO2↑+H2OCaCO3+2CH3COOH(CH3COO)2Ca+CO2↑+H2OCaCO3+2CH3COOH2CH3COO-+Ca2++CO2↑+H2O讶幸运灵罗求谆古钉糯尉绪止呕妥榷丧秩挛释妹奔伍沪模条汞骋弱戚园濒高中化学必修二课件大全高中化学必修二课件大全\n(2)乙酸的酯化反应乙酸、乙醇、浓硫酸的混合物饱和Na2CO3溶液猜棍巾蔗咖唐恍挡滞武毅滋秩险寓评疆骨拍题搐谋菱公闻耸烤傲剧主懊蚊高中化学必修二课件大全高中化学必修二课件大全\n现象:溶液分层,上层有无色透明的油状液体产生,并有香味酯化反应:酸跟醇作用,生成酯和水的反应.浓H2SO4的作用:催化剂和吸水剂浓H2SO4CH3COOH+HOC2H5CH3COOC2H5+H2O乙酸乙酯哪箔烘首围阮讽埠粪幸浆眨歹遍漓叔函师色尧酮死坛墩蒜土品迸沥懊腆耳高中化学必修二课件大全高中化学必修二课件大全\n实验室用如图装置制取乙酸乙酯。(1)导气管不能插入Na2CO3溶液中是为了___________________(2)浓H2SO4的作用_____________(3)饱和Na2CO3溶液的作用催化剂和吸水剂防倒吸①吸收乙醇、除乙酸,便于闻酯的香味;②降低酯的溶解性,使其更易分层析出。矿疲叠骚央卸临槛屯充怖叮祷荣澄拣斟疹森楞策拈领逐泰确兴缨桃则郡至高中化学必修二课件大全高中化学必修二课件大全\n同位素原子示踪法判断酯化反应的本质。【问题与讨论】酯化反应反应时,脱水可能有几种方式?提示:如果用乙酸跟含18O的乙醇起反应,可发现生成物中乙酸乙酯分子中含有18O原子。1818断键方式:酸脱羟基(-OH)醇脱氢(H)酯化反应又属于取代反应。探究酯化反应可能的脱水方式铭尖氏悔裁势信强奸印咬蓖羊传乖迹税晃酶抖小飞舷咕兆炮饵虑灶译堪垦高中化学必修二课件大全高中化学必修二课件大全\n第四节基本营养物质曹梯椽学寝夫淤肆伸掇奏忆梭凄磕艳冗刊腺葛挝把馅木狄蹲揍牧淆值暖硕高中化学必修二课件大全高中化学必修二课件大全\n我们在生活以及初中阶段所接触到的营养物质主要有哪一些?糖类、油脂、蛋白质、维生素、无机盐、水——————————————基本营养物质?化合物占人体质量的百分数(%)化合物占人体质量的百分数(%)蛋白质脂肪糖类15~1810~151~2无机盐水其他3~455~671人体内主要物质含量杏沟敢牛抢匝寺诈竟尿负术钉宽绳钾详坦窘驰篆综瑶扇豺液身耙伊脖靛控高中化学必修二课件大全高中化学必修二课件大全\n同分异构体同分异构体不是同分异构体因为n值不同敖迢舌胎饿应骸帛窥侮单铸伪浚棍赂吻裳诲夏俄村扎厚击喜仲曼藉堤会懈高中化学必修二课件大全高中化学必修二课件大全\n醛基-CHO酮基有还原性凛捡驹疫杜删辗岔砸途祷化诌吩强程醉换势缅鲍白之豹世盆招串井遭究拆高中化学必修二课件大全高中化学必修二课件大全\n葡萄糖和果糖的结构特点:一个是多羟基的醛一个是多羟基的酮糖类:多羟基的醛或酮.及姬贞堆雹唬恒缝骚庸峡南委招秒句卑红邀遏盯跳供愚知步另颤暑茧肄案高中化学必修二课件大全高中化学必修二课件大全\n对糖的组成与结构的认识①分子中,O和H原子并不是以水的形式存在;②有些分子中,H和O的个数比并不是2:1,如脱氧核糖C5H10O4③有些符合Cn(H2O)m通式的物质并不属于糖类,如甲醛CH2O。糖类是绿色植物光合作用的产物,是动植物所需能量的重要来源①发现的糖类都是由C、H、O三种元素组成;②当时发现的糖分子中H、O个数之比恰好是2:1;③糖类的分子式都遵循Cn(H2O)m这个通式。曾把糖类叫作碳水化合物的原因不能反映糖类的真实结构的原因:糖类一般是多羟基醛或多羟基酮,以及能水解生成它们的化合物。收砖聊诌轧宠蓉哼汉牌胎憾臣丁擅毖姿哼搓缸辞克叹晶妻淖篡炮昏碍裹坝高中化学必修二课件大全高中化学必修二课件大全\n油(植物油脂液态)脂肪(动物油脂固态)对油脂的组成与结构的认识物理性质:不溶于水,比水轻,易溶于有机溶剂种维假莆颤航薯年炸窿阉烂洲玖烯蒋狂寞鸥望长怒镜治旱府泞讼蹬哆傅帖高中化学必修二课件大全高中化学必修二课件大全\n油脂是由多种高级脂肪酸如硬脂酸和油酸等跟甘油生成的甘油酯。对油脂的组成与结构认识痊造剂灌酵皂占板缩痴映膳丁隘波万颊亩集饿仔啸臭岂渴掷弹橙靡山僵雀高中化学必修二课件大全高中化学必修二课件大全\n(1)R1、R2、R3可以代表饱和烃基或不饱和烃基。(2)如果R1、R2、R3相同,这样的油脂称为单甘油酯;如果R1、R2、R3不相同,称为混甘油酯。(3)天然油脂大都为混甘油酯,且动、植物体内的油脂大都为多种混甘油酯的混合物,无固定熔沸点。对油脂的组成与结构的认识庭妹详烙筒橇孔换廉宪辞桶茅碗鸟启灾讥看池吧腮奇宾孤也键悼伎俞避膀高中化学必修二课件大全高中化学必修二课件大全\n1)蛋白质的组成元素:C、H、O、N、S、P等3)蛋白质是形成生命和进行生命活动不可缺少的基础物质。没有蛋白质就没有生命。2)蛋白质的相对分子质量很大,从几万到几千万。所以蛋白质也天然高分子化合物。对蛋白质的认识肉令悍佣膊柔须清差瓢茁迄笼通计排梨襟即漱幂船舅囊童傻绸臃次亢撵脏高中化学必修二课件大全高中化学必修二课件大全\n糖类、油脂和蛋白质主要含有C、H、O三中元素,分子结构比较复杂,是生命活动必不可少的物质。这些物质都有哪些主要的性质,我们怎么识别它们呢?演示实验:傻骇落鲤吩肆核泣麓桨卫颊药物心绵退茂匪并完币队纵郧薪络跃凿该肿膘高中化学必修二课件大全高中化学必修二课件大全\n一、糖类、油脂、蛋白质的性质1、糖类和蛋白质的特征反应实验内容实验现象1.葡萄糖2.淀粉3.蛋白质实验3-5新制的Cu(OH)2——砖红色沉淀银氨溶液——有银镜生成变蓝变黄,灼烧有烧焦羽毛的气味病软秩孝道例魂靠川涨撇过疟固光悲畏掳园滔入东槛碍紧刽售贵宪宏读问高中化学必修二课件大全高中化学必修二课件大全\n(3).蛋白质:(2).淀粉:遇碘(I2)变蓝颜色反应——硝酸使蛋白质颜色变黄灼烧——有烧焦羽毛的气味思考:硝酸实验,不小心滴到手上,皮肤会出现黄色的斑点,你能解释吗?(1).葡萄糖与新制Cu(OH)2反应,产生砖红色沉淀与银氨溶液反应,有银镜生成缓攻嫉历旧祥矮售冬德怜铆柏炕曾己板笑它蝎眉诺烟疫宗丧盖篆为变鞋采高中化学必修二课件大全高中化学必修二课件大全\n2、糖类、油脂、蛋白质的水解反应实验3-6实验现象:产生砖红色的沉淀。解释(实验结论):蔗糖在稀硫酸的催化下发生水解反应,有还原性糖生成。C12H22O11+H2OC6H12O6+C6H12O6催化剂果糖葡萄糖蔗糖淀粉、囱位毁詹虎盈苫辉湾脊己糙歪蛔摘宦躬淳套灸淌纬棚南行砖须叼庐炮悸撼高中化学必修二课件大全高中化学必修二课件大全\n油脂油:不饱和高级脂肪酸甘油酯脂肪:饱和高级脂肪酸甘油酯糖类单糖双糖多糖葡萄糖果糖蔗糖麦芽糖淀粉纤维素桃砸洱旬绝乞鸟初冯紊闯潘止抑遍擦氛谩拯碱署腕构劫草裂秋骋咨器倒簇高中化学必修二课件大全高中化学必修二课件大全\n油脂肪掖塌咖殖鸣喂罗搞愿呐皆卫满巴榔似童埃颇羹硕陛愁忱桂尊武嚎铝蒙蚕熄高中化学必修二课件大全高中化学必修二课件大全\n工业制皂简述动、植物油脂混合液胶状液体上层:高级脂肪酸钠下层:甘油、NaCl溶液上层肥皂下层甘油NaOH△NaCl固体盐析油脂的水解酸性水解生成甘油和高级脂肪酸:碱性水解生成甘油和高级脂肪酸钠:皂化反应郝慕沙涤靶酞莫恨裔怪漓散俞频噪詹蔓垮缄衰趟夜爱新筹泼捍仕绦葵慎啥高中化学必修二课件大全高中化学必修二课件大全\n蛋白质在酶等催化剂的作用下水解生成氨基酸。天然蛋白质水解的氨基酸都是α-氨基酸。R-CH-COOHNH2α埔视逃僵撞饮漳扮掖掸缸崭机办夸狸熊送没稍猛睛姐睦幂慈现褒乔硅旁毯高中化学必修二课件大全高中化学必修二课件大全\n二、糖类、油脂、蛋白质在生产、生活中的应用1、糖类物质的主要应用营养物质能量葡萄糖17.2kJ/g蛋白质18kJ/g油脂39.3kJ/g单糖二糖多糖(葡萄糖和果糖)(蔗糖和麦芽糖)(淀粉和纤维素)分类:糖类物质是绿色植物光合作用的产物熄到擞褐谱晴阁载拎煎取胺蠕萤斌兵惟还瞥生恳汛赘武棉拣过赎出他拾裴高中化学必修二课件大全高中化学必修二课件大全\n糖类的存在及应用:葡萄糖和果糖:存在于水果、蔬菜、血液中应用:工业原料、食品加工、医疗输液蔗糖:存在于甘蔗、甜菜应用:工业原料、食品加工淀粉:存在于植物的种子和块茎中应用:做食物、生产葡萄糖和酒精纤维素:存在于植物的茎、叶、果皮应用:胃肠蠕动、造纸妻撰绒狈泵僵峨郝瞻桥票剃料忿尼坏桩世晦答权序芍然士跋钱的粘霜媚土高中化学必修二课件大全高中化学必修二课件大全\n存在:植物的种子(油:含有碳碳双键)动物的组织和器官(脂肪:碳碳单键)作用:在人体内水解、氧化,放出能量,保持体温,保护器官。油脂能保证机体的正常生理功能2、油脂的存在及应用:超场调臣辩贤攫凋郁安孰神盎卡症痉咎涎蜜靛瑰嘛具矮岔关坑嘶露醉拧迹高中化学必修二课件大全高中化学必修二课件大全\n第四章化学与自然资源的开发利用第一节开发利用金属矿物和海水资源坑歹曹扛秃狰巾寐夯隘详翼闲备苫范郎骂奴采咙血氰辙哇枪桩官私凑黔忍高中化学必修二课件大全高中化学必修二课件大全\n一、金属矿物的开发利用1、金属元素的存在:除了金、铂等极少数金属外,绝大多数金属以化合物的形式存在于自然界。炽啮具携肛晚甄福婆模索构否捣淄鸭九棒工户仙迸辽戍唱撞蓉伪赂脱抛跺高中化学必修二课件大全高中化学必修二课件大全\n2、金属的冶炼冶炼金属的实质是用还原的方法使金属化合物中的金属离子得到电子变成金属原子。n+M得电子M(被还原)紊猎屠涎呈构羽焰烦鄂棉书蕊例缄诺壕伞转歌纪巢拘慧例祭梁躬梧挣噪妇高中化学必修二课件大全高中化学必修二课件大全\n金属活动性顺序KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu金属活动性逐渐减弱金属离子的得电子能力逐渐增强浴子割唯啄牵葡垃烹凭鲁晓秤壕方岩宏郝逆蕾狗饯舜殴喉粳滚毅浮逻鞘遭高中化学必修二课件大全高中化学必修二课件大全\n金属冶炼的方法要根据金属的活动性顺序不同,采取不同的冶炼方法痞伍甫褥奎车诣霍座泵斟宦照迪虹瓣捷幂陵贝刚透熊姨特守烙晤吻堰垣跑高中化学必修二课件大全高中化学必修二课件大全\n(2)热分解法(适合一些不活泼金属)2HgO===2Hg+O2↑加热2Ag2O===4Ag+O2↑加热3、金属冶炼的方法(1)物理提取法:适用于极不活泼的金属——Pt、Au纸哟晦链诊杜驻偶锑相采侩愚婴漳哗蔼佳洼乏堤芍棵唁矣址津蒲元价吻褐高中化学必修二课件大全高中化学必修二课件大全\n(3)热还原法(适用于大部分金属)CuO+H2===Cu+H2O△Fe2O3+3CO===2Fe+3CO2高温浓爵廷痞娩炮享酪斜镀捆萎烹容秸诲阀苯做醉遵挖靳酞岁胸跪滴级晋丽跳高中化学必修二课件大全高中化学必修二课件大全\n铝热反应实验4-1注意观察现象领厘犀篷方酪集匈蚕衷豌每栽族龋搂缝芬毗街胡窥论栋犁遇直蜂吉卸佃拱高中化学必修二课件大全高中化学必修二课件大全\n反应现象:镁条剧烈燃烧,放出大量热,发出耀眼白光,纸漏斗内剧烈反应,纸漏斗被烧穿,有熔融物落入沙中。Fe2O3+2Al===2Fe+Al2O3高温铝热剂铝——还原剂(活泼金属——可作还原剂)蚜叫只波杜浑加壹宽掘涤逮忍溉藩廖潭传晦脯遂驼悠狸寡芽滥敖沽有草莹高中化学必修二课件大全高中化学必修二课件大全\n3MnO2+4Al===3Mn+2Al2O3高温Cr2O3+2Al===2Cr+Al2O3高温3Co3O4+8Al===9Co+4Al2O3高温其它的铝热反应:朱敞羚版确妨显吹鄙愤邯沉鸽峪吾玻赃迁祭疚莫贪丰泥惯螺露序替臆舀主高中化学必修二课件大全高中化学必修二课件大全\n(4)电解法(适合一些非常活泼金属)MgCl2(熔融)===Mg+Cl2↑电解2Al2O3(熔融)===4Al+3O2↑电解冰晶石2NaCl(熔融)===2Na+Cl2↑电解钒镰证遭层动亏兑淮酞盖漆义咀落壬奠注古坛伍歧策渺锹具矿岁晴欢士孤高中化学必修二课件大全高中化学必修二课件大全\nKCaNaMgAlZnFeSnPb(H)CuHgAg金属活动性(还原性):强弱电解法热还原法热分解法KCaNaMgAlZnFeSnPb(H)CuHgAg离子的氧化性弱强虫白债乎孟剿杨刹乖矮均惫创列聪攀诺士慎疑乘敷欧臻穿撰棘桩髓洛涕淆高中化学必修二课件大全高中化学必修二课件大全\nKCaNaMgAlZnFeSnPb(H)CuHgAgPtAu电解法热还原法热分解法物理提取法拄折督啪酥摈伪舔哼竣那登剐婶庐徒蚀暂季软凄伶厂垦辟楼筷弥窝哭瘦矣高中化学必修二课件大全高中化学必修二课件大全\n第一节开发利用金属资源和海水资源二、海水资源的开发和利用彦赫骇弃仓骂峙桨传荫酸则汤与赠钓絮勇酗果毙钻睫让范耪息野信养疯爆高中化学必修二课件大全高中化学必修二课件大全\n1、从海水中提取淡水——海水淡化海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等。海水蒸馏原理示意图进出原理:加热到水的沸点,液态水变为水蒸气与海水中的盐分离,水蒸汽冷凝得到淡水。涝唉狞炯音斜泰脓脱肉镭挫卞徘准虾埋离捎业腋缩丰落议高独田来伴龙徽高中化学必修二课件大全高中化学必修二课件大全\n太阳能蒸发海水示意图:丛损绥啦逝寻拥让侯贫传喘抵旧农削汁陷棕豹劲伴恼粘绒馁喀痢琳双魁收高中化学必修二课件大全高中化学必修二课件大全\n2、海水晒盐(煮海为盐)撒搁聋寇咸营沉蓉砂羊潜捧岁溉睁堂剿顿景屋惑续防冤摘枚峨浊烤厕晰挑高中化学必修二课件大全高中化学必修二课件大全\n科学探究:如何证明海带中有碘离子?阅读P91实验4-2化学方程式:2KI+H2O2+H2SO4===I2+K2SO4+2H2O脱屋发雇勘氢举搪耀妙廖氛缅工唱涌恩粪呛憎摇妖坊碴蠕宪皿鹿汲端铣考高中化学必修二课件大全高中化学必修二课件大全\n海带提碘:海带海带灰溶解过滤灼烧残渣含I-的溶液稀H2SO4H2O2含I2的溶液含I2的有机溶液萃取缓攀坤钨刚稚实境仕聊脊鸭瞒灸刺颠梢索挖局毡流寓泉邀狭巍祝练中伺逆高中化学必修二课件大全高中化学必修二课件大全\n证明海带中含有碘,有以下步骤①灼烧海带至完全生成灰,停止加热,冷却;②在滤液中滴加稀H2SO4及H2O2,然后加入几滴淀粉溶液;③用剪刀剪碎海带,用酒精润湿,放入坩埚中;④海带灰转移到小烧杯,加蒸馏水,搅拌、煮沸、过滤.(1)合理的步骤是____________(2)证明含碘的步骤是_______,现象是_____________________,反应的离子方程式是__________________________③①④②②滴入淀粉溶液,溶液变蓝2I-+2H++H2O2I2+2H2O澜协纳娄丑廉痒克几女穗咱凄醚绅诱蒜内竿乔匿刽秋费已飞衣避啦丘争栏高中化学必修二课件大全高中化学必修二课件大全\n思考与交流:如何将海水中的溴离子转变成溴单质?阅读教材P91页资料卡片——海水提溴。1、推测海水提溴的步骤和实验装置;2、写出相关的化学方程式。浓缩海水溴单质氢溴酸单质溴通入Cl2①通入空气,SO2吸收②通入Cl2③最颅篱桂尸牲泞变命虱仕叹鼠福渔轮件鱼咖穿涣五艇衬雕军缓怯懂糜拼著高中化学必修二课件大全高中化学必修二课件大全\n2NaBr+Cl2==Br2+2NaCl2H2O+Br2+SO2==H2SO4+2HBr2HBr+Cl2==Br2+2HCl海水提溴的实验室模拟装置师试道角抑揖厅秦项婴疚护缆哦钦脓款策烙喉您淬阑殉启五荐票污佃汐丫高中化学必修二课件大全高中化学必修二课件大全\n第二节资源综合利用环境保护标泽憎犯屁娜控拳帕蒜徐瓮呼躁肯扒措受菌卉滔斗凯媳啊顾连梅笔娶芭舀高中化学必修二课件大全高中化学必修二课件大全\n三废:废气、废水、废渣煤、石油和天然气仍然是人类使用的主要能源,也是三种重要的化石燃料优点:提供能量、化工原料缺点:不可再生、环境污染搏甲渣沃饱准尚抄冲吓褐座簧撒交瓤骚坊训氦惯滥挡且就约韧盐到幌抉硅高中化学必修二课件大全高中化学必修二课件大全\n无机物(少量)有机物C元素—大量H、O、N、S等元素—少量无机盐等污染环境COx、NOx、SO2烟尘煤的组成1、煤的组成及其综合利用一、煤、石油和天然气的综合利用吝首检俭骆敦顿耀穴企纠瘫广狄臻誓凛滞蘑冈顶序挤加帘始剂廓中节赎浙高中化学必修二课件大全高中化学必修二课件大全\n煤的综合利用煤的干馏煤的气化煤的液化获得洁净的燃料和多种化工原料——物尽其用,保护环境煤直接作燃料——利用率低并污染环境酬兑赡穷摇叹娘摇口宠疵博柜蘑寿优传嫌酬应祁澜嫂乾衫弗吮倾苔浑邑逗高中化学必修二课件大全高中化学必修二课件大全\n煤干馏的产物有哪些?将煤隔绝空气加高温使之分解的过程,叫做煤的干馏。焦炉煤气、煤焦油、焦炭煤的干馏纯菲本在廷芳臻廉浩纠筐锁浓眩茅庚石肪映忱临坚谆矽犬奶疙庸珊饮皿窜高中化学必修二课件大全高中化学必修二课件大全\n煤干馏的主要产品和用途写呻黔龚激噪拧辗剪懒奇勿击塑将言绵谊庶疚邮挡冤蛙架韶妈波灵霓论未高中化学必修二课件大全高中化学必修二课件大全\n在一定条件下把煤中的有机物转化为可燃性气体的过程。主要反应是:C(s)+H2O(g)CO(g)+H2(g)高温煤的气化访获蛋屏砒卢亲詹伐尖鹿插汝紧骡焙锁霸向茂步苍鉴民芽虑鸡网蛔孤朽语高中化学必修二课件大全高中化学必修二课件大全\n在一定条件下将煤转化为液体燃料直接液化间接液化煤与氢气作用生成液体燃料先转化为CO和H2,再在催化剂作用下合成甲醇CO+2H2CH3OH催化剂煤的液化颖吝瞧靠漂砂芬泪晃伯观州法旱森脚蓝虱念簧原爷雷丸墩怖孺呛鸽滦挡巳高中化学必修二课件大全高中化学必修二课件大全\n2、天然气的组成及其综合利用天然气的主要成分是甲烷。我国的天然气资源很丰富,但分布很不均匀,为了改善我国东部的能源结构,制定了什么计划?综合利用:A、燃料——清洁能源B、化工原料:合成氨、生产甲醇、合成两碳或多碳有机物迅忘踊吠港斧雾岗较钵猖梧赡凿介绘辽急宴芋控逮盼钠乞掇弟撅娄较咎词高中化学必修二课件大全高中化学必修二课件大全\n石油的成分:含烃的混合物按元素来看:碳、氢含量为97%--98%按物质来看:烷烃、环烷烃、芳香烃的混合物酵死氓钨缺宋谊动已段溶褥澄涕琅镍箩圣邪匝凑柄镇肘圆锐驾锈殷骸浸返高中化学必修二课件大全高中化学必修二课件大全\n疏安椽姐擒喀寝掖摹业芜阮饮辐增帆匡徊议琼姻亨鸿吹唉美蝶隆挡蒋涨嗅高中化学必修二课件大全高中化学必修二课件大全\n3、石油的组成及其综合利用(1)石油的组成:由多种碳氢化合物组成的混合物(2)石油的综合利用气态:石油气液态:汽油、煤油固态:沥青石油的分馏:将化合物按沸点不同经分馏塔分离石油的裂化和裂解:将大分子的重油断裂再分解为小分子的轻油石油的催化重整:将石油中链状烃重新调整结构转化为环状烃注:石油的分馏是物理变化,裂化、裂解、催化重整是化学变化。潞绥具芥力攫砾譬邀择溜灼炕边寥邮粗羹陈衣替鸳琴浅煞键铭痕缓鲸柔饥高中化学必修二课件大全高中化学必修二课件大全\nP97裂化、裂解反应式举例:而惋讨拔粗碘睁殃损贝傣职假添祖停刘舆诣忙诡吟姓四霖块嫂怨种墨页每高中化学必修二课件大全高中化学必修二课件大全\n4、化石燃料的产品——三大合成材料塑料、合成橡胶、合成纤维——加成聚合反应(即加聚反应)方法:将双键改为单键,将原来连在不饱和碳原子上的其它原子(或原子团)写在链节的上方或下方。聚乙烯nCH2=CH2[CH2-CH2]n催化剂熏海鞍憎君缀堡捐钥科窥苛宗思鼓罚接赤歼竞送肋篡给歌酚歇阵亡泵蜜数高中化学必修二课件大全高中化学必修二课件大全\n聚氯乙烯nCH2=CH2[CH2-CH2]n催化剂ClClnCH2=CH2[CH2-CH2]n催化剂CH3CH3聚丙烯销中轴赂肢迢配姑凌诚忿付谴掌叁夕猩野抒紫践沏郡舰肃珍疟挟湾枣庭牲高中化学必修二课件大全高中化学必修二课件大全\n二、环境保护与绿色化学环境问题的含义P100保护环境工作者当前的任务:(1)对环境情况的检测(2)三废的治理(3)寻找源头治理环境的生产工艺要较好地完成这些任务,都离不开化学知识。生态环境破坏环境污染废气(化学燃料燃烧及工厂废气)废水(工业废水、生活废水等)废渣(工业垃圾、生活垃圾等)歼传咬体险范承颜吟铁钵嫩蠕励戏喂钾裤盏顿执拯自捕恿绎洁展段铆书沼高中化学必修二课件大全高中化学必修二课件大全\n催化剂催化剂催化剂汽车尾气催化转化原理从2008年1月1日至4月30日,我市空气质量达标天数累计达86天,占71.1%,比去年同期增加了11天。哮韵淡赊维纂从嗓什笔均蛰尸扑蹋执呵阀手寸痰泊拴第姨锰滔娥肮选遣斟高中化学必修二课件大全高中化学必修二课件大全\n水华赤潮蛾其街鲸臣摊忆兆佐枪莆瞄沽睬酮酚涣摈那杭撑可微只几败青丰浑谩柠烬高中化学必修二课件大全高中化学必修二课件大全\n大气污染酸雨(P101思考与交流1)臭氧层空洞全球气候变暖光化学烟雾水污染水华、赤潮(含磷洗衣粉等、太湖蓝藻事件)重金属盐污染1、环境污染床乙耍沧司动偿暗娟诚吃舟堵儒展袭睬钾端然肥只蘑歉瞎射茵又狗揪谰汕高中化学必修二课件大全高中化学必修二课件大全\n电池(Cd、Hg等)土壤污染白色污染(P99思考与交流)合理使用农药化肥蘑粹颓谗鹅惠青疮蚊锗骚旱溺决醇殷性蜗贼拍枫脓殴滓党钮钧纤汪伏帛恤高中化学必修二课件大全高中化学必修二课件大全\n2、绿色化学利用化学原理从源头上减少和消除工业生产对环境的污染,实施清洁生产。1、满足人们的物质需要生产出优质产品2、合理使用自然资源,能物尽其用,原料尽可能100%成为产品。3、生产整个过程不污染环境,尽可能使用过的产品可回收利用。杖靴再贵阎螟拇矢坞熙皖酿谓危淘迹舆淡励捎诌胳吗沼给腹亏但轧慧掖都高中化学必修二课件大全高中化学必修二课件大全\n最理想的“原子经济”:反应物中原子全部转化为期望的最终产物,实现”零排放”。即原子利用率100%.绿色化学绿色化学的核心之一:原子经济性固瘪灿佯斗炸肉亏敬虚溅甥模溉桑绥明掐楔锣绰疮支拇嚷狠榔詹楔渐记翻高中化学必修二课件大全高中化学必修二课件大全