- 190.00 KB
- 2022-08-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
第三节
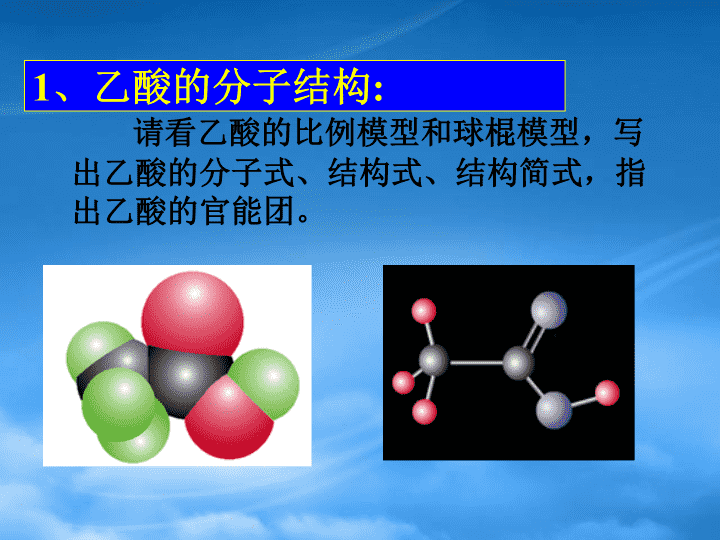
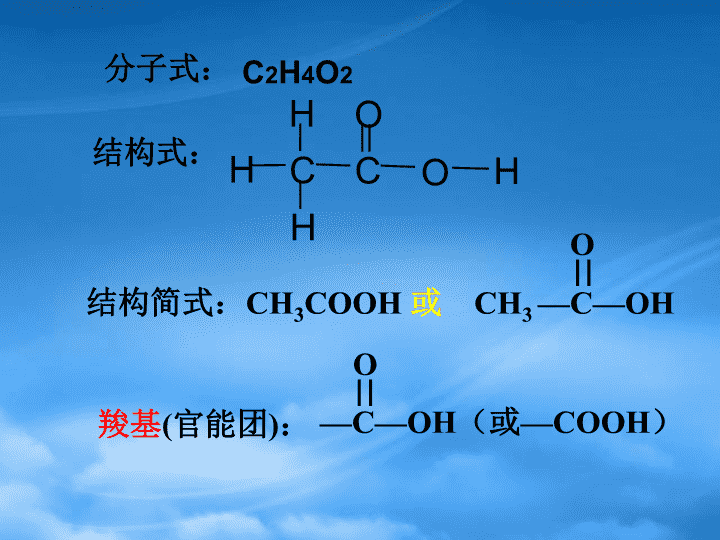
生活中两种常见的有机物二、乙酸\n1、乙酸的分子结构:请看乙酸的比例模型和球棍模型,写出乙酸的分子式、结构式、结构简式,指出乙酸的官能团。\n结构式:CHHHHCOO结构简式:羧基(官能团):分子式:C2H4O2CH3COOH或CH3—C—OHO—C—OH(或—COOH)O\n2、乙酸的物理性质:易溶于水、酒精等无色液体,熔点16.6℃,沸点117.9℃,可凝结成冰状晶体易挥发,有刺激性气味无水乙酸——冰醋酸请观察乙酸的试剂瓶和标签\n酸性:请同学们回忆酸的通性:与碱性氧化物反应与盐反应与碱反应使酸碱指示剂变色与活泼金属反应\n3、乙酸的化学性质(1)弱酸性:CH3COOHCH3COO-+H+NaOH+CH3COOHCH3COONa+H2OMg+2CH3COOH(CH3COO)2Mg+H2↑CuO+2CH3COOH(CH3COO)2Cu+H2ONa2CO3+2CH3COOH2CH3COONa+CO2↑+H2O使紫色石蕊溶液变红,酚酞不变色\nP75科学探究1、这利用了乙酸的什么性质?通过这个事实你能比较醋酸和碳酸的酸性强弱吗?CaCO3+2CH3COOH(CH3COO)2Ca+CO2↑+H2OCaCO3+2CH3COOH2CH3COO-+Ca2++CO2↑+H2O能,酸性:CH3COOH>H2CO3\n2、设计实验。目的:原理:药品和仪器:实验步骤:实验现象:方程式:比较醋酸和碳酸的酸性强酸制弱酸有大量气泡生成Na2CO3+2CH3COOH2CH3COONa+CO2↑+H2OP75科学探究?\n(2)乙酸的酯化反应乙酸、乙醇、浓硫酸的混合物饱和Na2CO3溶液阅读P75实验3-4\n现象:酯化反应:酸跟醇作用,生成酯和水的反应.浓H2SO4CH3COOH+HOC2H5CH3COOC2H5+H2O乙酸乙酯溶液分层,上层有无色透明的油状液体产生,并有香味\n酯化反应的注意事项(1)浓H2SO4的作用是脱水剂和催化剂(2)试管要与桌面成45°角,且试管中的液体不能超过试管体积的三分之一(3)导气管兼起冷凝和导气作用(4)导气管不能伸入碳酸钠液面以下,以防喷出和倒吸(5)饱和Na2CO3溶液的作用①中和乙酸、溶解乙醇杂质;②冷凝酯蒸气;③由于乙酸乙酯在该溶液中的溶解度较小,有利于乙酸乙酯析出__________________________\n同位素原子示踪法判断酯化反应的本质。【问题与讨论】酯化反应反应时,脱水可能有几种方式?提示:如果用乙酸跟含18O的乙醇起反应,可发现生成物中乙酸乙酯分子中含有18O原子。1818断键方式:酸脱羟基(-OH)醇脱氢(H)酯化反应又属于取代反应。\nOCH3—C—O—H酸性酯化反应小结:\n某有机物的结构为,它最不可能具有的性质是()。A.能与金属钠反应放出H2B.既能与C2H5OH发生酯化反应也能与CH3COOH发生酯化反应C.能发生加聚反应D.水溶液能使紫色石蕊试纸变红C\n