- 3.66 MB
- 2022-08-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
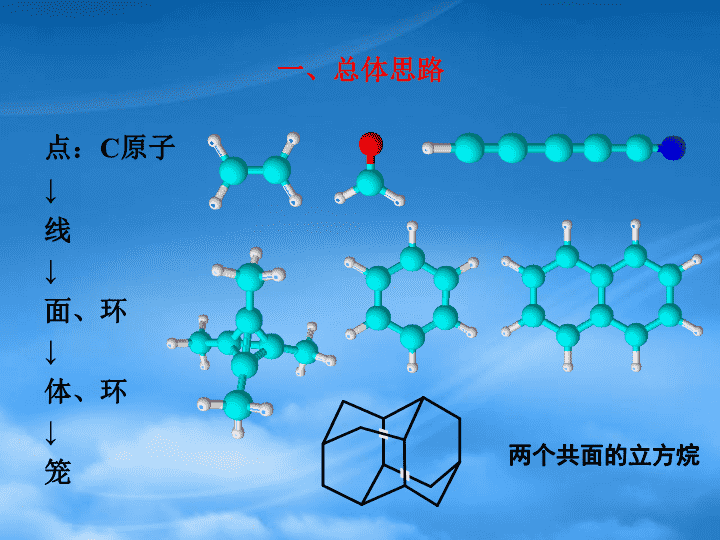
有机化学序言有机物结构基础\n一、总体思路点:C原子↓线↓面、环↓体、环↓笼两个共面的立方烷\nσ键和π键的比较σ键π键成键方向电子云形状牢固程度成键判断规律“头碰头”“肩并肩”轴对称镜像对称强度大,不易断裂强度较小,易断裂共价单键是键,共价双键中一个是键,另一个是键,共价三键中一个是键,另两个为键σσπσπ\n\n二、三种不同杂化状态的碳原子1、sp3杂化\n二、三种不同杂化状态的碳原子1、sp3杂化\n二、三种不同杂化状态的碳原子1个未杂化的P轨道\n二、三种不同杂化状态的碳原子2、sp2杂化\n二、三种不同杂化状态的碳原子2、sp2杂化\n二、三种不同杂化状态的碳原子3、sp杂化\n二、三种不同杂化状态的碳原子3、sp杂化\n二、三种不同杂化状态的碳原子3、sp杂化\n三、三种典型的成键方式1、共轭烯烃所有的原子在同一个平面上,C(SP2)一C(SP2)\n三、三种典型的成键方式特殊:丙二烯相互垂直\n三、三种典型的成键方式2、苯环\n三、三种典型的成键方式2、苯环\n四、四种典型的碳碳键的比较1、C-C2、C=C3、C三C4、苯环中的C~Ca是原子数,b是电子数。\n\n中心原子采取sp2杂化,还有一个未参加杂化的p轨道是与分子所在平面垂直。氧原子上有一个p轨道与碳原子的上p轨道互相平行,形成一个π键。甲醛分子中的π键\n