- 21.20 MB
- 2022-08-08 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
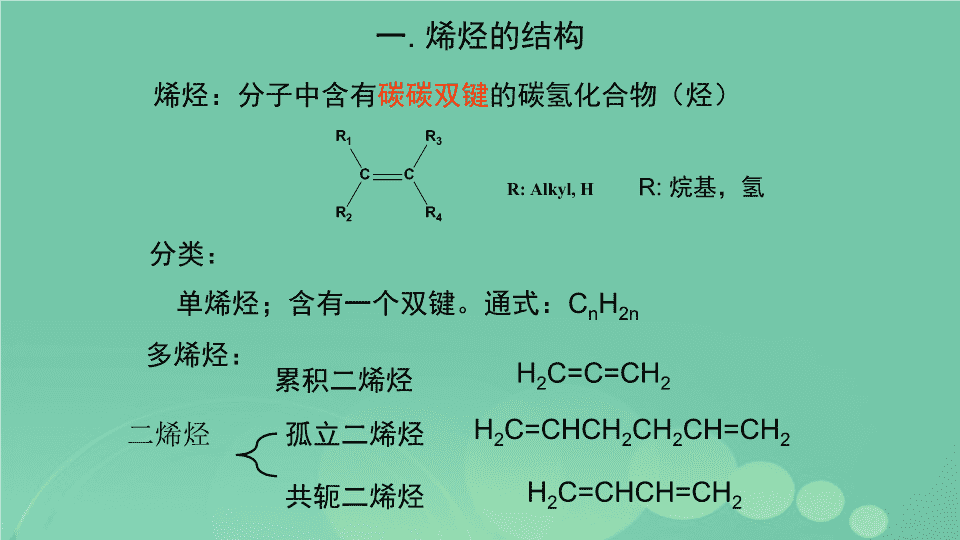
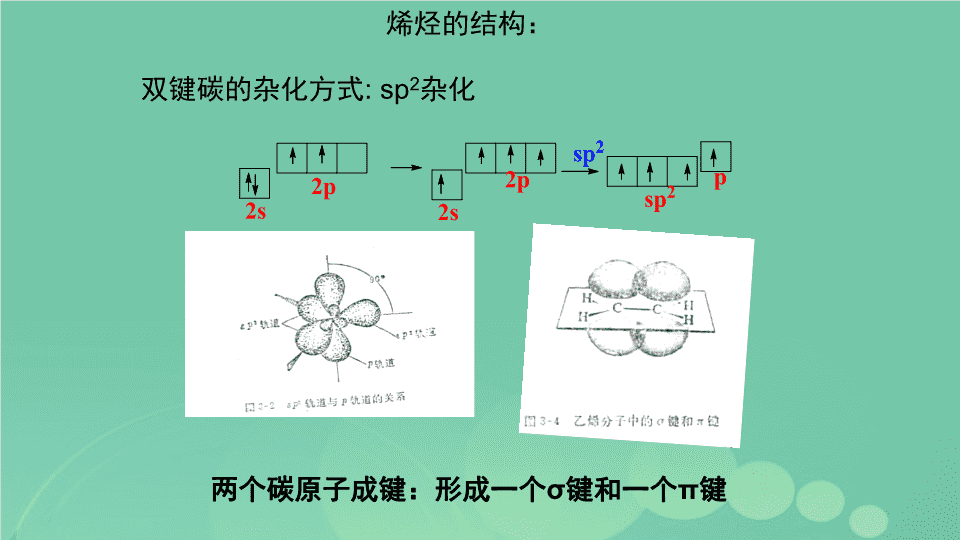
烯烃\n一.烯烃的结构烯烃:分子中含有碳碳双键的碳氢化合物(烃)R:烷基,氢分类:单烯烃;含有一个双键。通式:CnH2n多烯烃:二烯烃累积二烯烃H2C=C=CH2孤立二烯烃H2C=CHCH2CH2CH=CH2共轭二烯烃H2C=CHCH=CH2\n烯烃的结构:双键碳的杂化方式:sp2杂化两个碳原子成键:形成一个σ键和一个π键\n两个碳原子之间增加了一个Π键,也增加原子核对电子的吸引力,使碳原子间靠的更近,键长比单键键长短Π键是由两个p轨道侧面重叠而成,重叠的程度比σ键小的多,所以Π键比较容易破裂Π键的电子云分散在平面的两侧,原子核对Π电子的束缚力较小,具有较大的流动性,比较容易激化,而发生反应Π键没有轴对称,以双键相连的两个原子之间,不能自由旋转\n二.烯烃的同分异构和命名1.构造异构:包括碳链异构和双键的位置异构。例如:C5H10碳链异构:官能团位置异构:戊烯2-甲基-1-丁烯3-甲基-1-丁烯2-戊烯2-甲基-2-丁烯\n2.顺反异构(立体异构)\n顺反异构(立体异构):由于双键旋转受阻,构造相同的分子中的原子在空间排列方式的不同所造成的异构现象顺-2-丁烯反-2-丁烯一般反式异构体比较稳定:反-2-丁烯比顺-2-丁烯稳定4.6kJ/mol\n3.命名选择包含C=C双键在内的最长碳链为主链,命名为“某”烯从靠近双键的一端起编号双键的位次必须表明,只写出双键两个原子中位次较小的一个,放在烯烃名称的前面其他同烷烃的命名原则2,4-二甲基-2-己烯3-甲基-2-乙基-1-丁烯\n若分子中两个双键碳原子均与不同的基团相连,这时会产生两个立体异构体,可以采用Z、E构型来标示这两个立体异构体。即按顺序规则,两个双键碳原子上的两个顺序在前(大)的原子(或基团)同在双键一侧的为Z构型;在两侧的为E构型。E.顺反异构体命名。曾采用顺、反来标示双键的构型,规定连在两个双键碳原子上的相同或相似的基团处于双键同侧称为顺,处在双键异侧称为反。由于该法在判断相似基团时会出现一些混淆,现在大都采用Z、E构型标示\nZ-2,2,5-三甲基-3-己烯E-5-甲基-3-丙基-2-庚烯\n3-溴-丙烯2-戊烯2-甲基-3-(2-氯乙基)-1,4-二氯-E-3-辛烯4-甲基-3,7-二氯-Z-烯丙基溴\n4E-2-甲基4-乙基-2,4-己二烯下列基团的先后次序\n烯基烯烃去掉一个氢原子,称为某烯基(−enyl)。烯基的编号从带有自由价(freevalence)的碳原子开始,烯基的英文名称用词尾“enyl”\n三、烯烃的物理性质烯烃的物理性质与烷烃很相似。1.随着分子量的增加,烯烃的沸点和熔点升高3.一些烯烃分子具有较小的极性,这主要是由于烯键碳原子和烷基取代基碳原子的杂化轨道电负性不相等。spn杂化轨道中,n越小,s轨道成分大,电负性就大:s>sp>sp2>sp3>p2.难溶于水,易溶于有机溶剂。\nbp:3.7°Cmp:-138.9°Cbp:0.9°Cmp:-105.5°Cμ=0μ=0.33Dμ=0μ=0.33D\n四、烯烃的化学性质烯烃的结构:烯烃的双键是由一个σ键和一个π键组成。\n加成反应氧化反应、聚合反应α-氢的卤化反应四、烯烃的化学性质\n4.1烯烃的亲电加成反应烯烃的Π电子容易给出,受亲电试剂的进攻,发生亲电加成反应亲电试剂:缺电子的物种。例如:H+,正离子,lewis酸1.与卤素的加成邻二卤代烃\n这类反应可以用来检验烯烃和其他的不饱和化合物的存在4-甲基-2-戊烯4-甲基-2,3-溴戊烷\n烯烃与溴在不同介质中的反应结果b.反应分两步进行、形成正离子中间体为反应的诀速步骤一些典型烯烃加成的相对反应速率烯烃H2C=CH2CH3CH=CH2(CH3)2C=CH2BrCH=CH2相对速率123<0.04(烷基:供电子取代基)a.反应是亲电加成\n反应机理:产物是反式加成产物Π-络合物环状溴鎓离子c.反式加成\n反应机理:亲电加成、通过环正离子中间体、反应分两步进行的反式加成。B.与氯反应卤素作为亲电试剂的活性顺序:F2〉Cl2〉Br2〉I23,3-二甲基-1-丁烯3,3-二甲基-1,2-二氯丁烷ICl,IBr可以作为亲电试剂氟太活泼,反应剧烈,放出大量的热,使烯烃分解;碘与烯烃不发生离子型反应。\n2.与卤化氢加成(卤化氢气体或发烟氢卤酸)反应溶剂:中等极性的溶剂,如冰醋酸HX对烯烃的加成活性顺序:HI>HBr>HCl\n?区域选择性(Regio-selectivity):键的形成或断裂有两种以上取向而主要有一种产物生成。马尔科夫尼科夫(Markovnikov)规则:卤化氢等极性试剂与不对称烯烃的离子型加成反应,酸中的氢原子加在含氢较多的双键碳原子上,卤素或其他原子加在含氢较少的双键碳原子上。\n反应机理:??碳正离子\n碳正离子的稳定性:\n碳正离子的稳定性:电荷愈分散,碳正离子的稳定性愈强碳正离子的结构:sp2杂化方式a.诱导效应:烷基碳为sp3,供电子效应\n诱导效应:分子中引入一个原子或基团后,使分子中的电子云密度分布发生变化,而这种变化不但发生在直接部分部分,也可以影响到不相连的部分,这种因某一原子或基团的极性,σ键的电子沿着原子链向某一方向移动的效应称为诱导效应。诱导效应是指σ电子的偏移。\nb.共轭效应:σ-p超共轭,σ-Π超共轭超共轭效应的电子转移的取向:\n超共轭的大小,与p轨道或Π轨道相邻的碳上的C-H键的多少有关,C-H键越多,超共轭效应越大超共轭效应的大小:CH3->RCH2->R2CH->R3C-自由基的稳定顺序:自由基的碳为sp2杂化方式\n影响卤化氢与不同烯烃加成反应的反应因素:a.烯烃双键碳上烷基取代基越多,反应活性越高CH3CH=CHCH3CH3CH=CH2CH2=CH2>>b.双键碳上带有吸电子取代基集团,如CF3、NO2、CN、COOH等,这些吸电子基降低双键碳原子上的电荷密度,也降低了碳正离子的稳定性,使亲电加成反应变难。\n反马氏规则产物C.双键碳上含有X、O、N等具有孤对电子对的原子或基团时1.取代基为卤原子时(吸电子诱导效应和给电子共轭效应),吸电子诱导效应大于给电子共轭效应,降低了烯烃的反应活性。马氏规则产物\n2.取代基为含O、N原子的集团(OH、OR、OCOR、NR2、NHR、NHCOR)时,吸电子诱导效应小于给电子共轭效应,增加了双键的电子云密度,加快了反应活性。马氏规则产物一般烯烃的反应活性:R2NCH=CH2,ROCH=CH2〉RCH=CH2〉CH2=CH2〉XCH=CH2〉O2NCH=CH2\n烷基迁移负氢迁移碳正离子重排:\n写出HI与下列各化合物反应的主要产物:\n3.与硫酸反应烯烃和冷硫酸混合,在室温下就能发生反应,生成透明的硫酸氢酯溶液,加水稀释,加热水解可得到相应的醇。硫酸氢乙酯工业上常用种方法制备乙醇、异丙醇、叔丁醇\n4.在酸催化下与水反应烯烃在酸的催化下也可以直接加水生成醇。5.与有机酸、醇、酚反应300oC,7MPa强的有机酸较容易与烯烃发生反应;而弱的有机酸、醇、酚只有在强酸(H2SO4,TsOH,HBF4)的催化下,才能发生加成反应.乙酸乙酯叔丁醇甲醚\n写出下列反应的反应机理:\n6.与次卤酸(HOX)的反应氯或溴在稀水溶液中或碱性稀水溶液中与烯烃发生加成反应,得到β-卤代醇。1-氯-2-丙醇\n7.与乙硼烷的加成反应(硼氢化反应)乙硼烷:无色、有毒、气体,在空气中可以自然三烷基硼烷反马氏加成产物\n顺式加成一级醇不经过碳正离子中间体\n4.2自由基加成反应过氧化物反马氏加成产物链引发链增长链终止HCl,HI不能进行自由基加成反应。\n4.3烯烃的氧化反应1.环氧化反应常用过氧酸:过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸等。环氧乙烷\n2.用KMnO4,OsO4氧化碱性或中性顺式二醇酮酸在这反应中,高锰酸钾溶液的紫色退去,生成棕褐色二氧化锰沉淀,可以用来鉴定不饱和烃\n3.臭氧氧化烯烃溶剂在惰性溶剂中,在低温下通入臭氧,可发生加成反应,生成臭氧化物,经进一步处理,分解成醛、酮。臭氧化物易爆炸,不分离\n有A,B两个化合物,其分子式都为C6H12,A经臭氧化,并与锌和酸反应后得乙醛和甲基乙基酮;B经高锰酸钾氧化后只得到丙酸,请写出A,B的结构式\n4、加氢反应催化剂催化剂(catalyst):Pt、Pd、Ni等过渡金属——非均相催化剂[(C6H5)3P]3RhCl等——均相催化剂a.催化剂表面积的增大,有利于氢化反应。(过渡金属固定在有较大表面积的载体上,如:活性碳、Al2O3等)Pt/C,Pd/C,RaneyNi等b.加氢反应多数为顺式加成;C.碳碳双键上取代基越多,空间阻碍越大,越不易被催化剂吸附,氢化速率越小。\n在顺反异构体中反式异构体比顺式稳定。氢化热:顺>反顺-2-丁烯(118.9kJ·mol-1)>反-2-丁烯(114.7kJ·mol-1)烯烃的加氢反应是放热反应.氢化热:1mol烯烃与氢气加成所放出的热量。(催化剂的加入不改变烯烃的氢化热)氢化热越小,烯烃越稳定烯烃的稳定性\n比较三种烯烃异构体的氢化热氢化热:2-甲基2-丁烯<2-甲基1-丁烯<3-甲基1-丁烯稳定性顺序:2-甲基2-丁烯〉2-甲基1-丁烯〉3-甲基1-丁烯因此,烯烃双键上烷基取代基越多,氢化热越小,烯烃越稳定。\n由于σ-Π的超共轭效应4.5烯烃的聚合反应烯烃在引发剂或催化剂作用下,双键断裂而相互加成,得到长链的大分子或高分子的化合物。单体聚合物或高聚物聚合度\n4.6烯烃的α-氢的卤化反应机理:(自由基反应)烯丙基自由基\nα-溴代反应通常采用N-溴代丁二酰亚胺(简称NBS)为溴化剂,该反应可以在较低温度下,在光或引发剂的作用下进行。\n五、烯烃的制备1.醇失水84%少量\n2.卤代烷失去卤化氢3.邻二卤代烃失卤素