- 804.50 KB
- 2022-08-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
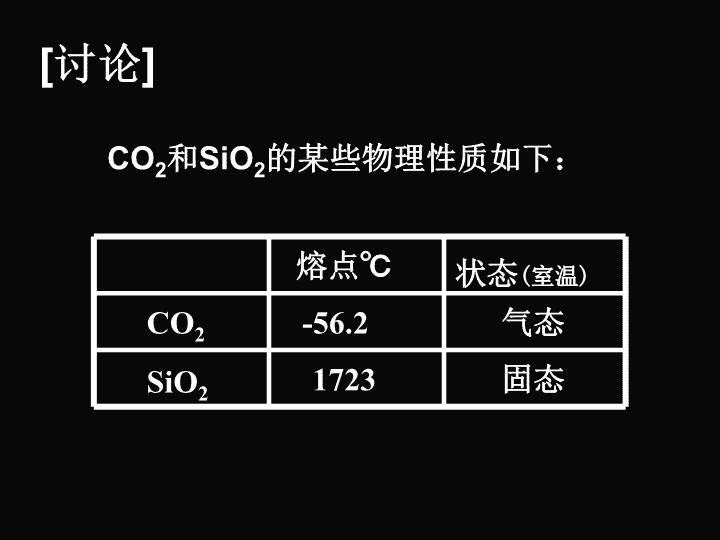
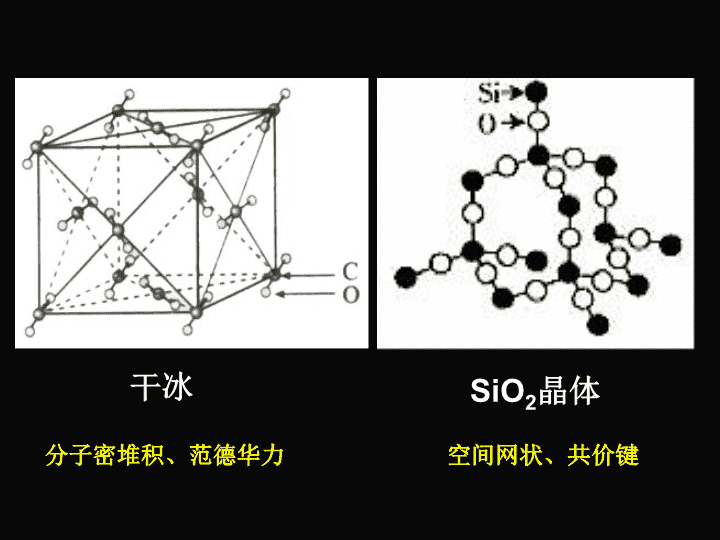
复习提问:1.典型的分子晶体有哪些?2.分子晶体的物理性质?3.分子晶体中粒子的堆积方式如何?\n[讨论]CO2和SiO2的某些物理性质如下:CO2SiO2熔点℃状态(室温)-56.21723气态固态\nSiO2晶体干冰分子密堆积、范德华力空间网状、共价键\n1.概念:2.构成微粒:3.作用力:原子晶体原子间以共价键相结合而形成的空间立体网状结构的晶体。原子共价键原子晶体熔化破坏的是共价键。一般的,原子间键长越短,键能越大,共价键越稳定,物质的熔沸点越高,硬度越大。共价晶体\n4.原子晶体的物理特性熔、沸点:很高硬度:很大导电性:一般不导电溶解性:难溶于一些常见的溶剂在原子晶体中,原子间以较强的共价键相结合而且形成空间立体网状结构\n5.常见的原子晶体(1)某些非金属单质:金刚石(C)、晶体硅(Si)、晶体硼(B)、晶体锗(Ge)等(2)某些非金属化合物:碳化硅(SiC)晶体、氮化硼(BN)晶体(3)某些氧化物:二氧化硅(SiO2)晶体、Al2O3(天然)\n对比分子晶体和原子晶体的物理参数\n6.原子晶体的结构模型:键角:109º28´键长:0.155nm金刚石①碳原子采取SP3杂化,每5个碳原子形成正四面体金刚石晶胞\n[讨论]①在金刚石晶体中,每个C与()个C成键,形成()结构;最小碳环由()个C原子组成且六原子()同一平面内.②在金刚石晶体中,C原子个数与C—C键数之比为()正四面体6不在41:2\n金刚石晶胞[讨论]③12克金刚石中,含C—C键数为()NA⑤每个C原子被个六元环共有?④每个C—C键被()个六元环共有。2126\nC42×2=12\n晶体Si晶体SiO2SiO2晶胞\n①在SiO2晶体中,每个Si原子与4个O原子结合,构成空间正四面体结构,Si位于四面体中心,O位于四面体顶点;②在SiO2晶体中,Si原子与O原子个数比为()【讨论】1:2晶体SiO2\n③在SiO2晶体中,最小的环为()个Si和()个O组成的()环。6十二元6④晶体中的最小环为十二元环,含有个Si-O键;每个Si-O键被个十二元环共有.126⑤每个O原子被个十二元环共有,每个Si原子被个十二元环共有.612晶体SiO2\n因为CO2是分子晶体,SiO2是原子晶体,所以熔化时CO2是破坏范德华力而SiO2是破坏化学键,所以SiO2熔沸点高。而破坏CO2分子,都是破坏共价键,而C—O键能>Si-O键能,所以CO2分子更稳定。为何CO2熔沸点低?而破坏CO2分子却比SiO2更难?\n(4)依据硬度和机械性能判断:原子晶体、分子晶体判断方法(1)依据组成晶体的粒子和粒子间的作用判断(2)记忆常见的、典型的原子晶体。(3)依据晶体的熔点判断:\n一种结晶形碳,有天然出产的矿物。铁黑色至深钢灰色。质软具滑腻感,可沾污手指成灰黑色。有金属光泽。六方晶系,成叶片状、鳞片状和致密块状。密度2.25g/cm3,化学性质不活泼。具有耐腐蚀性,在空气或氧气中强热可以燃烧生成二氧化碳。石墨可用作润滑剂,并用于制造坩锅、电极、铅笔芯等。知识拓展-石墨\n石墨过渡(混合)晶体易导电?\n(1)石墨分层,层间为范德华力,层内C原子通过共价键结合。(2)石墨晶体中最小环为六元环,键角120°平均每个环中含有2个C原子,3个C-C键;各层之间是范德华力结合,容易滑动,所以石墨很软。石墨属于混合型晶体\n石墨中r(C-C)比金刚石中r(C-C)短(大π键)\n石墨1、石墨为什么很软?2、石墨的熔沸点为什么很高(高于金刚石)?3、石墨属于哪类晶体?为什么?石墨为层状结构,各层之间是范德华力结合,容易滑动,所以石墨很软。石墨各层均为平面网状结构,碳原子之间存在很强的共价键(大π键),故熔沸点很高。石墨为混合键型晶体。\n例、如右图所示,在石墨晶体的层状结构中,每一个最小的碳环完全拥有碳原子数为___,每个C完全拥有C-C数为___石墨中C-C夹角为120☉,C-C键长为1.42×10-10m层间距3.35×10-10m23∕2\n1.下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是()(A)SO2和SiO2(B)CO2和H2O(C)NaCl和HCl(D)CCl4和KCl2.下列各组物质气化或熔化时,所克服的微粒间的作用(力),属同种类型的是()(A)碘和干冰的升华(B)二氧化硅和生石灰的熔化(C)氯化钠和铁的熔化(D)水和四氯化碳的蒸发BAD\n5.根据下表给出的几种物质的熔点、沸点数据判断说法中错误的是[]A.SiCl4是分子晶体B.MgCl2中键的强度比NaCl中键的强度小C.单质R是原子晶体D.AlCl3为离子晶体BD\n3.下列各组物质中,按熔点由低到高排列正确的是()(A)O2、H2、Hg(B)CO2、KCl、SiO2(C)Na、K、Rb(D)SiC、NaCl、SO24.下列晶体熔化时化学键没有被破坏的是( )(A)NaCl(B)冰(C)白磷(D)SiO2BBC\nThanks!