- 1.53 MB
- 2022-08-10 发布
- 1、本文档由用户上传,淘文库整理发布,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,请立即联系网站客服。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细阅读内容确认后进行付费下载。
- 网站客服QQ:403074932
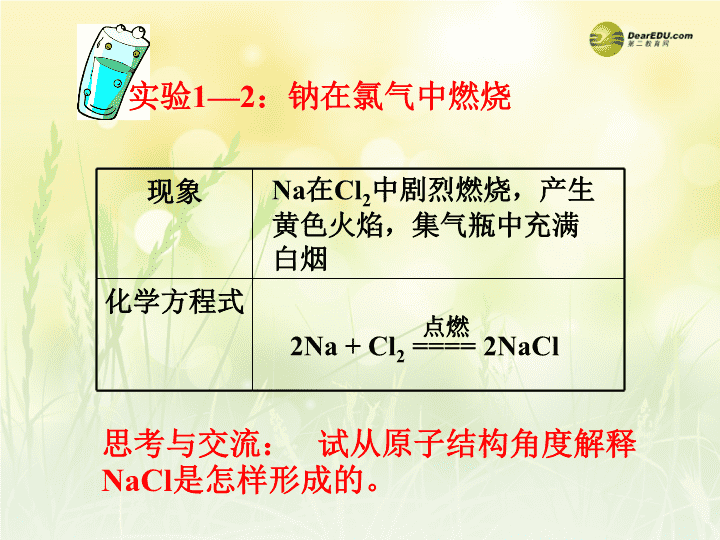
第一章物质结构元素周期表第三节化学健\n你有想过吗?1.为什么一百多种元素可形成千千万万种物质?元素的原子间通过什么作用形成如此丰富多彩的物质呢?2.物质中原子为什么总是按一定数目相结合?\n实验1—2:钠在氯气中燃烧现象化学方程式Na在Cl2中剧烈燃烧,产生黄色火焰,集气瓶中充满白烟2Na+Cl2====2NaCl点燃思考与交流:试从原子结构角度解释NaCl是怎样形成的。\nNa+Cl-电子转移氯化钠的形成过程:不稳定较稳定在氯化钠中Na+和Cl-间存在哪些作用力?1、Na+离子和Cl-离子间的相互吸引;2、电子与电子、原子核与原子核间的相互排斥作用\n\n离子键化学键——\n三、化学键1、离子键(1)定义:带相反电荷离子之间的相互作用称为离子键。(2)构成离子键的粒子:阴、阳离子(3)离子键的实质:静电作用静电引力静电斥力(4)成键条件①活泼金属和活泼非金属化合是易形成离子键。(AlCl3例外)②金属阳离子或NH4+和某些带电原子团之间能形成离子键。③类盐(NaH、CaH2等)形成的也是离子键。☆☆由离子键构成的化合物叫做离子化合物。\n在元素符号周围用“·”或“×”来表示原子最外层电子的式子,叫电子式。Na··Mg··O·····Cl·······原子的电子式:离子的电子式:Na+Ca2+[O]2-····::[Cl]-····::阳离子的电子式:简单阳离子的电子式就是它的离子符号,复杂阳离子(NH4+)例外。阴离子的电子式:不但要画出最外层电子数,而且还要用中括号“[]”括起来,并在右上角标出所带电荷“n-”。原子的电子式:在元素符号周围用小点“.”或小叉“×”来表示其最外层电子数。电子式·C···\n如何用电子式表示离子化合物的形成过程?例:用电子式表示硫化钠、溴化钙的形成过程1.原子A的电子式+原子B的电子式→化合物的电子式3.不能把“→”写成“=”。4.在箭号右边,不能把相同离子归在一起。注意2.用弧线标明电子的转移\n离子化合物的电子式:由阴、阳离子的电子式组成,但相同离子不能合并AB型AB2型A2B型书写时\n本节小结:由离子键构成的化合物一定是离子化合物区分:用电子式表示物质用电子式表示物质形成过程离子键:带相反电荷离子之间的相互作用\n课堂练习练习1、下列说法正确的是:A.离子键就是使阴、阳离子结合成化合物的静电引力B.所有金属与所有非金属原子之间都能形成离子键C.在化合物CaCl2中,两个氯离子之间也存在离子键D.钠离子与氯离子通过离子键结合形成氯化钠D\n练习2、下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合成稳定化合物的是:A.10与12B.8与17C.11与17D.6与14C\n活泼的金属元素和活泼非金属元素化合时形成离子键。请思考,非金属元素之间化合时,能形成离子键吗?为什么?不能,因非金属元素的原子均有获得电子的倾向。讨论\n请同学们动笔写出H原子和Cl原子结构示意图和电子式,两种原子怎样才能形成稳定结构呢?讨论、分析、思考:\n从微观角度分析氯化氢分子的形成过程共用电子对\n1.定义:原子之间通过共用电子对所形成的相互作用,叫做共价键。2.成键条件:同种或不同种非金属元素3.仅含有共价键的化合物是共价化合物二、共价键想一想:举几个你所熟悉的共价化合物的例子成键微粒本质\n氢分子的形成:H·氯化氢分子的形成:···Cl··:·H+→H·+→Cl····H····HH··H﹣H(结构式)H﹣Cl(结构式)4.用电子式表示物质形成过程以氯化钠和氯化氢为例,比较离子键和共价键形成过程的区别?\n没有形成阴阳离子,不需标出离子电荷、[]和电子转移。注意:\n碘用电子式表示下列共价分子的形成过程水二氧化碳氨硫化氢2·C···+···O···→﹕OCO﹕﹕﹕﹕﹕﹕﹕+→+→2H····O···﹕HOH﹕﹕﹕2H·+→﹕HSH﹕﹕﹕···S···3H·+→·N····﹕HN﹕﹕﹕HH·I····:I·····:····I··:I··::\n同种元素原子不同种元素原子原子吸引电子能力相同原子吸引电子能力不相同电子对不发生偏移成键原子不显电性电子对发生偏移成键原子显电性5.共价键的类型HH··Cl····H····极性共价键(极性键)非极性共价键(非极性键)\n反馈检测:1、下列物质中,只含有非极性共价键的是()A、NaBrB、NaCIC、Br2D、H2SCCD2、下列物质中,含有极性共价键的是()A、I2B、MgCI2C、NaOHD、H2O\n3、下列书写是否正确ABC·I····::I·····I····:I····::+→D2H·+···O···:HHO::::+﹕HSH﹕﹕﹕···S···2H·Cl[]-H+ClH\n从有关离子键和化合键的讨论中,我们可以看到,离子键使离子结合成离子化合物;共价键使原子结合成共价化合物.这种使离子相结合或原子相结合的作用力统称为化学键。化学键\n阅读课本P23讨论:用化学键的观点来分析化学反应的本质是什么?\n化学反应的实质反应物分子被破坏生成物分子生成旧化学键被破坏新化学键的生成吸收能量放出能量一个化学反应的的过程,本质上就是旧化学键断裂和新化学键形成的过程。\n离子键和共价键的比较[小结]离子键共价键成键微粒阴、阳离子原子相互作用静电作用共用电子对成键元素活泼的金属元素(IA,IIA族)和活泼的非金属元素(VIA,IIA族)同种或不同种非金属元素存在离子化合物中某些离子化合物共价化合物非金属单质中\n氢氧化钠晶体中,钠离子与氢氧根离子以离子键结合;在氢氧根离子中,氢与氧以共价键结合。请用电子式表示氢氧化钠。[]+-·H·Na﹕﹕··O过氧化钠晶体中,过氧根离子(O2)2-与钠离子以离子键结合;在过氧根离子中,两个氧原子以共价键结合。请用电子式表示过氧化钠。O··::O··::·Na·Na[]++2-\n小结:元素种类与化学键的种类的关系\n